
【题目】有机化合物P是合成抗肿瘤药物的中间体,其合成路线如下:
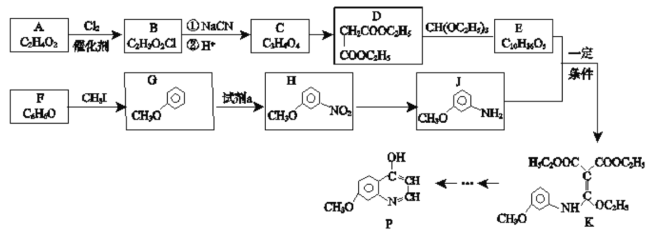
已知:RCl![]() RCOOH
RCOOH
(1)H的官能团名称___________。写出E的结构简式___________。
(2)B→C中①的化学方程式___________。
(3)检验F中官能团的试剂及现象_________。
(4)D的同分异构体有多种,其中满足以下条件的有________种。
①1mol D能与足量 NaHCO3反应放出2mol CO2
②核磁共振氢谱显示有四组峰
(5)H→J的反应类型___________。
(6)已知: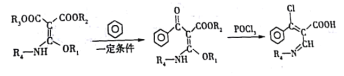
K经过多步反应最终得到产物P:
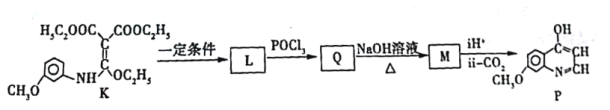
①K→L的化学方程式___________。
②写出M的结构简式___________。
【答案】醚键、硝基 (C2H5OOC)2C=CHOC2H5 ClCH2COOH+NaCN→CNCH2COOH+NaCl FeCl3溶液,显紫色 3 还原反应 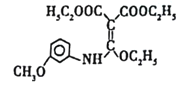
![]()
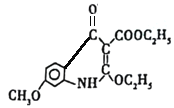 +C2H5OH
+C2H5OH 
【解析】
A和Cl2反应生成B,B中只有1个Cl,所以应该是取代反应,B发生了给出的已知中的反应,所以C中有羧基,C有4个氧原子,而且C的不饱和度为2,再根据D的结构简式,可知C为丙二酸,B为ClCH2COOH,A为CH3COOH。根据K和J的结构简式可知E的结构简式为(C2H5OOC)2C=CH(OC2H5),根据G的结构简式可知F为苯酚。
(1)根据H的结构简式,H的官能团名称为醚键和硝基。E的结构简式为(C2H5OOC)2C=CH(OC2H5)。
(2)B→C中①的化学方程式为ClCH2COOH+NaCN![]() NCCH2COOH+NaCl。
NCCH2COOH+NaCl。
(3)F为苯酚,苯酚遇 FeCl3溶液显紫色,或和浓溴水反应生成三溴苯酚白色沉淀。
(4)D的同分异构体有多种,1mol D能与足量 NaHCO3反应放出2mol CO2,说明1个D分子中有2个羧基。核磁共振氢谱显示有四组峰,说明D分子有比较高的对称性。符合要求的有HOOCCH2CH2CH2CH2CH2COOH、HOOCCH(CH3)CH2CH(CH3)COOH和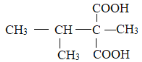 ,共3种。
,共3种。
(5)H→J是H中的硝基变成了氨基,是还原反应。
(6)①根据已知,K→L发生了苯环上的一个氢原子和酯基上的乙氧基断裂结合成乙醇,苯环上的碳原子和断裂乙氧基的碳原子结合成新的碳碳单键的反应,再结合P的结构可知,苯环上断裂的氢原子是和氮原子处于邻位、和甲氧基处于对位的氢原子,所以K→L的化学方程式为:
![]()
 +C2H5OH。
+C2H5OH。
②得到的L继续发生给出的已知的反应,生成Q(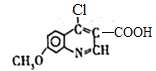 ),Q在NaOH溶液中发生水解,Cl被羟基代替,同时羧基和NaOH发生中和反应生成钠盐,故M的结构简式为
),Q在NaOH溶液中发生水解,Cl被羟基代替,同时羧基和NaOH发生中和反应生成钠盐,故M的结构简式为 。
。


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:
【题目】中药麻黄成分中含有生物碱、黄酮、鞣质、挥发油、有机酚、多糖等许多成分,其中一种有机酚的结构简式如图。下列说法正确的是( )
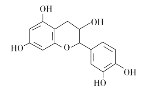
A.分子中所有碳原子可以处于同一平面
B.分子中含有2个手性原子
C.1mol该有机物跟足量浓溴水反应,最多消耗5molBr2
D.1mol该有机物与NaOH溶液反应最多消耗5molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫在自然界的循环过程如图所示。下列说法中,不正确的是
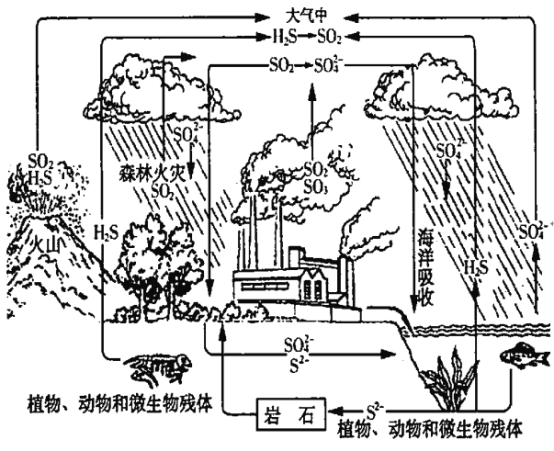
A. 火山喷发、森林火灾会产生SO2
B. 氢、氧两种元素没有参与硫的循环
C. 工厂产生的烟气应经脱硫处理后再排放
D. 硫在自然界的循环过程中,涉及了氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】检验溶液中的离子,实验步骤和结论均正确的是
A.加入AgNO3溶液,有白色沉淀生成,一定含有Cl-离子
B.加入HNO3酸化的Ba(NO3)2溶液有白色沉淀生成,一定含有![]() 离子
离子
C.加入淀粉溶液变蓝,可能含有I2
D.加入BaCl2溶液,有白色沉淀,一定含有![]() 离子
离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学用语回答下列问题:
(1)写出二氧化碳分子的电子式:_____________。
(2)写出氮气分子的结构式_____________。
(3)①CaBr2②H2O③NH4Cl④H2O2⑤HClO⑥I2,只含有离子键的是(用序号回答,下同)_____________,含有共价键的离子化合物是_____________,含有非极性共价键的共价化合物是_____________,常温时为固体,当其熔化时,不破坏化学键的是_____________。
(4)在①![]() Li、②
Li、②![]() N、③
N、③![]() Li、④
Li、④![]() C几种核素中:
C几种核素中:
①_____________和_____________(填序号,下同)互为同位素。
②_____________和_____________的质量数相等,但不能互称同位素。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y是主族元素,I为电离能,单位是KJ/mol.根据下表所列数据判断错误的是( )
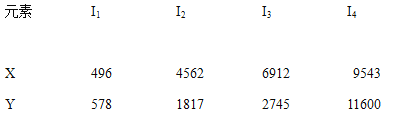
A. 元素X的常见化合价是+1价
B. 元素Y是ⅢA族的元素
C. 元素X与氯形成化合物时,化学式可能是XCl
D. 若元素Y处于第3周期,它可与冷水剧烈反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控。
(1)实验室用金属铜和稀硝酸制取NO的离子方程式为:__________________。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。
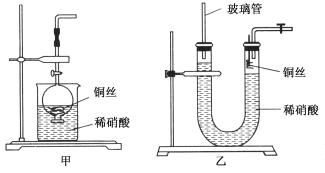
①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________(填选项编号)。
A.铁B.铝C.铂D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是____________________(填化学方程式)。
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反应开始后,可以在U形管右端观察到无色的NO气体。长玻璃管的作用是______________________________________________。
(4)以下收集NO气体的装置,合理的是________(填选项代号)。
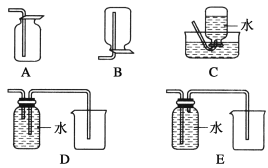
(5)假设实验中12.8gCu全部溶解,需要通入标况下________LO2才能使NO全部溶于水。
(6)用金属铜制取硝酸铜,从节约原料和防止环境污染的角度考虑,下列4种方法中最好的是________(填“甲”、“乙”、“丙”或“丁”),理由是____________________________。
甲:铜+浓硝酸→硝酸铜
乙:铜+稀硝酸→硝酸铜
丙:铜+氯气→氯化铜;氯化铜+硝酸→硝酸铜
丁:铜+空气→氧化铜;氧化铜+硝酸→硝酸铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g) ΔH=-24.8 kJ·mol-1
Fe2O3(s)+![]() CO(g)===
CO(g)===![]() Fe3O4(s)+
Fe3O4(s)+![]() CO2(g) ΔH=-15.73 kJ·mol-1
CO2(g) ΔH=-15.73 kJ·mol-1
Fe3O4(s)+CO(g)===3FeO(s)+CO2(g) ΔH=640.4 kJ·mol-1
则14gCO气体还原足量FeO固体得到Fe固体和CO2气体时对应的ΔH约为( )
A. -218 kJ·mol-1B. -109 kJ·mol-1
C. 218 kJ·mol-1D. 109 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
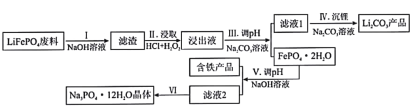
【题目】磷酸亚铁锂(LiFePO4)是目前使用量最多的一种锂电池电极材料,LiFePO4废料中(含Al、石墨)磷、铁、锂的综合回收工艺流程图:
已知:①![]() ,
,![]()
②常温下,![]() ,
,![]() ,
,![]()
(1)过程I“碱浸”的目的是____________,该过程发生反应的离子方程式为_________________。
(2)过程II“酸浸”加人双氧水的目的是_________________。
(3)①浸出液中存在大量![]() 、
、![]() 离子,从平衡移动角度解释过程Ⅲ得到磷酸铁晶体的原因_________________。
离子,从平衡移动角度解释过程Ⅲ得到磷酸铁晶体的原因_________________。
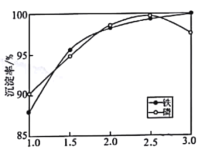
②一定条件下,探究了pH对磷酸铁沉淀的影响,结果如图所示。由图可知,过程Ⅲ应选取的最佳沉淀pH为____。随pH的增加,磷的沉淀率开始下降,而铁沉淀率未下降,分析原因为_________________。
(4)测得滤液1中c(Li+)=0.l5mol/L,某同学取该100mL滤液进行“沉锂”反应.加入50mlNa2CO3溶液却未见沉淀,若不考虑Na2CO3的水解和液体混合时的体积变化,则该同学加入的Na2CO3溶液最大浓度为c(Na2CO3)=_____________mol/L
(5)过程Ⅵ将滤液2________,________,经过滤、干燥后得Na3PO4·12H2O晶体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com