
【题目】化学用语回答下列问题:
(1)写出二氧化碳分子的电子式:_____________。
(2)写出氮气分子的结构式_____________。
(3)①CaBr2②H2O③NH4Cl④H2O2⑤HClO⑥I2,只含有离子键的是(用序号回答,下同)_____________,含有共价键的离子化合物是_____________,含有非极性共价键的共价化合物是_____________,常温时为固体,当其熔化时,不破坏化学键的是_____________。
(4)在①![]() Li、②
Li、②![]() N、③
N、③![]() Li、④
Li、④![]() C几种核素中:
C几种核素中:
①_____________和_____________(填序号,下同)互为同位素。
②_____________和_____________的质量数相等,但不能互称同位素。
【答案】![]() N≡N ① ③ ④ ⑥ ① ③ ② ④
N≡N ① ③ ④ ⑥ ① ③ ② ④
【解析】
(1)二氧化碳分子中,每个碳氧之间形成两对共用电子对,电子式为:![]() ;
;
(2)氮气分子中,氮与氮之间形成三对共用电子对,结构式为:N≡N;
(3)①CaBr2是离子化合物,只含离子键;②H2O是共价化合物,只含极性共价键;③NH4Cl是离子化合物,含离子键和极性共价键;④H2O2是共价化合物,含极性共价键和非极性共价键;⑤HClO是共价化合物,只含极性共价键;⑥I2是单质,只含非极性共价键;所以只含有离子键的是①,含有共价键的离子化合物是③,含有非极性共价键的共价化合物是④,常温时为固体,当其熔化时,不破坏化学键的是⑥。
(4)①同位素指质子数相同中子数不同的同一元素的不同种原子,所以①和③互为同位素。
②②和④的质量数相等,质子数和中子数都不等,所以不能互称同位素。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】有机物苯:常常作为工农业生产中的良好溶剂。
(1)若将苯倒入盛有碘水的试管中,振荡后静置,现象是__________________________,说明苯的密度比水_________,且________________。
(2)若将乒乓球碎片、食盐固体分别加入盛有苯的试管中,振荡后静置,现象是___________________,说明苯是很好的_____________________________。
(3)将盛有苯的两支试管分别插入100℃的沸水和0℃的冰水的现象是________________________,说明苯的沸点_________________,熔点_________。
人们对苯的认识有一个不断深化的过程。
(4)由于苯的含碳量与乙炔相同,人们认为它是一种不饱和烃,写出分子式为C6H6的一种含两个三键且无支链的链烃的结构简式_____________________________________。
(5)已知分子式为C6H6的有机物有多种,其中的两种为:
(I)![]() (II)
(II)![]() 这两种结构的区别表现在以下两方面:
这两种结构的区别表现在以下两方面:
①定性方面(即化学性质方面):(II)能___________(填字母),而(I)不能。
a. 被高锰酸钾酸性溶液氧化 b. 与溴水发生取代反应
c. 与溴发生取代反应 d. 与氢气发生加成反应
②定量方面(即消耗反应物的量的方面):1molC6H6与H2加成时:(I)需要H2______mol,而(II)需要H2_____mol。
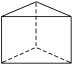
(6)今发现C6H6还可能有另一种如右图所示的立体结构,该结构的一氯代物有_________种;现代化学认为苯分子中碳碳之间的键是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】螺环烃是指分子中两个碳环共用一个碳原子的脂环烃。![]() 是其中一种,下列关于该化合物的说法错误的是( )
是其中一种,下列关于该化合物的说法错误的是( )
A.该化合物的分子式为C9H12
B.一氯代物有四种
C.该化合物可以发生氧化、取代、加成、加聚等反应
D.与Br2以物质的量之比l:1加成生成2种产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知原子序数,可能推断原子的
①质子数 ②中子数 ③质量数 ④核电荷数 ⑤核外电子数
⑥原子结构示意图 ⑦元素在周期表中的位置
A. ①②③④⑥ B. ①④⑤⑥⑦
C. ②③④⑤⑦ D. ③④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酚酞含片是一种治疗消化系统疾病的药物,其有效成分的结构简式如图所示.下列对该有效成分的说法正确的是( )
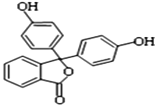
A. 核磁共振氢谱中有5个峰
B. 最多有15个碳原子共平面
C. 可能发生缩聚反应生成高分子化合物
D. 1mol该物质最多能与含4molNaOH的烧碱溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物P是合成抗肿瘤药物的中间体,其合成路线如下:
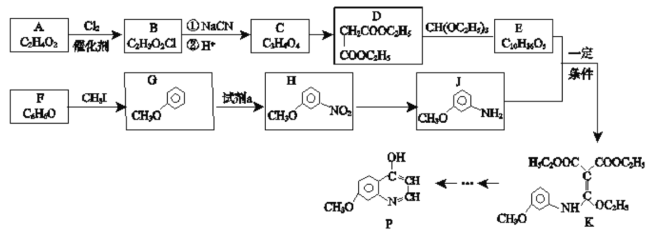
已知:RCl![]() RCOOH
RCOOH
(1)H的官能团名称___________。写出E的结构简式___________。
(2)B→C中①的化学方程式___________。
(3)检验F中官能团的试剂及现象_________。
(4)D的同分异构体有多种,其中满足以下条件的有________种。
①1mol D能与足量 NaHCO3反应放出2mol CO2
②核磁共振氢谱显示有四组峰
(5)H→J的反应类型___________。
(6)已知: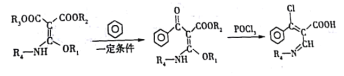
K经过多步反应最终得到产物P:
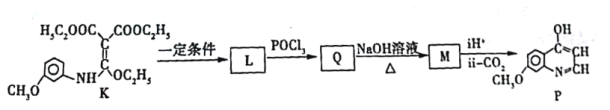
①K→L的化学方程式___________。
②写出M的结构简式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯仿(CHCl3)常因保存不慎而被氧化,产生剧毒物光气(COCl2):2CHCl3+O2―→2HCl +2COCl2。下列说法不正确的有

A. CHCl3分子的空间构型为正四面体
B. COCl2分子中中心C原子采用sp2杂化
C. COCl2分子中所有原子的最外层电子都满足8电子稳定结构
D. 使用前可用硝酸银稀溶液检验氯仿是否变质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe 三种金属元素组成,回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过_______方法区分晶体、准晶体和非晶体。
(2)基态 Fe原子有_______个未成对电子,Fe3+的电子排布式为 _____,可用硫氰化钾检验Fe3+,形成的配合物的颜色为________ 。
(3)新制备的Cu(OH)2可将乙醛〔CH3CHO)氧化成乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道类型为____________,乙酸的沸点明显高于乙醛,其主要原因是________。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有_______个铜原子。
(4)Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为_____ 。列式表示Al单质的密度___________g·cm-3(不必计算出结果)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯氢的制备是目前的研究热点,利用太阳能光伏电池电解水制高纯氢,工作示意图如图所示。下列有关说法正确的是
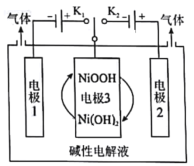
A.连接K1可以制取O2
B.电极2发生反应2H2O+2e-=H2↑+2OH-
C.电极3的主要作用是通过NiOOH和Ni(OH)2相互转化提供电子转移
D.连接K2溶液的pH减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com