
【题目】已知原子序数,可能推断原子的
①质子数 ②中子数 ③质量数 ④核电荷数 ⑤核外电子数
⑥原子结构示意图 ⑦元素在周期表中的位置
A. ①②③④⑥ B. ①④⑤⑥⑦
C. ②③④⑤⑦ D. ③④⑤⑥⑦
科目:高中化学 来源: 题型:
【题目】根据下面的反应路线及所给信息,回答下列问题: 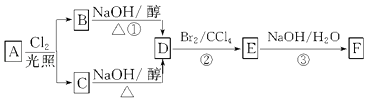
A在氧气中充分燃烧可以产生88g CO2和45g H2O.
(1)A的分子式是 .
(2)B和C均为一氯代烃,反应后只生产D,B、C的名称(系统命名)分别为、 .
(3)D的结构简式 , D中碳原子是否都处于同一平面? .
(4)E的同分异构体的结构简式是 .
(5)①、③的反应类型依次是、 .
(6)写出③的反应化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个6L的密闭容器中,放入3L X(g)和2L Y(g),在一定条件下发生下列反应:4X(g)+3Y(g)=2Q(g)+nR(g),达到平衡后,容器内温度不变,混合气体的压强比原来增加5%,X的浓度减小 ![]() ,则该反应方程式中n的值是( )
,则该反应方程式中n的值是( )
A.3
B.4
C.5
D.6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度相同的NaOH溶液各100 mL倒入A、B、C三个烧杯中,分别向三份溶液中通入不等量
的CO2,充分反应后,再向三份所得溶液中逐滴加入0.2 mol/L的盐酸,产生CO2的体积与
所加盐酸体积之间关系如下图所示。下列判断正确的是
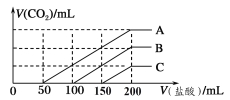
A.通入CO2后,A烧杯中的溶质成分是Na2CO3
B.B烧杯中通入的CO2体积为448 mL
C.原NaOH溶液的浓度为0.2 mol/L
D.通入CO2后,C烧杯中溶质成分的物质的量之比为n(NaOH)∶n(Na2CO3)=1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O ![]() 3Zn(OH)2+2Fe(OH)3+4KOH 下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH 下列叙述不正确的是( )
A.放电时负极反应为:3Zn﹣6e﹣+6OH﹣═3Zn(OH)2
B.充电时阳极反应为:Fe(OH)3﹣3e﹣+5OH﹣═FeO42﹣+4H2O
C.放电时每转移3 mol电子,正极有1 mol K2FeO4被还原
D.充电时阴极溶液的碱性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水中的溶解氧是水生生物生存不可缺少的条件.某课外小组采用碘量法测定学校周边河水中的溶解氧.实验步骤及测定原理如下:
Ⅰ.取样、氧的固定
用溶解氧瓶采集水样,记录大气压及水体温度.将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2 , 实现氧的固定.
Ⅱ.酸化、滴定
在碘量瓶中将因氧后的水样酸化,MnO(OH)2被I﹣还原为Mn2+(该反应放热),在暗处静置5min,然后用标准Na2S2O3溶液滴定生成的I2(2S2O ![]() +I2═2I﹣+S4O
+I2═2I﹣+S4O ![]() )
)
回答下列问题:
(1)“氧的固定”中发生反应的化学方程式为 .
(2)水样酸化后发生反应的离子方程式 .
(3)在碘量瓶(如图)中进行反应,要盖上塞子且在塞子上倒少量水,这样做的目的是 . 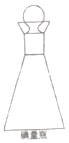
(4)Na2S2O3溶液不稳定,易被氧化,且易受到水中CO2以及微生物的影响而分解,配制该溶液时需要的蒸馏水必须经过煮沸、冷却后才能使用,其目的是 .
(5)Na2S2O3溶液不稳定,使用前需标定,KIO3做其准物标定Na2S2O3溶液的浓度,称取0.214g KIO3与过量的KI作用,析出的碘用Na2S2O3溶液滴定,用去24.00mL,此Na2S2O3溶液的浓度为(已知M(KIO3)=214.0gmol﹣1)
(6)取100.00mL 水样经固氧、酸化后,用该 Na2S2O3溶液滴定,以淀粉溶液作指示剂,终点现象为;若消耗Na2S2O3溶液的体积为10mL,则水样中溶解氧的含量为mgL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以工业生产硼砂所得废渣硼镁泥为原料制取MgSO4H2O的过程如图所示: 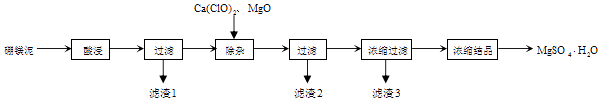
硼镁泥的主要成分如表:
MgO | SiO2 | FeO、Fe2O3 | CaO | Al2O3 | B2O3 |
30%~40% | 20%~25% | 5%~15% | 2%~3% | 1%~2% | 1%~2% |
资料:B2O3溶于水形成硼酸,由于硼酸易溶于水,溶解度随温度的升高而升高,而硫酸镁在80℃溶解度最大,所以常规方法很难将二者分离,目前常采用高温结晶法
回答下列问题:
(1)“滤渣1”中主要含有(写化学式)
(2)“滤渣2”中主要含有(写化学式),判断“除杂”基本完成的检验方法正确的是 .
A.取上层清液,滴加苯酚试液不显紫色
B.取上层清液,滴加KSCN,不变红
C.取上层清液,滴加K3[Fe(CN)6]不产生蓝色沉淀
(3)氧化镁的作用是 . 有同学认为用碳酸镁比用氧化镁要好,原因是 .
(4)分离滤渣3应趁热过滤的原因是 . 分离滤渣3后的母液中含有的溶质是和 , 可以采用加压、的方法得到一水合硫酸镁.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一些含氯产品。

(1)储氯钢瓶中应贴的标签为_________(填字母代号)。
A.易燃品 B.有毒品 C.爆炸品
(2)“威猛先生”使用注意事项中特别说明在使用时切勿与漂白剂一同使用,否则会产生有害气体。“84”消毒液的有效成分是次氯酸钠,写出“84”消毒液与“威猛先生”(有效成分为盐酸)混合后反应的离子方程式_______。
(3)漂白粉的有效成分是_______(填化学式),老师新买的漂白粉没有保存说明书,请你为漂白粉设计一份保存注意事项,并用化学用语解释设计原因。
注意事项(不超过30个字):_________________。
解释(用化学用语):___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青铜(Cu-Zn)是我国最早大量使用的合金,其中锌是现代工业上常用金属。
I. 某废催化剂含58.2%的SiO2(不溶于水和稀酸)、21.0%的ZnO、4.5%的ZnS(不溶于水但溶于稀酸)和12.8%的CuS(不溶于水也不溶于稀酸)。某同学用15.0 g该废催化剂为原料,以稀硫酸和H2O2为试剂,回收其中的锌和铜。
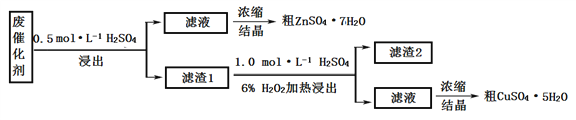
(1)浸出后的操作中,使用到的玻璃仪器有:烧杯、玻璃棒、__________________。
(2)滤渣2是______,第二次浸出发生的反应化学方程式是_________________________。
(3)两次结晶的操作是_________________________________________________________。
(4)某同学在实验完成之后,得到1.5gCuSO4·5H2O(M=250 g·mol–1),则铜的回收率为_______。
II.锌的化学性质与铝相似,锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成Zn(NH3)42+。回答下列问题:
(5)Al溶于NaOH溶液,反应的离子方程式为:_______________________________。
(6)Zn溶于NaOH溶液,反应的化学方程式为:_______________________________。
(7)下列各组中的两种溶液,用相互滴加的实验方法不可鉴别的是____________。
①硫酸铝和氢氧化钠 ②硫酸铝和氨水 ③硫酸锌和氢氧化钠 ④硫酸锌和氨水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com