
【题目】光气(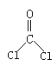 )界面缩聚法合成一种高分子化合物聚碳酸酯G的合成路线如图所示:
)界面缩聚法合成一种高分子化合物聚碳酸酯G的合成路线如图所示:
已知:2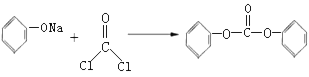 +2NaCl
+2NaCl
(1)C的核磁共振氢谱只有一组吸收峰,C的化学名称为___。
(2)E的分子式为___,H中含有的官能团是氯原子和___,B的结构简式为___。
(3)写出F生成G的化学方程式___。
(4)F与I以1:2的比例发生反应时的产物K的结构简式为___。
(5)H→I时有多种副产物,其中一种含有3个环的有机物的结构简式为___。
(6)4-氯-1,2-二甲苯的同分异构体中属于芳香族化合物的有___种。
(7)写出用2-溴丙烷与D为原料,结合题中信息及中学化学所学知识合成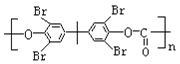 的路线,无机试剂任取。______(已知:一般情况下,溴苯不与NaOH溶液发生水解反应)。
的路线,无机试剂任取。______(已知:一般情况下,溴苯不与NaOH溶液发生水解反应)。
例:CH3CH2OH![]() CH2=CH2
CH2=CH2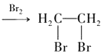
【答案】丙酮 C15H16O2 羧基 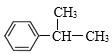 n
n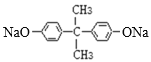 +n
+n ![]()
![]()
![]() +2nNaCl
+2nNaCl 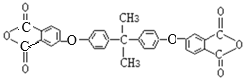
 13
13 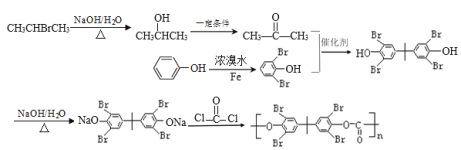
【解析】
A分子式是C3H6,结构简式为CH2=CH-CH3,与苯发生加成反应产生B: ,B在一定条件下反应产生C:
,B在一定条件下反应产生C:![]() 和D:
和D:![]() ,C、D在一定条件下反应产生E:
,C、D在一定条件下反应产生E: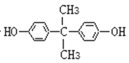 ,E与NaOH溶液反应产生F:
,E与NaOH溶液反应产生F: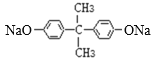 ,F与光气
,F与光气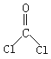 发生反应产生G:
发生反应产生G:![]() ;
;![]() 被酸性KMnO4溶液氧化产生H:
被酸性KMnO4溶液氧化产生H: ,H分子中含有2个羧基,脱去1分子水,生成I:
,H分子中含有2个羧基,脱去1分子水,生成I: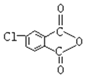 ,F与I以1:2的比例发生反应得到K
,F与I以1:2的比例发生反应得到K  。
。
(7)2-溴丙烷与NaOH的水溶液共热反应产生2-丙醇,然后发生催化氧化产生丙酮;D是![]() ,与浓溴水在Fe作催化剂时发生反应产生
,与浓溴水在Fe作催化剂时发生反应产生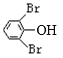 ,丙酮与
,丙酮与 反应产生
反应产生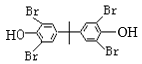 ,该物质与NaOH溶液反应产生
,该物质与NaOH溶液反应产生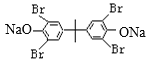 ,
, 与光气反应产生
与光气反应产生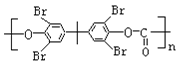 。
。
根据上述分析可知A是CH2=CH-CH3,B是 ,C是
,C是![]() ,D是
,D是![]() ,E:
,E: ,F是
,F是 ,G是
,G是![]() ,H是
,H是 ,I是
,I是 ,K是
,K是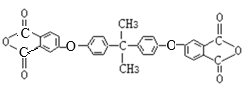 。
。
(1)C结构简式为![]() ,根据物质结构可知C的化学名称为丙酮;
,根据物质结构可知C的化学名称为丙酮;
(2)E结构简式是 ,可知其分子式为C15H16O2,H结构简式为
,可知其分子式为C15H16O2,H结构简式为 ,分子中含有的官能团是氯原子和羧基,B的结构简式为
,分子中含有的官能团是氯原子和羧基,B的结构简式为 。
。
(3)F结构简式是 ,F与光气
,F与光气 发生反应产生G:
发生反应产生G:![]() ;生成G的化学方程式为:n
;生成G的化学方程式为:n +n
+n
![]()
![]() +2nNaCl。
+2nNaCl。
(4)F与I以1:2的比例发生反应时的产物K的结构简式为 。
。
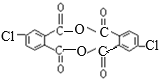
(5)H的结构简式为: ,2个H分子的四个羧基发生分子间脱水反应产生的一种含有3个环的有机物的结构简式为
,2个H分子的四个羧基发生分子间脱水反应产生的一种含有3个环的有机物的结构简式为 。
。
(6)4-氯-1,2-二甲苯的属于芳香族化合物的同分异构体中,若只有一个侧链,可能为-CH2CH2Cl、-CHClCH3两种同分异构体;若有2个侧链,可能是-CH3、-CH2Cl;-Cl、-CH2CH3两种情况,两个取代基的位置有邻、间、对三种位置,因此有两个取代基的同分异构体的种类为2×3=6种;若有三个取代基,分别是-CH3、-CH3、-Cl,取代基三个都相邻的有2种不同的位置,三个取代基都相间的有1种,有两个取代基相邻的有3种不同的情况,所以符合4-氯-1,2-二甲苯的属于芳香族化合物所有同分异构体共有2+6+2+1+3=14种,去掉4-氯-1,2-二甲苯,则4-氯-1,2-二甲苯的芳香族化合物的同分异构体共有13种。
(7)2-溴丙烷与NaOH的水溶液共热反应产生2-丙醇,2-丙醇发生催化氧化产生丙酮;D是![]() ,与浓溴水在Fe作催化剂时发生反应产生
,与浓溴水在Fe作催化剂时发生反应产生 ,丙酮与
,丙酮与 反应产生
反应产生 ,该物质与NaOH溶液反应产生
,该物质与NaOH溶液反应产生 ,
, 与光气反应产生
与光气反应产生 。故合成路线为:
。故合成路线为:
 。
。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】物质的结构决定其性质,元素周期表和元素周期律揭示了化学元素间的内在联系,使其构成了一个完整的体系。回答下列问题:
(1)在硼、氮、氧、氟中,第一电离能由大到小排序为___________(用元素符号表示,下同)。四种元素中的基态原子中,未成对电子数最多的是___________。
(2)已知硼酸的电离方程式为H3BO3+H2O![]() [B(OH)4]+H+。
[B(OH)4]+H+。
①硼酸是___________元酸。
②[B(OH)4]-中含有的化学键类型有___________(填标号)。
a.σ键 b.π键 c.配位键 d.非极性键
③由[B(OH)4]-推出[Al(OH)4]-的结构式为______________________。
(3)氟化硝酰(NO2F)与NO3-的结构相似,则其分子的立体构型是___________,N原子的杂化轨道类型为___________。
(4)已知单质硼晶体的熔点为1873℃,单质硼晶体是___________晶体。
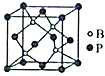
(5)磷化硼(BP)是一种超硬耐磨涂层材料,其立方晶胞如图所示。已知晶胞中B-P键键长均为anm,阿伏加德罗常数的值为NA,则磷化硼晶体的密度为___________g·cm-3(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是
A. 苯佐卡因(![]() )是局部麻醉药,分子中含有2种官能团,分子式为C9H10NO2
)是局部麻醉药,分子中含有2种官能团,分子式为C9H10NO2
B. 香叶醇( )能发生加成反应不能发生取代反应
)能发生加成反应不能发生取代反应
C. 青蒿素(![]() ) 的一氯代物有5种(不含立体异构)
) 的一氯代物有5种(不含立体异构)
D. 某有机物的分子式为C4H8,能使溴的CCl4溶液褪色,则它在一定条件下与水反应时最多可生成的有机物(不考虑立体异构)有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸是一种合成药物达菲的原料,鞣酸存在于苹果、生石榴等植物中。下列关于这两种有机化合物的说法正确的是
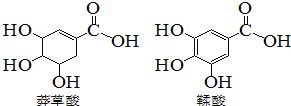
A. 莽草酸分子式为C7H10O5
B. 两种酸都能与溴水发生加成反应
C. 鞣酸分子与莽草酸分子互为同系物
D. 等物质的量的两种酸与足量氢氧化钠反应,消耗氢氧化钠的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与社会、生活及工业生产密切相关。下列有关说法正确的是![]()
A.高炉炼铁、煅烧石灰石和海水提镁的过程中均涉及氧化还原反应
B.煤经过气化和液化等物理变化后,可得到清洁燃料
C.由于![]() 具有较强的氧化性,
具有较强的氧化性,![]() 常用作净水剂
常用作净水剂
D.静电除尘治理悬浮颗粒污染的依据是胶体粒子带有电荷
查看答案和解析>>
科目:高中化学 来源: 题型:
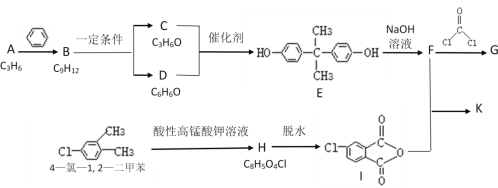
【题目】某研究小组以甲苯为主要原料,采用以下路线合成医药中间体F和Y。
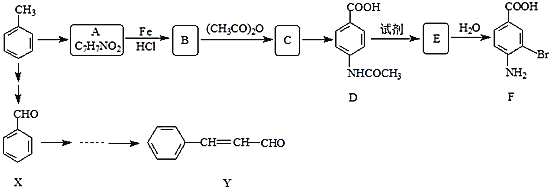
已知:Ⅰ.![]()
![]()
![]()
Ⅱ.2CH3CHO![]()
![]()
Ⅲ.—NH2易被强氧化剂氧化
请回答下列问题:
![]() 写出Y中官能团的名称______;
写出Y中官能团的名称______;
![]() 写出由甲苯
写出由甲苯![]() 反应的化学方程式:______;
反应的化学方程式:______;
![]() 在合成F的过程中,
在合成F的过程中,![]() 步骤不能省略,理由是______,F在一定条件下形成的高分子化合物的结构简式是______;
步骤不能省略,理由是______,F在一定条件下形成的高分子化合物的结构简式是______;
![]() 写出同时符合下列条件的Y的同分异构体的结构简式______;
写出同时符合下列条件的Y的同分异构体的结构简式______;
![]() 苯环上只有两种不同化学环境的氢原子
苯环上只有两种不同化学环境的氢原子
![]() 与
与![]() 溶液反应显紫色
溶液反应显紫色
![]() 分子中只存在一个环状结构
分子中只存在一个环状结构
![]() 结合本题信息和所学知识,以X和乙烯为原料可合成Y,请写出你设计的合成路线______
结合本题信息和所学知识,以X和乙烯为原料可合成Y,请写出你设计的合成路线______![]() 无机试剂及溶剂任选
无机试剂及溶剂任选![]() 。合成路线的书写格式如下:
。合成路线的书写格式如下:
CH3CHO![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g) ![]() 2SO3(g)反应过程的能量变化如图所示。已知 1 molSO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1 。
2SO3(g)反应过程的能量变化如图所示。已知 1 molSO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1 。

请回答下列问题:
(1)图中A、C分别表示____________________、___________________,E的大小对该反应的反应热有无影响?________________。该反应通常用 V2O5 作催化剂,加V2O5会使图中B点升高还是降低?__________, 理由是______________________;
(2)图中ΔH=_____kJ·mol-1;
(3) V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式_____;
(4)已知单质硫的标准燃烧热 ΔH=﹣296 kJ·mol-1,计算由S(s)生成3 mol SO3(g)放出的热量 为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是![]()
![]()
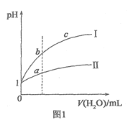

A.图1表示相同温度下![]() 的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强
的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强
B.图2中在b点对应温度下,将![]() 的
的![]() 与
与![]() 的NaOH溶液等体积混合后,溶液显中性
的NaOH溶液等体积混合后,溶液显中性
C.图1中,b点酸的总浓度大于a点酸的总浓度
D.图2中纯水仅升高温度,就可以从a点变到c点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO常用于工业冶炼金属。在不同温度下CO还原四种金属氧化物达平衡后气体中![]() 与温度
与温度![]() 的关系曲线如图。下列说法正确的是
的关系曲线如图。下列说法正确的是
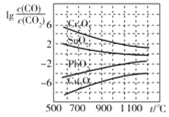
A.通过增高反应炉的高度,增大矿石和CO接触面积,能减少尾气中CO的含量
B.CO不适宜用于工业冶炼金属Cr
C.CO还原![]() 的反应
的反应![]()
D.工业冶炼金属Cu时,高温有利于提高CO的转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com