
����Ŀ�������������ڹ�ũҵ�����ж�����ҪӦ�á�
��1���£�N2H4���������ᷴӦ�����ɵ�����һ���⻯��ڱ�״���£����⻯��������ܶ�Ϊ1.92g/L�������е�Ԫ�ص���������Ϊ0.977����÷�Ӧ�Ļ�ѧ����ʽΪ____.
��2������������һ�������£����Է������·�Ӧ��SO2(g)+NO2(g)![]() SO3(g)+NO(g) ��H= -42kJ��mol-1����2L�ĺ����ܱ������г���SO2(g)��NO2(g)����ʵ���������£�
SO3(g)+NO(g) ��H= -42kJ��mol-1����2L�ĺ����ܱ������г���SO2(g)��NO2(g)����ʵ���������£�
ʵ���� | �¶� | ��ʼ���ʵ���mol | ƽ��ʱ���ʵ���/mol | |
n(SO2) | n(NO2) | n(NO) | ||
�� | T1 | 4.0 | 1.0 | 0.9 |
�� | T2 | 1.0 | 4.0 | 0.8 |
�� | T2 | 0.4 | 0.6 | a |
����ʵ����У���2minʱ��÷ų���������8.4kJ��0��2minʱ���ڣ���SO2��ʾ��ƽ����Ӧ����v(SO2)=_______________�����¶��µ�ƽ�ⳣ��Ϊ_________�������������С�������λ��
���ɱ������ݿ���֪��T1_______T2������>����<������=����
��ʵ����У��ﵽƽ��ʱNO2��ת����Ϊ______________.
��3����ҵ�Ͽ����ð�ˮ��SO2ת��ΪNH4HSO3����������(NH4)2SO4�������²��NH4HSO3��ҺpHΪ6������Һ��![]() ________________________.����֪��H2SO3��Kal =1.5��10-2Ka2 =1.0��10-7��
________________________.����֪��H2SO3��Kal =1.5��10-2Ka2 =1.0��10-7��
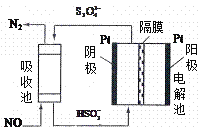
��4��ʹ�ü�ӵ绯ѧ�����Դ���ú�����е�NO��װ����ͼ����֪������Һ��pH��4��7֮�䣬д�������ĵ缫��Ӧʽ__________________��
 ��
��
���𰸡� N2H4+HNO2��HN3+2H2O 0.05 mol��L-1��min-1 2.61 �� 40�� 1500 2HSO3��+2e����S2 O42��+2OH����2HSO3��+2e��+2H+��S2 O42��+2H2O
����������1���£�N2H4���������ᷴӦ�����ɵ�����һ���⻯��ڱ�״���£����⻯��������ܶ�Ϊ1.92g/L������⻯���Ħ������Ϊ![]() ����֪���е�Ԫ�ص���������Ϊ0.977������⻯�������Nԭ�ӵ���ĿΪ
����֪���е�Ԫ�ص���������Ϊ0.977������⻯�������Nԭ�ӵ���ĿΪ![]() ����ˣ������ʽΪHN3���÷�Ӧ�Ļ�ѧ����ʽΪN2H4+HNO2��HN3+2H2O.
����ˣ������ʽΪHN3���÷�Ӧ�Ļ�ѧ����ʽΪN2H4+HNO2��HN3+2H2O.
��2������ʵ����У���2minʱ��÷ų���������8.4kJ����0��2minʱ����SO2�ı仯��Ϊ0.2mol����SO2��ʾ��ƽ����Ӧ����v(SO2)=![]() 0.05 mol��L-1��min-1���ﵽƽ��ʱ��NO�ı仯��Ϊ0.9mol���������������ʵı仯��Ҳ��0.9mol��SO2��NO2��SO3��NO��ƽ�����ֱ�Ϊ3.1mol��0.1mol��0.9mol��0.9mol��SO2��NO2��SO3��NO��ƽ��Ũ�ȷֱ�Ϊ1.55mol/L��0.05mol/L��0.45mol/L��0.45mol/L�����¶��µ�ƽ�ⳣ��Ϊ
0.05 mol��L-1��min-1���ﵽƽ��ʱ��NO�ı仯��Ϊ0.9mol���������������ʵı仯��Ҳ��0.9mol��SO2��NO2��SO3��NO��ƽ�����ֱ�Ϊ3.1mol��0.1mol��0.9mol��0.9mol��SO2��NO2��SO3��NO��ƽ��Ũ�ȷֱ�Ϊ1.55mol/L��0.05mol/L��0.45mol/L��0.45mol/L�����¶��µ�ƽ�ⳣ��Ϊ![]() 2.61��
2.61��
���ɱ������ݿ�֪������Ͷ��������൱����NO��ƽ������С�����ҵ�ƽ�ⳣ����С�����ڸ÷�Ӧ�Ƿ��ȷ�Ӧ������T1��T2��
����ʵ���ҿ�������÷�Ӧ��T2�¶��µ�ƽ�ⳣ��Ϊ1����ʵ�����NO2��ת����Ϊx����NO2�ı仯��Ϊ0.6x�������������ʵı仯��Ҳ��0.6x��SO2��NO2��SO3��NO��ƽ��Ũ�ȷֱ�Ϊ0.2-0.3x��0.3-0.3x��0.3x��0.3x������![]() ����֮��x=0.4�����ԣ��ﵽƽ��ʱNO2��ת����Ϊ40��.
����֮��x=0.4�����ԣ��ﵽƽ��ʱNO2��ת����Ϊ40��.
��3�������²��NH4HSO3��ҺpHΪ6��c(![]() )
)![]() ��Kal
��Kal ![]() Ka2 =
Ka2 =![]() 1.5��10-2
1.5��10-2![]() 1.0��10-7=1.5��10-9������Һ��
1.0��10-7=1.5��10-9������Һ��![]() .
.
��4�������е������Һ��pH��4��7֮�䣬��ͼ����Ϣ��֪��HSO3���������ϱ���ԭΪS2 O42�����������ĵ缫��Ӧʽ2HSO3��+2e����S2 O42��+2OH����2HSO3��+2e��+2H+��S2 O42��+2H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ý�屨��,����һ�ҹ�˾Tiamat��ǰ�з����ȵ�ǰ�㷺ʹ�õ�﮵�سɱ����͡���������������ٶȸ���������ӵ��,Ԥ�ƴ�2020�꿪ʼʵ�ֹ�ҵ�������õ�صĸ�������ΪNa2Co2TeO6(�Ʊ�ԭ��ΪNa2CO3��Co3O4��TeO2)�����ҺΪNaClO4��̼���ϩ����Һ��
�ش���������:
��1��Te����Ԫ�����ڱ���_____��Ԫ��,���̬ԭ�ӵļ۵����Ų�ʽΪ_____��
��2����̬Naԭ����,�������ռ�ݵ�ԭ�ӹ������Ϊ____,����ܲ����������ͼ��״Ϊ_____
��3�����������Ϣ�ж�:C��O��Cl�ĵ縺���ɴ�С��˳��Ϊ_____(��Ԫ�ط��ű�ʾ)��
��4��CO32-�ļ��ι���Ϊ______;̼���ϩ���Ľṹ��ʽ��ͼ��ʾ,������̼ԭ�ӵ��ӻ��������Ϊ_________,1mol̼���ϩ���м�����ĿΪ________.

��5��[Co(H2O)6]3+�ļ��ι���Ϊ����������,������_____,�������Ӱ�����������Ϊ__(��ѡ����ĸ)��
A.���Ӽ� B.���Լ� C.��λ�� D.��� E.������
��6��Na��O�γɵ����ӻ�����ľ����ṹ��ͼ��ʾ,������O����λ��Ϊ______,�þ������ܶ�Ϊ��g/cm3,�����ӵ�������ֵΪNA����Na��O֮�����̾���Ϊ_____cm(�ú�����NA�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
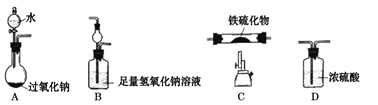
����Ŀ��ijѧϰС��������ͼװ��(�г�װ����ȥ)�ⶨij������(FexSy)����ɡ�
[ʵ�鲽��]
��1����װ�����������ĸ�װ�õ���ȷ����˳��Ϊ____��
��2�����װ�������ԣ�Ӧ��β�����____��
��3������ҩƷ����ʼʵ�飺Ӧ��____��һ��ʱ�����____��
��4��ֹͣ��Ӧ����Ӳ�ʲ������й����������ٸı�ʱ��ֹͣ���ȣ�����ͨ�롪��ʱ���O2����Ŀ����____��
��5���ⶨSԪ�ص���������B��������Һ��ˮ���Ƴ�250 mL��Һ��ȡ25.00 mL������Һ������������˫��ˮ���ټ������������ữ��BaCl2��Һ�������ó������ˡ�ϴ�ӡ������������Ϊ2.33g��֮ǰ��ȡ�����������Ϊ6g����FexSy�Ļ�ѧʽΪ____��
[ʵ�鷴˼����̽��]
��6����ͬѧ��Ϊ���裨5���������Ϊ��ȡ25��00 mL������Һ������������BaCl2��Һ�������ó������ˡ�ϴ�ӡ�����Ƶ�BaSO3����������������Ϊ�˷���____(��ǡ���)������������____��
��7����ͬѧΪ�˼���̽����Ӧ��Ӳ�ʲ������й���ijɷ֣���������ȡ������ȫ����ϡ�����У�������Һ�м���K3Fe(CN)6��Һ��δ�۲쵽����������Ӳ�ʲ���������������Ӧ�Ļ�ѧ����ʽΪ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ�� ![]() +
+ ![]()
![]()
![]() ���Ҫ�ϳɻ�����A����ṹΪ��
���Ҫ�ϳɻ�����A����ṹΪ�� ![]() ����˵������ȷ���ǣ�������
����˵������ȷ���ǣ�������
A.������A��HBr �������ʵ���1��1�ӳ�ʱ�������ֲ�ͬ�IJ���
B.�÷�Ӧ��ԭ���Ǽӳɷ�Ӧ
C.�ϳ�A��ԭ�Ͽ����ǣ���Ȳ��2��3��������1��3������ϩ
D.�ϳ�A��ԭ�Ͽ����ǣ�2����Ȳ��2������1��3������ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���¶�ΪTʱ����2.0L�����ܱ������г���1.0mol PCl5 �� ��ӦPCl5��g��PCl3��g��+Cl2��g������һ��ʱ���ﵽƽ�⣮��Ӧ�����вⶨ�IJ������ݼ���������˵����ȷ���ǣ�������
t/s | 0 | 50 | 150 | 250 | 350 |
n��PCl3��/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A.��Ӧ��ǰ50s��ƽ������v��Cl2��=0.0016 molL��1min��1
B.���������������䣬�����¶ȣ�ƽ��ʱc��PCl3��=0.11 molL��1 �� ��÷�Ӧ�ġ�H��0
C.�¶�ΪTʱ����ʼʱ�������г���1.0 mol PCl5��0.20 mol PCl3��0.20 mol Cl2 �� ��Ӧ�ﵽƽ��ǰv��������v���棩
D.�¶�ΪTʱ����ʼʱ�������г���0.5 mol PCl3��0.5 mol Cl2 �� �ﵽƽ��ʱ��PCl3��ת����С��80%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������¡����ݵ��ܱ������н��������������淴Ӧ��(��)2X(g)![]() Y(g)+Z(s)�� (��)A(s)+2B(g)
Y(g)+Z(s)�� (��)A(s)+2B(g)![]() C(g)+D(g)�����������������ٷ����仯ʱ�����Ա������Ҿ��ﵽƽ��״̬����
C(g)+D(g)�����������������ٷ����仯ʱ�����Ա������Ҿ��ﵽƽ��״̬����
�ٻ�������ܶ�
�ڷ�Ӧ������������İٷֺ���
�۷�Ӧ����������������������������֮�ȵ��ڻ�ѧ������֮��
�ܻ�������ѹǿ
�ݹ�������
�������������ʵ���
A���٢ڢۢܢݢ� B���٢ڢۢ� C���٢ڢ� D���ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ��Ƽ����³ɹ��Ȼ�����гɹ��л��ŵ���������ǣ� ��
A.����ܽ���ϡ��������ȡ����B.�����Ϸ��ֿ�ű��ҩ������
C.�ɶ����з������ѽ����D.������Ȼ��ˮ�����Բ�����60��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
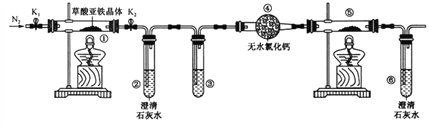
����Ŀ��������������(FeC2O4��2H2O)��һ�ֵ���ɫ��ĩ��ij����С����������װ�ü�����������������ȷֽ�IJ��ֲ��
����˵����ȷ����
A. ���ۺ͢��зֱ�ʢ������NaOH��Һ��CuO���ɼ������ɵ�CO
B. ʵ��ʱֻ��Ҫ��װ�â��з�Ӧ��������ͨ��N2
C. �������е���ˮCaCl2������ˮ����ͭ�ɼ���ֽ����ɵ�ˮ����
D. ʵ��������е���ɫ��ĩ��ȫ��ɺ�ɫ�������һ��Ϊ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����298 Kʱ��ʵ������Һ�еķ�ӦH2O2��2HI===2H2O��I2�ڲ�ͬŨ��ʱ�Ļ�ѧ��Ӧ���������ʾ���ɴ˿���֪��5��ʵ����c(HI)��c(H2O2)������Ϊ
ʵ���� | 1 | 2 | 3 | 4 | 5 | 6 |
c(HI)/(mol��L��1) | 0.100 | 0.200 | 0.150 | 0.100 | �� | 0.500 |
c(H2O2)/(mol��L��1) | 0.100 | 0.100 | 0.150 | 0.200 | �� | 0.400 |
v/(mol��L��1��s��1) | 0.007 60 | 0.015 2 | 0.017 1 | 0.015 2 | 0.022 8 | 0.152 |
A. 0.150 mol��L��1��0.200 mol��L��1
B. 0.300 mol��L��1��0.100 mol��L��1
C. 0.200 mol��L��1��0.200 mol��L��1
D. 0.100 mol��L��1��0.300 mol��L��1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com