
【题目】碳酸锰是制取其他含锰化合物的原料,也可用作脱硫的催化剂等。一种焙烧氯化铵和菱锰矿粉制备高纯度碳酸锰的工艺流程如图所示
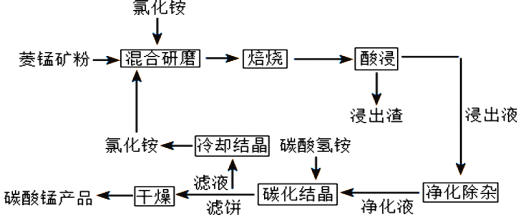
已知①菱锰矿粉的主要成分是MnCO3,还有少量的Fe、Al、Ca、Mg等元素
②常温下,相关金属离子在浓度为0.1mol/L时形成M(OH)n沉淀的pH范围如表
金属离子 | Al3+ | Fe3+ | Fe2+ | Ca2+ | Mn2+ | Mg2+ |
开始沉淀的pH | 3.8 | 1.5 | 6.3 | 10.6 | 8.8 | 9.6 |
沉淀完全的pH | 5.2 | 2.8 | 8.3 | 12.6 | 10.8 | 11.6 |
回答下列问题:
(1)“混合研磨”的作用为_______________________
(2)“焙烧”时发生的主要反应的化学方程式为_________________________________
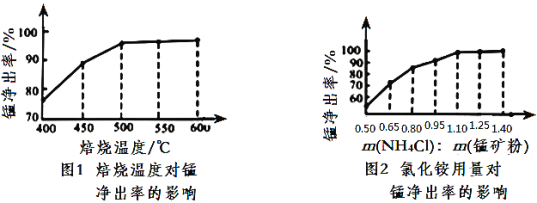
(3)分析图1、图2,焙烧氯化铵、菱锰矿粉的最佳条件是_____________________________
(4)净化除杂流程如下
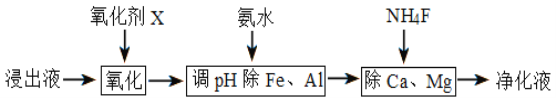
①已知几种物质氧化能力的强弱顺序为(NH4)2S2O8>KMnO4>MnO2>Fe3+,则氧化剂X宜选择__________
A.(NH4)2S2O8 B.MnO2 C.KMnO4
②调节pH时,pH可取的范围为_________________
(5)“碳化结晶”过程中不能用碳酸铵代替碳酸氢铵,可能的原因是__________________
【答案】加快反应速率 MnCO3+2NH4Cl=MnCl2+2NH3↑+CO2↑+H2O 温度为500℃,且m(MnCO3):m(NH4Cl)=1.10 B 5.2≤pH<8.8 CO32-水解程度大于HCO3-,易生成氢氧化物沉淀
【解析】
菱锰矿的主要成分为MnCO3,加入氯化铵焙烧发生MnCO3+2NH4Cl![]() MnCl2+CO2↑+2NH3↑+H2O↑,气体为二氧化碳和氨气、水蒸气,浸出液中含MnCl2、FeCl2、CaCl2、MgCl2、AlCl3等,结合表中离子的沉淀pH及信息可知,浸取液净化除杂时加入少量MnO2氧化亚铁离子为铁离子,加氨水调pH,生成沉淀氢氧化铁和氢氧化铝,加入NH4F,除去Ca2+、Mg2+,净化液加入碳酸氢铵碳化结晶过滤得到碳酸锰,据此分析解题。
MnCl2+CO2↑+2NH3↑+H2O↑,气体为二氧化碳和氨气、水蒸气,浸出液中含MnCl2、FeCl2、CaCl2、MgCl2、AlCl3等,结合表中离子的沉淀pH及信息可知,浸取液净化除杂时加入少量MnO2氧化亚铁离子为铁离子,加氨水调pH,生成沉淀氢氧化铁和氢氧化铝,加入NH4F,除去Ca2+、Mg2+,净化液加入碳酸氢铵碳化结晶过滤得到碳酸锰,据此分析解题。
(1)“混合研磨”可增大反应物的接触面积,加快反应速率;
(2) 根据流程,菱镁矿粉与氯化铵混合研磨后焙烧得到氨气、二氧化碳和Mn2+,主要化学反应方程式为:MnCO3+2NH4Cl![]() MnCl2+2NH3↑+CO2↑+H2O;
MnCl2+2NH3↑+CO2↑+H2O;
(3) 由图可知,锰的浸出率随着焙烧温度、氯化铵与菱镁矿粉的质量之比增大而提高,到500℃、1.10达到最高,再增大锰的浸出率变化不明显,故氯化铵焙烧菱镁矿的最佳条件是焙烧温度500℃,氯化铵与菱镁矿粉的质量之比为1.10;
(4) 净化过程:加入少量MnO2氧化亚铁离子为铁离子,加氨水调pH,生成沉淀氢氧化铁和氢氧化铝,加入NH4F,除去Ca2+、Mg2+;
①最合适的试剂为MnO2,氧化亚铁离子,反应的离子方程式为:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O,且不引入新杂质,故答案为B;
②调节溶液pH使Fe3+,A13+沉淀完全,同时不使Mn2+沉淀,根据表中数据可知调节溶液pH范围5.2≤pH<8.8;
(5) 碳化结晶中生成MnCO3的离子方程式为Mn2++HCO3-+NH3═MnCO3↓+NH4+,不用碳酸铵溶液替代NH4HCO3溶液,可能的原因是碳酸铵溶液中的c(OH-)较大,会产生Mn(OH)2沉淀。


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一密闭容器中进行,则下列说法或结论中,正确是( )
CO(g)+H2(g)在一密闭容器中进行,则下列说法或结论中,正确是( )
A.保持压强不变,充入少量氦气,反应速率会减小
B.若v(CO)=v(H2O),则反应达平衡状态
C.其他条件不变,适当增加C(s)的质量会使反应速率增大
D.其他条件不变,仅将容器的体积缩小一半,反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、硫、氯及其化合物是中学化学重要的组成部分。
(1)氨气燃料电池使用的电解质溶液是KOH溶液,电池反应为:4NH3+3O2=2N2+6H2O。该电池负极的电极反应式为__________;用该电池进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,以CuSO4溶液为电解质溶液,下列说法正确的是________。
a.电能全部转化为化学能
b.SO42﹣的物质的量浓度不变(不考虑溶液体积变化)
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
e.若阳极质量减少64g,则转移电子数为2NA个
(2)①将SO2通入到BaCl2溶液中,出现了异常现象,看到了明显的白色沉淀,为探究该白色沉淀的成分,他设计了如下实验流程:所得悬浊液![]() 白色沉淀
白色沉淀![]() 观察现象并判断,则试剂A的化学式为_________。实验表明,加入试剂A后,白色沉淀未见溶解,产生该白色沉淀的离子方程式是________。
观察现象并判断,则试剂A的化学式为_________。实验表明,加入试剂A后,白色沉淀未见溶解,产生该白色沉淀的离子方程式是________。
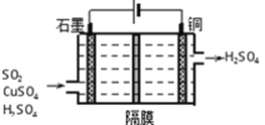
②利用如图所示电化学装置吸收工业尾气中SO2,阴极上生成Cu。写出装置中阳极的电极反应式_________。
(3)已知Ksp(BaSO4)=1.0×10﹣10,Ksp(BaCO3)=2.5×10-9。某同学设想用下列流程得到BaCl2,BaSO4![]() BaSO3
BaSO3![]() BaCl2。则①的离子方程式为________,该反应的平衡常数K=_________。
BaCl2。则①的离子方程式为________,该反应的平衡常数K=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨晶体结构中的某一种的某一部分。
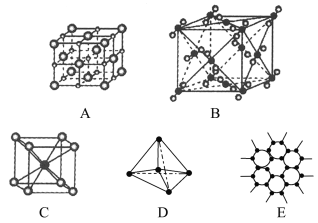
(1)其中代表金刚石的是(填编号字母,下同)________,其中每个碳原子与________个碳原子最接近且距离相等。金刚石属于________晶体。
(2)其中代表石墨的是________,其中每个正六边形占有碳原子数平均为________个。
(3)其中代表NaCl晶体的是________,每个Na+周围与它最接近且距离相等的Na+有________个。
(4)代表CsCl晶体的是________,它属于________晶体,每个Cs+与________个Cl-紧邻。
(5)代表干冰的是________,它属于________晶体,每个CO2分子与________个CO2分子紧邻。
(6)上述五种物质熔点由高到低的排列顺序为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气与氧气生成水的反应是氢能源应用的重要途径。下列有关说法正确的是
A. 一定温度下,反应2H2(g)+O2(g) ![]() 2H2O(g)能自发进行,该反应的ΔH<0
2H2O(g)能自发进行,该反应的ΔH<0
B. 氢氧燃料电池的负极反应为O2+2H2O+4e![]() 4OH
4OH
C. 常温常压下,氢氧燃料电池放电过程中消耗11.2 L H2,转移电子的数目为6.02×1023
D. 反应2H2(g)+O2(g) ![]() 2H2O(g)的ΔH可通过下式估算:
2H2O(g)的ΔH可通过下式估算:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D都是短周期元素,A元素的原子核外有两个电子层,最外层已达到饱和,B元素位于A元素的下一周期,最外层的电子数是A元素最外层电子数的![]() ,C元素的离子带有两个单位正电荷,它的核外电子排布与A元素原子相同,D元素与C元素属同一周期,D元素原子的最外层电子数比C的最外层电子数少1。
,C元素的离子带有两个单位正电荷,它的核外电子排布与A元素原子相同,D元素与C元素属同一周期,D元素原子的最外层电子数比C的最外层电子数少1。
根据上述内容判断
(1)A______、B______、C______、D______(填元素符号)。
(2)B元素位于第_______周期_______族,B的最高价氧化物的化学式是______,其最高价氧化物的水化物是一种______酸(填强或弱)。
(3)在C与D的单质中,与冷水反应较剧烈的反应的离子方程式是______。
(4)C离子的核外电子排布式为______;D原子的核外电子排布式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在其他条件不变时,只改变某一条件,化学反应aA(g)+B(g)![]() cC(g)的平衡的变化图象如下(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率),据此分析下列说法正确的是
cC(g)的平衡的变化图象如下(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率),据此分析下列说法正确的是

A. 在图象反应Ⅰ中,说明正反应为吸热反应
B. 在图象反应Ⅰ中,若p1>p2,则此反应的ΔS>0
C. 在图象反应Ⅱ中,说明该正反应为吸热反应
D. 在图象反应Ⅲ中,若T1>T2,则该反应能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属及其相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)下列关于金属及金属键的说法不正确的是______。(填字母代号)
a.金属键没有方向性与饱和性
b.金属键是金属原子与自由电子间的相互作用
c.金属熔沸点不同的原因可以用金属键强弱解释
d.电子气理论可解释金属材料的延展性,不能解释金属有良好的导电性
(2)钒广泛用于催化及钢铁工业,基态钒原子的价层电子排布图为_________________。
(3)二茂铁又叫双环戊二烯基铁[Fe(C5H5)2],熔点是172.5~173 ℃,100 ℃以上升华,二茂铁属于_____晶体。已知分子中的大π键可用符号![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为![]() )。已知二茂铁的每个茂环带有一个单位负电荷,则每个环中的大π键应表示为________________。
)。已知二茂铁的每个茂环带有一个单位负电荷,则每个环中的大π键应表示为________________。
(4)铜可以形成一种离子化合物[Cu(NH3)4(H2O)2]SO4,若要确定[Cu(NH3)4(H2O)2]SO4是晶体还是非晶体,最科学的方法是对其进行______实验,其中阴离子的空间构型是_____,该化合物加热时首先失去的组分是H2O,原因是_______________________。
(5)最近发现,只含镁、镍和碳三种元素的晶体也具有超导性,该物质形成的晶体的立方晶胞结构如图所示。
①与Mg紧邻的Ni有________个。
②原子坐标参数可表示晶胞内部各原子的相对位置。该晶胞中原子的坐标参数为a为(0,0,0);b为(1/2,1/2,0);d为(1,1,1)。则c原子的坐标参数为_______。
③若晶胞中Ni、Mg之间的最短距离为a pm,阿伏加德罗常数的值为NA,则晶体的密度ρ=______g·cm-3(用含a、NA的代数式表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1923年,在汉阳兵工厂工作的我国化学家吴蕴初先生研制出了廉价生产味精的方案,并于1926年向英、美、法等化学工业发达国家申请专利。这也是历史上中国的化学产品第一次在国外申请专利。以下是利用该方法合成味精的流程![]() 部分产物及反应条件已省略
部分产物及反应条件已省略![]() :
:
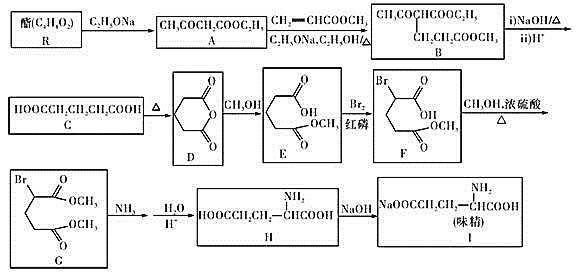
请回答下列问题:
![]() 下列有关蛋白质和氨基酸的说法不正确的是________
下列有关蛋白质和氨基酸的说法不正确的是________![]() 填字母代号
填字母代号![]() 。
。
![]() 蛋白质都是高分子化合物
蛋白质都是高分子化合物
![]() 谷氨酸
谷氨酸![]() 自身不能发生反应
自身不能发生反应
![]() 氨基酸和蛋白质都能发生盐析
氨基酸和蛋白质都能发生盐析
![]() 天然蛋白质水解的最终产物都是
天然蛋白质水解的最终产物都是![]() 氨基酸
氨基酸
![]() 的系统命名是________;F中含氧官能团的名称是_______________。
的系统命名是________;F中含氧官能团的名称是_______________。
![]() 的反应类型是____________,R的结构简式为_______________。
的反应类型是____________,R的结构简式为_______________。
![]() 写出G和
写出G和![]() 反应的化学方程式:_________________。
反应的化学方程式:_________________。
![]() 是H的同分异构体,T中同时具备下列条件的结构有________种。其中在核磁共振氢谱上有4组峰且峰的面积比为
是H的同分异构体,T中同时具备下列条件的结构有________种。其中在核磁共振氢谱上有4组峰且峰的面积比为![]() 的可能结构简式为_______。
的可能结构简式为_______。
![]() 能发生水解反应
能发生水解反应
![]() 只有2种官能团,其中一种是
只有2种官能团,其中一种是![]()
![]() 发生银镜反应能生成
发生银镜反应能生成![]() 银
银
![]() 参照上述流程,以
参照上述流程,以![]() 和甲醇为原料
和甲醇为原料![]() 其他无机试剂任选
其他无机试剂任选![]() ,设计合成苯丙氨酸
,设计合成苯丙氨酸![]()
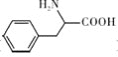
![]() 的流程:_____________________。
的流程:_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com