
【题目】化学上常用燃烧法确定有机物的组成,如下图所示装置是用燃烧法确定烃或烃的含氧衍生物分子式的常用装置,这种方法是在电炉加热时用纯氧氧化管内样品,根据产物的质量确定有机物的组成。

完成下列问题:
(1)A中发生反应的化学方程式为_______________________________________。
(2)B装置的作用是_______________________________________________,燃烧管C中CuO的作用是______________________________________________________。
(3)产生氧气按从左向右流向,燃烧管C与装置D、E的连接顺序是:C→________→__________。
(4)反应结束后,从A装置锥形瓶内的剩余物质中分离出固体,需要进行的实验操作是_____________。
(5)准确称取 1.8 g 烃的含氧衍生物X的样品,经充分燃烧后,D管质量增加 2.64 g ,E管质量增加 1.08 g ,则该有机物的实验式是___________________________。实验测得X的蒸气密度是同温同压下氢气密度的45倍,则X的分子式为_________________________,1 mol X分别与足量Na、NaHCO 3 反应放出的气体在相同条件下的体积比为1∶1,X可能的结构简式为____________________。
【答案】(1) 2H2O![]() 2H2O+O2↑;(2)吸收氧气中的水蒸气(或答:干燥氧气) ,使有机物不完全燃烧的产物全部转化为CO2 和H2 O ;(3)E,D ;(4)过滤;(5)CH2 O,C3 H6 O3 ,HOCH 2 CH 2 COOH、
2H2O+O2↑;(2)吸收氧气中的水蒸气(或答:干燥氧气) ,使有机物不完全燃烧的产物全部转化为CO2 和H2 O ;(3)E,D ;(4)过滤;(5)CH2 O,C3 H6 O3 ,HOCH 2 CH 2 COOH、 ![]() 。
。
【解析】
试题分析:(1)装置A的作用是制备氧气,用MnO2作催化剂,使H2O2分解,其反应方程式为2H2O![]() 2H2O+O2↑;(2)实验目的是有机物的燃烧,测有机物的组成,氧气中的水蒸气干扰实验,必须除去,B中盛放浓硫酸,作用是干燥氧气,CuO的作用是防止有机物不完全燃烧产生CO,CO还原CuO,使得有机物中的碳原子全部转化成CO2;(3)碱石灰的作用是吸收CO2,无水CaCl2的作用是吸收H2O,因此是E、D;(4)MnO2不溶于水,因此通过过滤的方法得到;(5)D管增重2.64g,增重的是CO2,即n(C)=2.64/44mol=0.06mol,E管增重的是水的质量,则有n(H)=1.08×2/18mol=0.12mol,因此有m(O)=(1.8-0.06×12-0.12×1)g=0.96g,即n(O)=0.96/16mol=0.06mol,三种原子的比值为0.06:0.12:0.06=1:2:1,最简式为CH2O,是同温同压下,氢气密度的45倍,即分子量为90,则有机物的分子式为C3H6O3,能与NaHCO3反应说明含有羧基,1molX和NaHCO3反应产生1molCO2,和金属钠反应产生氢气也是1mol,说明含有羟基,则结构简式为:HOCH2CH2COOH、CH3CH(OH)COOH。
2H2O+O2↑;(2)实验目的是有机物的燃烧,测有机物的组成,氧气中的水蒸气干扰实验,必须除去,B中盛放浓硫酸,作用是干燥氧气,CuO的作用是防止有机物不完全燃烧产生CO,CO还原CuO,使得有机物中的碳原子全部转化成CO2;(3)碱石灰的作用是吸收CO2,无水CaCl2的作用是吸收H2O,因此是E、D;(4)MnO2不溶于水,因此通过过滤的方法得到;(5)D管增重2.64g,增重的是CO2,即n(C)=2.64/44mol=0.06mol,E管增重的是水的质量,则有n(H)=1.08×2/18mol=0.12mol,因此有m(O)=(1.8-0.06×12-0.12×1)g=0.96g,即n(O)=0.96/16mol=0.06mol,三种原子的比值为0.06:0.12:0.06=1:2:1,最简式为CH2O,是同温同压下,氢气密度的45倍,即分子量为90,则有机物的分子式为C3H6O3,能与NaHCO3反应说明含有羧基,1molX和NaHCO3反应产生1molCO2,和金属钠反应产生氢气也是1mol,说明含有羟基,则结构简式为:HOCH2CH2COOH、CH3CH(OH)COOH。


科目:高中化学 来源: 题型:
【题目】某化合物由两种单质直接反应生成,将其加入Ba(HCO3)2溶液中同时有气体和沉淀产生。下列化合物中符合上述条件的是 ( )
A.A1Cl3 B.Na2O C.NaAl(OH)4 D.SiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作和实验事故处理不正确的是
A. 用蘸浓盐酸的玻璃棒靠近盛放氨气的装置,检査是否漏气
B. 浓硫酸沾在皮肤上,立刻用稀氢氧化钠溶液冲洗
C. 液溴应保存在棕色磨口玻璃塞的试剂瓶中,并加少量水进行水封
D. 为防止被氧化,FeSO4溶液存放在加有少量铁粉的试剂瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.8g的甲烷含有0.5NA共价键
B.乙醇与水任意比互溶与氢键有关
C.离子化合物中不可能有共价键
D.所有物质都存在范德华力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度(通过CO2与样品反应后生成O2的量测定Na2O2的含量)。

回答下列问题:
(1)装置B的作用是_____________;装置C的作用是____________;装置E中碱石灰的作用是_______。
(2)装置D中发生反应的化学方程式是:_________________。
(3)若开始时测得样品的质量为2.0g,反应结束后测得气体体积为224mL(标准状况),则Na2O2试样的纯度为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是( )
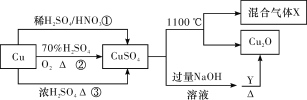
A.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3∶2
B.相对于途径①、③,途径②更好地体现了绿色化学思想
C.1 mol CuSO4在1100 ℃所得混合气体X中O2为0.75 mol
D.Y可以是葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁香醛是常用的一种食用香精。存在下列转化关系:
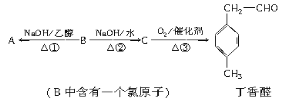
(1)B的分子式为________,C中含氧官能团的名称为________。
(2)反应②的化学方程式为____________________________________。
(3)A发生加聚反应所得产物的结构简式为________________。
(4)与A含有相同官能团的芳香族化合物的同分异构体还有________种(不考虑顺反异构),其中只有一个取代基且不含甲基的物质的结构简式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面给出的是元素周期表的一部分,表中所列小写字母分别代表一种化学元素。
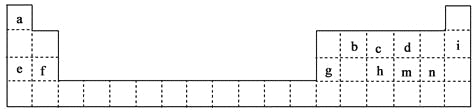
(1)根据上表回答下列问题: ①上述元素中形成物质种类最多的是_________(填元素符号),m的阴离子结构示意图为_________。
②h、m、n所形成的最高价氧化物的水化物的酸性由强到弱的顺序为_________(填化学式)。
③d、e、f、g形成的简单离子的半径由小到大的顺序为_________(用离子符号填写)。
(2)下列能够用来比较m、n两种元素非金属性强弱的有_________。
A.比较这两种元素的气态氢化物的稳定性
B.将这两种元素的单质分别与氢氧化钠溶液反应
C.将n的单质通入到m的氢化物的水溶液中
(3)分别写出下列反应的离子方程式:
g、d形成的化合物 与e、d、a形成化合物的水溶液反应
c的气态氢化物与其最高价氧化物对应的水化物反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在100 mL 0.8mol/L硝酸溶液中加入足量铜粉,则被溶解的铜的质量为____________g。
(2)在上述溶液中再加入足量稀硫酸,又有_______g铜溶解。此过程中生成的气体在标准状况下的体积为_________L。
(3)若向100 mL 0.8mol/L硝酸溶液中加入铁粉,测得反应后的溶液中Fe2+与Fe3+的浓度之比为1:1,则加入铁的质量为____________g。
(4)向100 mL 0.8mol/L硝酸溶液中加入一定量Fe、FeO、Fe2O3的混合物,充分反应后,放出气体224mL(标准状况下),且测得溶液中铁元素只以Fe2+形式存在,为使Fe2+完全沉淀,可向反应后的溶液中加入0.1mol/L的NaOH溶液___________mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com