
【题目】按要求书写下列反应的方程式:
(1)NO2 溶于水的化学反应方程式:_____。
(2)实验室制取氨气的化学反应:_____。
(3)足量的 SO2 气体通入到 NaOH 中的离子反应方程式:______________。
(4)红热的碳和浓硝酸的化学反应方程式:_____。
【答案】3NO2+H2O=2HNO3+NO 2NH4Cl+Ca(OH)2![]() 2NH3↑+ CaCl2 + 2H2O SO2+OH- = HSO3- 4HNO3(浓)+C
2NH3↑+ CaCl2 + 2H2O SO2+OH- = HSO3- 4HNO3(浓)+C![]() CO2↑+4NO2↑+2H2O
CO2↑+4NO2↑+2H2O
【解析】
(1)NO2 溶于水生成硝酸和一氧化氮,其化学反应方程式为:3NO2+H2O=2HNO3+NO,故答案为:3NO2+H2O=2HNO3+NO;
(2)实验室用氯化铵和氢氧化钙制取氨气,其化学反应方程式为:2NH4Cl+Ca(OH)2![]() 2NH3↑+ CaCl2 + 2H2O,故答案为:2NH4Cl+Ca(OH)2
2NH3↑+ CaCl2 + 2H2O,故答案为:2NH4Cl+Ca(OH)2![]() 2NH3↑+ CaCl2 + 2H2O;
2NH3↑+ CaCl2 + 2H2O;
(3)足量的 SO2 气体通入到 NaOH 中生成亚硫酸氢钠,其离子反应方程式为:SO2+OH- = HSO3-,故答案为:SO2+OH- = HSO3-;
(4)红热的碳和浓硝酸反应生成二氧化碳、二氧化氮和水,其化学反应方程式为:4HNO3(浓)+C![]() CO2↑+4NO2↑+2H2O,故答案为:4HNO3(浓)+C
CO2↑+4NO2↑+2H2O,故答案为:4HNO3(浓)+C![]() CO2↑+4NO2↑+2H2O;
CO2↑+4NO2↑+2H2O;


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】中科院一项最新成果实现了甲烷高效生产乙烯,甲烷在催化作用下脱氢,在气相中经自由基偶联反应生成乙烯,其反应如下:2CH4(g)C2H4(g)+2H2(g) ΔH>0
化学键 | H—H | C—H | C=C | C—C |
E(kJ/mol) | a | b | c | d |
(1)已知相关化学键的键能如上表,甲烷制备乙烯反应的ΔH=____________ (用含a、b、c、d的代数式表示)。
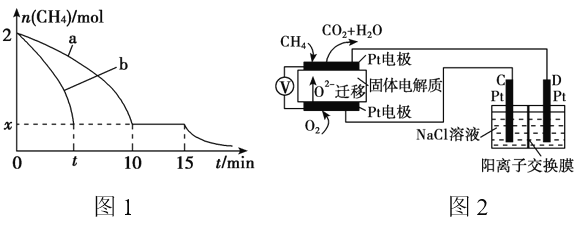
(2)T1温度时,向1 L的恒容反应器中充入2mol CH4 ,仅发生上述反应,反应过程中 0~15min CH4的物质的量随时间变化如图1,测得10~15min时H2的浓度为1.6mol/L。
①0~10min内CH4表示的反应速率为__________mol/(L·min)。
②若图1中曲线a、曲线b分别表示在温度T1时,使用质量相同但表面积不同的催化剂时,达到平衡过程中n(CH4)变化曲线,其中表示催化剂表面积较大的曲线是 ________ (填“a”或 “b”)。
③15min时,若改变外界反应条件,导致n(CH4)发生图1中所示变化,则改变的条件可能是_____________________________________(任答一条即可)。
(3)实验测得v正=k正c2(CH4),v逆=k逆c(C2H4)·c2(H2)其中k正、k逆为速率常数仅与温度有关,T1温度时k正与k逆的比值为______ (填数值)。若将温度由T1升高到T2,则反应速率增大的倍数v正____v逆(填“>”“=”或“<”),判断的理由是_________________ 。
(4)科研人员设计了甲烷燃料电池并用于电解。如图2所示,电解质是掺杂了 Y2O3与 ZrO2的固体,可在高温下传导O2-。
①C极的Pt为______ 极(填“阳”或“阴” )。
②该电池工作时负极反应方程式为_____________________。
③用该电池电解饱和食盐水,一段时间后收集到标况下气体总体积为112mL,则阴极区所得溶液在25℃时pH=_______ (假设电解前后NaCl溶液的体积均为500mL)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知断裂 1 mol 共价键所需要吸收的能量分别为 H-H 键:436 kJ;I-I 键:153 kJ;H-I 键:299 kJ。下列对反应 H2(g)+I2(g)2HI(g)的判断中,错误的是( )
A.该反应是放出能量的反应B.该反应是吸收能量的反应
C.该反应是氧化还原反应D.I2 与 H2 具有的总能量大于生成的 HI 具有的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸![]() 是一种精细磷化工产品,具有较强还原性,
是一种精细磷化工产品,具有较强还原性,![]() 可用电渗析法制备。“四室电渗析法”工作原理如图所示
可用电渗析法制备。“四室电渗析法”工作原理如图所示![]() 阳膜和阴膜分别只允许阳离子、阴离子通过
阳膜和阴膜分别只允许阳离子、阴离子通过![]() ,回答下列问题:
,回答下列问题:

![]() 写出阳极的电极反应式:________。
写出阳极的电极反应式:________。
![]() 请判断离子交换膜类型:A________,B________。
请判断离子交换膜类型:A________,B________。![]() 填“阴膜”或“阳膜”
填“阴膜”或“阳膜”![]()
![]() 早期采用“三室电渗析法”制备
早期采用“三室电渗析法”制备![]() :将“四室电渗析法”中阳极室的稀硫酸用
:将“四室电渗析法”中阳极室的稀硫酸用![]() 稀溶液代替,并撤去阳极室与产品室之间的离子交换膜,从而合并了阳极室与产品室。其缺点是产品中混有________杂质,该杂质产生的原因是________。
稀溶液代替,并撤去阳极室与产品室之间的离子交换膜,从而合并了阳极室与产品室。其缺点是产品中混有________杂质,该杂质产生的原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向恒容密闭容器中加入2mol X和4 mol Y,发生如下反应:X(s)+2Y(g)![]() 2Z(g),此反应达到平衡的标志是
2Z(g),此反应达到平衡的标志是
A.容器内压强不随时间变化B.V正(X)=2V逆(Z)
C.容器内X、Y、Z的浓度相等D.容器内气体密度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银是一种在工业、生活上有广泛用途的金属。
已知:①金属在水中存在如下溶解平衡过程:M![]() Mx+ + xe-,
Mx+ + xe-,
氢气在水溶液中也存在如下平衡过程:H2![]() 2H++ 2e-
2H++ 2e-
②Ag2S 的Ksp=6.7×10-50; AgCl的Ksp=1.6×10-10
据此回答下列有关问题:
(1)银质餐具可杀菌消毒,原因是_________________(用适当的方程式和文字表述说明);金属银与氢硫酸可反应生成黑色固体和无色气体,写出该反应的化学方程式_______________
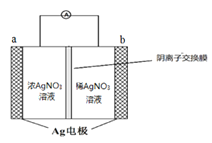
(2)金属银与硝酸银溶液组成电池示意图如右,a电极的反应为________________,NO3-从电池________侧溶液向电池_______侧溶液移动 (填“左”或“右”)。
(3)硝酸银见光或受热易分解为Ag、NO2、O2,反应中生成NO2、O2的 物质的量之比为___________,将混合气体通过水吸收后,剩余气体为________________
(4)已知:Ag+(aq) + 2NH3H2O(aq)![]() [Ag(NH3)2]+(aq) + 2H2O K=1.6×107,写出AgCl溶于氨水的离子方程式________________________;计算该反应的平衡常数K=___________。在氯化银溶于氨水后的溶液中滴加稀硝酸,会再产生白色氯化银沉淀,滴加硝酸至刚好沉淀完全,取上层清液测其pH,发现呈酸性,主要原因是_______________(用离子方程式表示)。
[Ag(NH3)2]+(aq) + 2H2O K=1.6×107,写出AgCl溶于氨水的离子方程式________________________;计算该反应的平衡常数K=___________。在氯化银溶于氨水后的溶液中滴加稀硝酸,会再产生白色氯化银沉淀,滴加硝酸至刚好沉淀完全,取上层清液测其pH,发现呈酸性,主要原因是_______________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图所示。下列说法错误的是( )
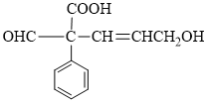
A.该有机物的分子式为C12H12O4
B.1 mol该有机物最多能与4 mol H2反应
C.该有机物可与NaHCO3溶液反应放出CO2,生成2.24 L CO2(标准状况下)需要0.1 mol该有机物
D.该有机物可发生氧化、取代、加成和还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,电解质溶液的性质与变化是多样的,下列说法正确的是( )
A. pH相同的①CH3COONa ②NaClO ③NaOH三种溶液c(Na+)大小:①>②>③
B. 往稀氨水中加水,![]() 的值变小
的值变小
C. pH=4的H2S溶液与pH=10的NaOH溶液等体积混合,存在下列等式:c(Na+)+c(H+)c=(OH—)+2c(S2—)
D. Ca(ClO)2溶液中通入少量CO2,ClO—水解程度增大,溶液碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维生素B3可以维持身体皮肤的正常功能,而且具有美容养颜的功效,其分子中六元环的结构与苯环相似。下列有关维生素B分子的说法错误的是
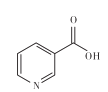
A.所有的碳原子均处于同一平面B.与硝基苯互为同分异构体
C.六元环上的一氯代物有4种D.1mol该分子能和4mol H2发生加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com