
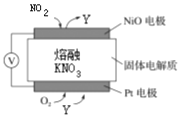
【题目】(1)通过NOx传感器可监测NOx的含量,其工作原理示意图如下图。回答下列问题:
①Pt电极上还需通入的气体是________。
②写出NiO电极的电极反应式:_____________________________________________。
(2)盐桥电池是一种比较普遍的原电池,该电池反应原理如下图所示。
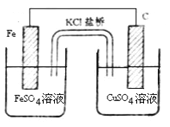
①负极电极反应式为________。
②当电路中通过电子为0.1mol时,两电极质量差为___g,此时原电池电解质溶液的总质量与开始时电解质溶液总质量差值为___g(不考虑溶液离子向盐桥移动)。
【答案】 N2O5 NO2-e-+NO3-=N2O5 Fe-2 e-= Fe2+ 6 7.05
【解析】本题主要考查原电池原理。
(1)①Pt电极上为了使O2转化而来的O2-成为NO3-,还需通入的气体是N2O5。
②NiO电极的电极反应式:NO2-e-+NO3-=N2O5。
(2)①负极是铁电极反应式为Fe-2 e-= Fe2+。
②当电路中通过电子为0.1mol时,负极消耗0.05mol即2.8gFe,正极得到0.05nol即3.2gCu,两电极质量差为(2.8+3.2)g=6g,负极产生0.05mol即2.8gFe2+,正极消耗0.05nol即3.2gCu2+,盐桥中0.1mol即7.45gKCl移向溶液,此时原电池电解质溶液的总质量与开始时电解质溶液总质量差值为(2.8-3.2+7.45)g=7.04g。


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】现有三组混合物:①汽油和氯化钠溶液;②乙醇的水溶液;③溴的水溶液,分离以上各混合液的正确方法依次是
A.分液、萃取、蒸馏B.分液、蒸馏、萃取
C.萃取、蒸馏、分液D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来雾霾天气经常肆虐北京、天津、河北等地区,其中汽车尾气和燃煤是造成空气污染的原因之一。因此研究氮氧化物的反应机理,对消除和防治环境污染有重要意义。
(1) 对于2NO(g) + 2H2(g) = N2(g) + 2H2O(g) △H = 665 kJ/mol 的反应分三步完成:
① 2NO(g) = N2O2(g) (快)
② N2O2(g) + H2(g) = N2O(g) + H2O(g) (慢)
③ ______________________________ (快),请完成第③步的化学方程式。因此决定此总反应速率的是第_____步的反应。(填序号)
(2) 已知:H2(g) + CO2(g) = H2O(g) + CO(g) △H = + 41 kJ/mol汽车尾气的净化原理主要是用催化剂把NO与CO反应转化为两种对大气无污染的气体,试写出该反应的热化学方程式:______________。
该反应在一定条件下达到平衡后,为了能加快反应速率并让反应向正方向移动,可采取的措施有:(__________)
A.适当升高温度 B.适当降低温度 C.压缩体积增大压强 D.使用正催化剂
该反应采取上述措施重新达到平衡后K值将______(填“增大”、“减小”和“不变”)
(3) 升高温度能让绝大多数的化学反应加快反应速率,但是研究发现2NO(g) + O2(g) = 2NO2(g) △H < 0 存在一些特殊现象。现有某化学小组通过实验测得不同温度下该反应速率常数k (代表反应速率的一个常数)的数值如下表:
T(K) | k | T(K) | k | T(K) | k |
143 | 1.48 × 105 | 273 | 1.04 × 104 | 514 | 3.00 × 103 |
195 | 2.58 × 104 | 333 | 5.50 × 103 | 613 | 2.80 × 103 |
254 | 1.30 × 104 | 414 | 4.00 × 103 | 663 | 2.50 × 103 |
由实验数据测到v(正)~c(O2)的关系如图所示,当x点升高到某一温度时,反应重新达到平衡,则变为相应的点为_____点(填字母),并解析原因:①__________,②__________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下2 mL 1 mol·L-1 NaHCO3溶液,pH约为8,向其中滴加几滴饱和CaCl2溶液,有白色沉淀和无色气体生成。下列说法中,不正确的是
A. NaHCO3溶液中,HCO3-水解程度大于其电离程度
B. NaHCO3溶液中,c(Na+) > c(HCO3-) > c(OH-) > c(H+)
C. 最终所得的混合溶液中,c(Na+) + c(H+) = c(HCO3-) + 2c(CO32-)+ c(OH-)
D. 滴加饱和CaCl2溶液促进了HCO3-的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是________
A. KMnO4 B. H2O2 C. Cl2 水 D. HNO3
然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的________
A. NaOH B. NH3·H2O C. CuO D. Cu(OH)2
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为________,Fe3+完全沉淀时溶液的pH为________,通过计算确定上述方案________(填“可行”或“不可行”)(已知lg2=0.3)
(3)同学们用0.1000 mol·L-1的酸性高锰酸钾标准溶液滴定某试样中过氧化氢的含量,反应原理为2MnO4-+5H2O2+6H+===2Mn2++8H2O+5O2↑。
①滴定到达终点的现象是______________________________________。
②用移液管吸取25.00 mL试样置于锥形瓶中,重复滴定四次,每次消耗的酸性KMnO4标准溶液体积如下表所示:
第一次 | 第二次 | 第三次 | 第四次 | |
体积(mL) | 17.10 | 18.10 | 17.00 | 16.90 |
则试样中过氧化氢的浓度为___________mol·L-1。
③若滴定前尖嘴中有气泡,滴定后消失,则测定结果______(填“偏低”、“偏高”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解Na2CO3溶液制取NaHCO3溶液和NaOH溶液的装置如下图所示。下列说法中,不正确的是

A. 阴极产生的物质A是H2
B. 溶液中Na+由阳极室向阴极室迁移
C. 阳极OH﹣放电,H+浓度增大,CO32-转化为HCO3-
D. 物质B是NaCl,其作用是增强溶液导电性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设想合成具有以下结构的四种烃分子,下列有关说法错误的是

A. 1mol甲分子内含有10mol共价键 B. 乙分子的一氯取代产物只有一种
C. 丙分子的二氯取代产物只有两种 D. 丁分子显然是不可能合成的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com