
【题目】I.如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液。回答下列问题:

锌为__极,该电极上发生__反应(“氧化”或“还原”),电极反应式为__,该原电池的总反应离子方程式为__.
II.(1)氮化钠的电子式是_____________。
(2)氮化钠与水反应的化学方程式是__________________。
(3)氮化钠与盐酸反应生成_______种盐。
(4)氮化钠中两种微粒的半径大小比较: r(Na+)___r(N3-)(填“大于”、“小于”或“等于”)。
【答案】 负 氧化 Zn﹣2e﹣=Zn2+ Zn+Cu2+=Zn2++Cu ![]() Na3N+H2O=NH3+3NaOH )两 小于
Na3N+H2O=NH3+3NaOH )两 小于
【解析】I.锌的金属性强于铜,锌为负极,该电极上发生氧化反应,电极反应式为Zn-2e-=Zn2+,正极是银,溶液中铜离子得到电子,该原电池的总反应离子方程式为Zn+Cu2+=Zn2++Cu。
II.(1)氮化钠是离子化合物,电子式是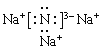 。(2)氮化钠与水反应生成氢氧化钠和氨气,反应的化学方程式是Na3N+H2O=NH3↑+3NaOH。(3)氮化钠与盐酸反应生成氯化铵和氯化钠两种盐。(4)氮化钠中两种微粒的核外电子排布相同,离子半径随原子序数的增大而减小,则 r(Na+)小于r(N3-)。
。(2)氮化钠与水反应生成氢氧化钠和氨气,反应的化学方程式是Na3N+H2O=NH3↑+3NaOH。(3)氮化钠与盐酸反应生成氯化铵和氯化钠两种盐。(4)氮化钠中两种微粒的核外电子排布相同,离子半径随原子序数的增大而减小,则 r(Na+)小于r(N3-)。


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:
【题目】化学在生活中有着广泛的应用,下列对立关系正确的是( )
选项 | 化学性质 | 实际应用 |
A | SO2具有还原性 | 漂白纸浆 |
B | HF具有弱酸性 | 在玻璃上刻字, |
C | 铝的金属活动性强于氢 | 用铝制容器贮运浓硝酸 |
D | FeCl3溶液能与Cu反应 | 蚀刻铜箔制造电路板 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子可能大量共存的是
A. 不能使酚酞试液变红的无色溶液中:Na+、CO![]() 、K+、ClO-、AlO
、K+、ClO-、AlO![]()
B. 常温下水电离出的c(H+)·c(OH-)=10-20的溶液中:Na+、Cl-、S2-、SO![]()
C. 能与金属铝反应放出氢气的溶液中: K+、NO![]() 、Cl-、NH
、Cl-、NH![]()
D. 含有HCO![]() 的溶液中:K+、OH-、NO
的溶液中:K+、OH-、NO![]() 、Ca2+
、Ca2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过渡元素由于其特殊的核外电子排布而其有特殊的性质,成为化学研究的重点和前沿。
(l)过波元素处于周期表的____区和f 区。
(2)过渡元素能形成简单化合物,还能形成多种配位化合物
① 通常,d轨道全空或全满的过渡金属离子与水分子形成的配合物无颜色,否则有颜色。如[Co(H2O)6]2+显粉红色,据此判断,[Mn(H2O)6]2+____(填“有”或“无”)颜色。
② Ni2+可形成多种配合物,如Ni(CN)42-。写出CN-的电子式____,若其中两个CN-被NO2-替换,得到的配合物只有两种结构,则Ni(CN)42-的空间构型是_____, NO2-的空间构型是_____,其中N原子的杂化方式是_____。
③ 从结构角度分析并比较CoF2与CoCl2晶体的熔点高低___________。
(3)金、铜等金属及合金可用作生产石墨烯的催化剂,下图是一种铜金合金的晶胞示意图:

① 在该铜金合金的晶体中,与Cu原子距离相等且最近的Au原子数为_______。
② 原子坐标参数是用来表示晶胞内部各原子相对位置的指标,若A的原子坐标参数为(0,0,0);B的原子坐标参数为(0,1,0) , C的原子坐标参数为(l,0,0)。则D的原子子坐标参数为_________。
③ 若Au、Cu原子半径分别为r1和r2,则该晶胞中的原子空间利用率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量的铝分别与等物质的量浓度的稀硫酸和氢氧化钠溶液反应,放出的气体体积在标准状况下相等,则所取稀硫酸和氢氧化钠溶液的体积比为 ( )
A. 1︰2 B. 3︰2 C. 3︰1 D. 6︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于Al(OH)3的性质叙述错误的是( )
A. Al(OH)3受热易分解生成Al2O3和H2O
B. Al(OH)3是难溶于水的白色胶状物质
C. Al(OH)3能凝聚水中的悬浮物,也能吸附色素
D. Al(OH)3既能溶于NaOH溶液、氨水,又能溶于盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验中常将溶液或试剂进行酸化,下列酸化处理的措施正确的是
A. 定性检验SO![]() ,将BaCl2溶液用HNO3酸化
,将BaCl2溶液用HNO3酸化
B. 为提高高锰酸钾溶液的氧化能力,用盐酸将高锰酸钾溶液酸化
C. 检验溶液中是否含有Fe2+时,用硝酸酸化
D. 检验溶液中是否含有SO![]() 时,在无其他阳离子干扰的条件下,先用盐酸酸化,所得溶液再加BaCl2溶液
时,在无其他阳离子干扰的条件下,先用盐酸酸化,所得溶液再加BaCl2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用相同体积的0.1mol· L-1的BaCl2溶液,能分别使相同体积的Fe2(SO4)3、ZnSO4、Na2SO4溶液的SO42-完全沉淀,则三种溶液的物质的量浓度之比为( )
A. 3∶2∶1 B. 1∶2∶3 C. 3∶1∶1 D. 1∶3∶3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com