
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A.78g 苯含有C=C双键的数目为3NA
B.1L 1mol·L -1的Na2CO3溶液中含有阴离子的数目大于NA
C.常温常压下,14g由N2与CO组成的混合气体含有的原子数目为2NA
D.标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】 Fe和Mg与H2SO4反应的实验如下:
实验 |
|
|
|
|
现象 | Fe表面产生大量无色气泡 | Fe表面产生气泡后迅速停止 | Mg表面迅速产生大量气泡 | Fe表面有大量气泡,Mg表面有少量气泡 |
关于上述实验说法不合理的是( )
A.I中产生气体的原因是:Fe + 2H+=Fe2++ H2↑
B.取出Ⅱ中的铁棒放入CuSO4溶液立即析出亮红色固体
C.Ⅲ中现象说明Mg在浓H2SO4中没被钝化
D.Ⅳ中现象说明Mg的金属性比Fe强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种电池的正极材料,可通过下列方法制得:
①称取一定量的固体铁氧体磁性材料溶于过量盐酸,接着先后加入双氧水和氢氧化钠溶液,静置24 h,过滤
②将沉淀加入反应瓶中,加入过量的氢氟酸溶液,80'c恒温加热24 ha
③蒸发多余氢氟酸和水,得淡红色FeF3凝胶
④在干燥箱中,以100℃预处理6 h,最后掺入铁氧体磁性材料混合研磨制得正极材料
(1)加入双氧水的作用是______(用离子方程式表示)
(2)步骤②的反应瓶材质可能是____(填序号)
A.玻璃 B.陶瓷 C.聚四氟乙烯
(3)加氢氟酸反生反应的化学方程式为____
(4)从安全的角度考虑,在实验室里制三氟化铁时应在____中进行
(5)三氟化铁与Li在固体电解质铁氧体中发生置换反应,产生的电流可供电脑使用,该电池反应的化学方程式为________
(6)取上述铁氧体样品溶于足量盐酸,在通入标准状况下672 mL C12, Fe2+恰好被完全氧化成Fe3十,然后把溶液蒸干,灼烧至恒重得9. 6 g固体,则该铁氧体的化学式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g)![]() C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
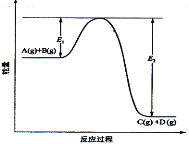
(1)该反应是__________________反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率______(填“增大”“减小”“不变”),原因是__________________;
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_________,E2________(填“增大”“减小、”“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)N2、CO2、SO2三种气体的物质的量比为1∶1∶1时,它们的分子个数比为___________;质量比为___________;同温、同压下体积之比为___________。
(2) 同温同压下,质量相同的四种气体: ① CO2 ② H2 ③ O2 ④ CH4
所占的体积由大到小的顺序是(填序号,下同)______ ______; 密度由大到小的顺序是__________。
(3) 22.2 g CaR2含R-0.4 mol,则CaR2的摩尔质量为___________,R的相对原子质量为___________。
(4) 将质量比为14 :15的N2和NO混合,则混合气体中N2和NO的物质的量之比为_________,氮原子和氧原子的个数比为___________,该混合气体的平均摩尔质量为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既属于氧化还原反应,又属于放热反应的是
A.灼热的碳与二氧化碳的反应 B.盐酸与烧碱溶液的反应。
C.乙醇在空气中的燃烧 D.氢氧化钡晶体与氯化铵晶体在常温下的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各图所示实验设计能达到相应实验目的的是

A. 用图①装置验证氯、碳、硅元素非金属性
B. 用图②装置能收集O2、CO2和H2
C. 用图③装置电解精炼铝
D. 用图④装置验证NaHCO3和Na2CO3的热稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于气体制备的说法不正确的是( )
A.用碳酸钠粉末可以制备CO2
B.用铁片和稀H2SO4反应制取H2时,为加快产生H2的速率可改用浓H2SO4
C.加热分解NH4HCO3固体,将所得的气体进行适当处理可获得NH3
D.用KMnO4固体和用KClO3固体制备O2的装置完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是几种常见弱酸的电离平衡常数(25 ℃)
酸 | 电离方程式 | 电离平衡常数K |
CH3COOH | CH3COOH | 1.76×10-5 |
H2CO3 | H2CO3 HCO3- | K1=4.4×10-7 K2=4.7×10-11 |
H2S | H2S HS- | K1=1.3×10-7 K2=7.1×10-15 |
H3PO4 | H3PO4 H2PO4- HPO42- | K1=7.1×10-3 K2=6.3×10-8 K3=4.20×10-13 |
回答下列问题:
(1)当温度升高时,K值________(填“增大”“减小”或“不变)。
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关系?___________________。
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、H2PO4-、HPO42-都看作是酸,其中酸性最强的是________,最弱的是________。
(4)多元弱酸是分步电离的,每一步都有相应的电离平衡常数,对于同一种多元弱酸的K1、K2、K3之间存在着数量上的规律,此规律是________,产生此规律的原因是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com