
【题目】某校化学兴趣小组根据反应:H2O2+2HI=2H2O+I2探究影响化学反应速率的因素。实验数据如下:
实验 编号 | H2O2溶液浓度/(mol·L-1) | HI溶液浓度/(mol·L-1) | 温度/℃ | 反应速率/(mol·L-1·s-1) |
① | 0.1 | 0.1 | 25 | 0.0076 |
② | 0.1 | 0.2 | 25 | 0.0153 |
③ | 0.1 | 0.3 | 25 | 0.0227 |
④ | 0.1 | 0.1 | 35 | 0.0304 |
回答下列问题:
(1)反应:H2O2+2HI=2H2O+I2中,氧化剂是___。
(2)25℃时,表明增大反应物浓度,化学反应速率___(填“增大”或“减小”)。
(3)能表明温度对化学反应速率影响的实验编号是①和___。
(4)H2O2不稳定,写出H2O2发生分解反应的化学方程式:___。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】下图为某燃煤电厂处理废气的装置示意图,下列说法错误的是
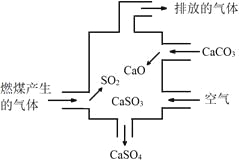
A.使用此装置可以减少导致酸雨的气体的排放
B.该装置内既发生了化合反应,也发生了分解反应
C.总反应可表示为:2SO2+ 2CaCO3 + O2=2CaSO4+ 2CO2
D.若排放的气体能使澄清石灰水变浑浊,说明该气体中含SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是温度和压强对X+3Y![]() 2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
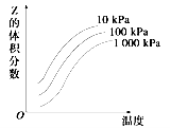
A.上述反应的正反应ΔH>0
B.升高温度,化学平衡常数K减小
C.X、Y、Z均为气态
D.当Y的浓度不再发生变化时,该反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中充入1mol N2和3molH2,一定条件下发生反应N2(g) + 3H2(g) ![]() 2NH3(g),达到化学平衡时,下列说法正确的是( )
2NH3(g),达到化学平衡时,下列说法正确的是( )
A.反应停止了B.正逆反应速率相等
C.N2的浓度为0D.H2的转化率为100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置或操作能达到实验目的的是
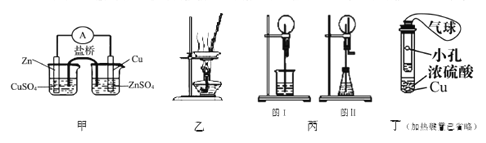
A. 甲装置构成铜锌原电池
B. 用图乙所示装量加热AlCl3饱和溶液然后利用余热蒸干制备AlCl3固体
C. 丙装置里图I烧瓶中充满氨气,烧杯中盛装水,在图II的锥形瓶中,加入足量的Cu与稀硝酸,图I和图II都产生喷泉现象且原理相同
D. 利用丁装置制取SO2,并检验其还原性,小试管中的试剂可为酸性KMnO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)关注营养平衡,合理使用药物,有利于身心健康,现有下列四种物质:
A. 维生素 B. 油脂 C. 青霉素 D. 碘酸钾
请根据题意,选择恰当的选项字母代号填空。
①在人体内提供能量的物质是___________。
②为预防甲状腺肿大,常在食盐中加入的物质是___________。
③能阻止多种细菌生长的重要抗生素是___________。
④存在于蔬菜、水果中,具有还原性的物质是___________。
(2)随着工业发展和社会的进步,人们日益关注环境污染问题。
①垃圾处理遵循无害化、减量化和资源化的原则。垃圾分类收集是实现上述原则的措施之一。贴有如图所示标志的垃圾箱收集的是___________(填字母代号):

A. 可回收物 B.有害垃圾 C.其它垃圾
②我国城市发布的“空气质量日报”中,下列物质不列入首要污染物的是___________(填字母代号):
A. 二氧化硫 B.二氧化碳 C.二氧化氮 D.可吸入颗粒物
③使用Pb2+含量超标的水,会严重危害人体健康,某冶炼厂产生了Pb2+含量超标的废水,处理此废水的方法是加入适量Na2S,使Pb2+沉淀而除去。请写出该反应的离子方程式: ___________。
(3)材料是人类生存和发展的物质基础,合理使用材料可以节约资源。
①下列生活中的常见物质,属于硅酸盐材料的是___________(填字母代号):
A. 汽车轮胎 B. 不锈钢 C. 水泥
②我国航天员穿的航天服主要是由具有密度小、强度大、耐腐蚀、柔软等优良性能的特殊材料制成,这些材料属于___________(填字母代号):
A. 镁铝合金 B. 合成纤维 C. 天然纤维
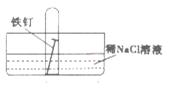
(4)某同学取一颗光亮的铁钉按如图装置做吸氧腐蚀实验。几天后观察到:试管内铁钉生锈、液面上升。此过程中正极的反应式为:O2+4e- +2H2O=4OH- ,则负极的反应式为:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应叙述相符的是
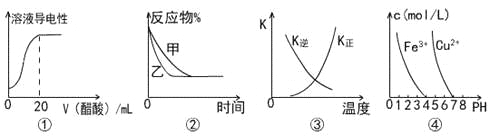
A.图①表示向20 mL 0.1 mol/L氨水中逐滴加入0.1 mol/L醋酸,溶液导电性随加入酸体积的变化
B.图②表示压强对可逆反应A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
C.图③中曲线表示反应3A(g) + B(g)![]() 2C(g)△H<0,正、逆反应的平衡常数K随温度的变化
2C(g)△H<0,正、逆反应的平衡常数K随温度的变化
D.据图④,若要除去CuSO4溶液中的Fe3+,可加入NaOH溶液至pH在4左右
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜别名一氯化铜为白色立方结晶或白色粉末,难溶于水,不溶于乙醇,在潮湿空气中易被迅速氧化。
Ⅰ.实验室用CuSO4-NaCl混合液与Na2SO3溶液反应制取CuCl。相关装置及数据如图。
回答以下问题:
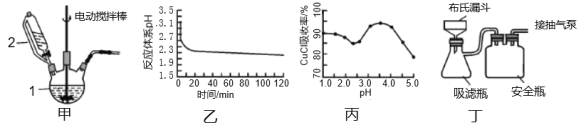
(1)甲图中仪器1的名称是___;制备过程中Na2SO3过量会发生副反应生成[Cu(SO3)2]3-,为提高产率,仪器2中所加试剂为___(填“A”或“B”)
A.CuSO4-NaCl混合液 B.Na2SO3溶液
(2)乙图是体系pH随时间变化关系图,写出制备CuCl的离子方程式___;丙图是产率随pH变化关系图,实验过程中往往用Na2SO3—Na2CO3混合溶液代替Na2SO3溶液,其中Na2CO3的作用是___,并维持pH在___左右以保证较高产率。
(3)反应完成后经抽滤、洗涤、干燥获得产品。抽滤所用装置如丁图所示,其中抽气泵的作用是使吸滤瓶与安全瓶中的压强减小,跟常规过滤相比,采用抽滤的优点是___(写一条);洗涤时,用“去氧水”作洗涤剂洗涤产品,作用是___。
Ⅱ.工业上常用CuCl作O2、CO的吸收剂,某同学利用如图所示装置模拟工业上测定高炉煤气中CO、CO2、N2、和O2的含量。
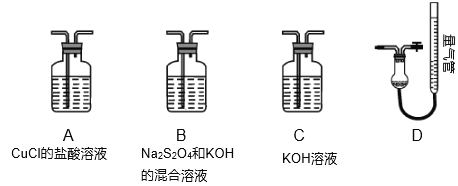
已知:Na2S2O4和KOH的混合液也能吸收氧气。
(4)装置的连接顺序应为___→D。
(5)用D装置测N2含量,读数时应注意___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸在有机合成、医药化工、化纤等行业应用非常广泛。工业上用氨催化氧化法可生产硝酸,其生产过程可表示为:
4NH3+5O2![]() 4NO+6H2O ----①
4NO+6H2O ----①
4NO+3O2+2H2O→4HNO3----②
完成下列计算:
52、如果以一定量的氨气在一密闭容器中与足量氧气发生上述反应,冷却后所得溶液中溶质的质量分数是_________________(保留2位小数,下同)。
53、现以1.70吨液氨为原料生产硝酸,然后加入4.50吨水,得到密度为1.31g/cm3的硝酸,该硝酸的物质的量浓度是_______mol/L(假设生产过程中反应物和生成物均无损耗)。
54、把22.40 g铁完全溶解于某浓度的硝酸中,反应只收集到 0.30 mol NO2 和0.20 mol NO。通过计算推断反应后溶液中溶质的成分及其物质的量__________(写出计算过程)。
55、硝酸工业尾气中的NO、NO2属于大气的主要污染物。已知1m3硝酸工业的尾气中含3160mg NOx,其中n(NO) : n(NO2) = 9:1。
(1)如果用NaOH溶液完全吸收NOx,至少需要补充标准状况下的富氧空气多少升?
_________________________(富氧空气中O2的体积分数为0.25)(写出计算过程)
(2)如果用氨催化还原法,即用氨作催化剂,将NO、NO2转化为氮气直接排入空气中,需要氨气的质量为多少克?__________________________(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com