
【题目】(1)关注营养平衡,合理使用药物,有利于身心健康,现有下列四种物质:
A. 维生素 B. 油脂 C. 青霉素 D. 碘酸钾
请根据题意,选择恰当的选项字母代号填空。
①在人体内提供能量的物质是___________。
②为预防甲状腺肿大,常在食盐中加入的物质是___________。
③能阻止多种细菌生长的重要抗生素是___________。
④存在于蔬菜、水果中,具有还原性的物质是___________。
(2)随着工业发展和社会的进步,人们日益关注环境污染问题。
①垃圾处理遵循无害化、减量化和资源化的原则。垃圾分类收集是实现上述原则的措施之一。贴有如图所示标志的垃圾箱收集的是___________(填字母代号):

A. 可回收物 B.有害垃圾 C.其它垃圾
②我国城市发布的“空气质量日报”中,下列物质不列入首要污染物的是___________(填字母代号):
A. 二氧化硫 B.二氧化碳 C.二氧化氮 D.可吸入颗粒物
③使用Pb2+含量超标的水,会严重危害人体健康,某冶炼厂产生了Pb2+含量超标的废水,处理此废水的方法是加入适量Na2S,使Pb2+沉淀而除去。请写出该反应的离子方程式: ___________。
(3)材料是人类生存和发展的物质基础,合理使用材料可以节约资源。
①下列生活中的常见物质,属于硅酸盐材料的是___________(填字母代号):
A. 汽车轮胎 B. 不锈钢 C. 水泥
②我国航天员穿的航天服主要是由具有密度小、强度大、耐腐蚀、柔软等优良性能的特殊材料制成,这些材料属于___________(填字母代号):
A. 镁铝合金 B. 合成纤维 C. 天然纤维
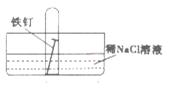
(4)某同学取一颗光亮的铁钉按如图装置做吸氧腐蚀实验。几天后观察到:试管内铁钉生锈、液面上升。此过程中正极的反应式为:O2+4e- +2H2O=4OH- ,则负极的反应式为:_________________________________。
【答案】B D C A A B Pb2++S2-=PbS↓ C B Fe-2e-=Fe2+
【解析】
(1)根据各营养物质在人体内的作用分析解答;(2)根据化学环境保护相关知识分析解答;(3)根据材料的组成和性质分析解答;(4)根据电化学腐蚀原理分析解答。
(1)①人体的六大营养物质是:水、无机盐、蛋白质、脂肪、糖类和维生素,蛋白质、脂肪、糖类是给人体提供能量的物质,所以B符合,故答案为:B;
②碘是合成甲状腺激素的元素,食盐加碘酸钾可以预防甲状腺肿大,D符合,故答案为:D;
③青霉素是最早发现的对许多病原菌有抑制作用,对人和动物组织无毒的抗生素,所以C符合,故答案为:C;
④维生素是生物的生长和代谢所必需的微量有机物,可分为脂溶性维生素和水溶性维生素两类,是维持人体生命活动必须的一类有机物质,也是保持人体健康的重要活性物质,存在于蔬菜、水果中,具有还原性,所以A符合,故答案为:A.
(2)① 表示可回收垃圾,故答案为:A;
表示可回收垃圾,故答案为:A;
②空气质量日报”涉及的污染物有二氧化硫(SO2)、二氧化氮(NO2)、可吸入颗粒物等,二氧化碳为空气组成成分,不属于污染物,故答案为B;
③S2-和Pb2+结合生成PbS沉淀,离子方程式为:Pb2++S2-=PbS↓,故答案为:Pb2++S2-=PbS↓;
(3)①汽车轮胎属于有机合成材料;不锈钢属于金属材料;水泥属于硅酸盐材料;故答案为:C;
②我国航天员穿的航天服主要是由具有密度小、强度大、耐腐蚀、柔软等优良性能的特殊材料制成,这些材料属于合成纤维,故答案为:B;
(4)该腐蚀为吸氧腐蚀,正极得电子,则Fe作负极,失去电子发生氧化反应,电极反应式为:Fe-2e-=Fe2+,故答案为:Fe-2e-=Fe2+。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。
(1)3He是高效核能原料,其原子核内中子数为_____________。
(2)Na的原子结构示意图为______。
(3)MgCl2在工业上应用广泛,可由MgO制备。
①月球上某矿石经处理得到的MgO中含有少量SiO2,用NaOH溶液除去SiO2的化学方程式为______。
②MgO与炭粉和氯气在一定条件下反应可制备MgCl2,尾气中的氯气可用足量冷的NaOH溶液完全吸收,则生成的盐为_________、_________(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积恒定为3L的密闭容器中,进行如下化学反应:CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)上述反应涉及三种元素,其中原子半径最大的元素核外电子排布式为_________,原子核外电子运动状态最多的元素是_______(写元素符号)。
(2)上述反应所涉及的四种物质中非极性分子的沸点顺序是_____,其主要原因是_________。
(3)该反应的化学平衡常数表达式为_______;该反应的正方向是________反应(选填“吸热”、放热)
(4)某温度下,2min内生成10.8g H2O(g),用CO浓度变化表示这段时间内的平均反应速率为____________;若平衡时各物质浓度符合下式:c(CO2)c(H2)=c(CO)c(H2O),试判断此时的温度为_________℃
(5)能判断该反应是否达到化学平衡状态的依据是_______
a.容器中压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是一种具有多种药理学活性的黄烷酮类药物。实验室由芳香化合物A制备G的合成路线如下:
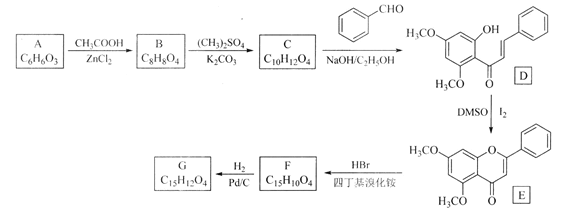
回答以下问题:
(1)A中的官能团名称为________________。E的分子式为________________。
(2)由A生成B和由F生成G的反应类型分别是________________、____________。
(3)由C生成D的化学方程式为____________________。
(4)G的结构简式为____________________。
(5)芳香化合物X是B的同分异构体,可与FeCl3溶液发生显色反应,1molX可与4 mol NaOH反应,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为3:2:2:1。写出一种符合要求的X的结构简式____________。
(6)写出用环戊烯和正丁醛为原料制备化合物![]() 的合成路线(其他试剂任选):__
的合成路线(其他试剂任选):__
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组根据反应:H2O2+2HI=2H2O+I2探究影响化学反应速率的因素。实验数据如下:
实验 编号 | H2O2溶液浓度/(mol·L-1) | HI溶液浓度/(mol·L-1) | 温度/℃ | 反应速率/(mol·L-1·s-1) |
① | 0.1 | 0.1 | 25 | 0.0076 |
② | 0.1 | 0.2 | 25 | 0.0153 |
③ | 0.1 | 0.3 | 25 | 0.0227 |
④ | 0.1 | 0.1 | 35 | 0.0304 |
回答下列问题:
(1)反应:H2O2+2HI=2H2O+I2中,氧化剂是___。
(2)25℃时,表明增大反应物浓度,化学反应速率___(填“增大”或“减小”)。
(3)能表明温度对化学反应速率影响的实验编号是①和___。
(4)H2O2不稳定,写出H2O2发生分解反应的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是( )
A.18g重水(D2O)所含电子的数目为10NA
B.6.4gS2、S4、S6的混合物中所含硫原子的数目为0.2NA
C.标准状况下,2.24LHF中分子的数目为0.1NA
D.60g乙酸与足量乙醇发生酯化反应时断裂C—O键的数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。请根据要求回答问题:
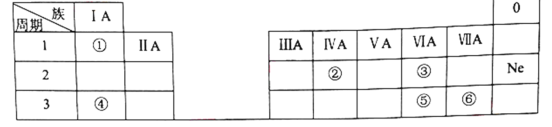
(1)②的元素符号是______。
(2)⑤和⑥两种元素的非金属性强弱关系是:⑤______⑥。
(3)①和③两种元素组成的化合物中含有的化学键为________(填“离子键”或“共价键”)。
(4)④和⑥两种元素组成的化合物与AgNO3溶液反应的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为氢氧燃料电池装置示意图,下列有关说法正确的是( )
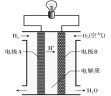
A. 电极A为正极
B. 产物为水,属于环境友好电池
C. 电子流向:电极B→导线→电极A
D. 该电池的化学能可以100%转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲图为一种新型污水处理装置,该装置可利用一种微生物将有机废水的化学能直接转化为电能。乙图是一种家用环保型消毒液发生器,用惰性电极电解饱和食盐水。下列说法中不正确的是 ( )。

A.装置乙的a极要与装置甲的X极连接
B.装置乙中b极的电极反应式为2Cl--2e-=Cl2↑
C.若有机废水中主要含有葡萄糖,则装置甲中M极发生的电极应为C6H12O6+6H2O-24e-=6CO2↑+24H+
D.N电极发生还原反应,当N电极消耗5.6 L(标准状况下)气体时,则有2NA个H+通过离子交换膜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com