
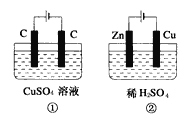
����Ŀ����ͼ��ʾ������ʵ��װ���У���Һ�������Ϊ200mL����ʼʱ�������Һ��Ũ�Ⱦ�Ϊ0.1mol/L������һ��ʱ���õ����Ͼ�ͨ��0.02mol���ӣ�����������Һ����ı仯����������������ȷ���ǣ� ��
A. ����������������1��>��2��
B. ��ҺPH�ı仯����1������2����С
C. �缫���������ʵ���������1��>��2��
D. �缫��Ӧʽ����1����������40H--4e-=2H2O+O2����2���и�����2H++2e-=H2��
���𰸡�C
����������1������ӵ�Դ���ǵ�������2��û����ӵ�Դ����ԭ��أ�п�Ļ����Դ���ͭ�ģ�����п�Ǹ�����ͭ�����������������ͨ��0.02mol���ӣ���A����1����������4OH--4e-=2H2O+O2��������0.005molO2����2��������ӦΪ2H++2e-=H2��������0.01molH2�����������������1������2����A������B����1������OH-������H+����ҺpH��С����2������H+����ҺpH����B����C����1���������൱��CuO����������=0.02mol/2��80g/mol=0.8g����2����������������������=0.02mol/2g/mol��2=0.02g�����ԣ�1������2����C��ȷ��D����2���и�����ӦΪZn-2e-=Zn2+��D��������ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Dz��ֶ�����Ԫ��ԭ�ӣ�����ĸ��ʾ��������������ԭ�������Ĺ�ϵͼ��˵����ȷ���ǣ� ��

A. X��W�γɵĻ�������ֻ�й��ۼ�
B. X��Z�γɵĻ�������ֻ�����Ӽ�
C. Ԫ�صķǽ����ԣ� X��R��W
D. �����ӵİ뾶��W��R��X
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л��������˵����ȷ����
A. (CH3)2C=CH2������Ϊ2-��-1-��ϩ
B. ����Ķ��ȴ�����4��ͬ���칹��
C. �����ӵ�̼̼˫���������������ӳɷ�Ӧ
D. ���������������ԭ����һ��ƽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��̬��A��1 mol����2 mol HCl��ȫ�ӳ�����B��B�ϵ���ԭ�ӱ�Clԭ����ȫȡ����Ҫ8 molCl2����A�����ǣ� ��
A. ��ȲB. 2-��ȲC. 2-��ϩD. 2-����ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʾ�Ϊ�������һ����
A. ���ʯ���ɱ���S02 B. KCI�����ᡢNaOH
C. CuS04��5H20�������Ҵ� D. ������CaC03�����Ͻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ÿ���и����������ʣ����Ƕ����÷�Һ©����������� ��
A�� ����������ˮ���ƾ���ˮ��ֲ���ͺ�ˮ
B�� ���Ȼ�̼��ˮ���屽��ˮ����������ˮ
C�� ���ͺ�ˮ�������ˮ��������Ҵ�
D�� ���ͺ�ˮ�����ͼױ��������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(Te)�㷺���ڲ�ɫ�������մɡ���ҵ���þ���ͭ�������ࣨ��Ҫ����TeO2������Ag��Au)Ϊԭ���Ʊ������ڵ�һ�ֹ����������£�
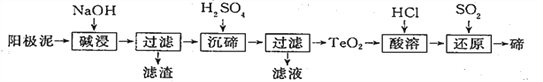
��֪TeO2����ˮ�������ڽ�Ũ��ǿ���ǿ����
(1)�������ʱ������Ӧ�����ӷ���ʽΪ____________________��
(2)�����ġ����������Բ�������ϡ���ᣬ������Ӧ�Ļ�ѧ����ʽ��______________��
(3)�����ڡ�ʱ������Һ��pHΪ4. 55. 0������TeO2���������Բ��ܹ�ǿ����ԭ����_______________����ֹ�ֲ���ȹ���IJ���������_________��
(4)�����ܡ���SO2ͨ��TeCl4������Һ�н��С���ԭ���õ��ڣ��÷�Ӧ�Ļ�ѧ����ʽ��__________��
(5)25��C ʱ�������ᣨH2TeO3) ��Ka1=1��10-3��Ka2=2��10-8��
��0.1 mol��L-1 H2TeO3����Ȧ�ԼΪ_____________������=![]() ��100%)
��100%)
��0. lmol L-1��NaH TeO3��Һ�У��������ӵ����ʵ���Ũ�ȹ�ϵ��ȷ����___________��
A.c(Na+ )>c(HTeO3- )>c(OH-)>c(H2TeO3)>c(H+ )
B.c(Na+) + c( H+) >= c(HTeO3- ) +c(TeO32-) +c(OH- )
C.c(Na+ ) =c(TeO32-) +c( HTeO3-) + c( H2TeO3)
D.c(H+)+c(H2TeO3)=c(OH-)+e(TeO32-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����������A������ʽΪC6H12O2��ʵ�����A������������Һ��������B��C��B�����ᷴӦ�����л���D��C��ͭ���ͼ�������������ΪE������D��E�����ܷ���������Ӧ���ɴ��ж�A�Ŀ��ܽṹ��
A��6�� B��4�� C��3�� D��2��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com