
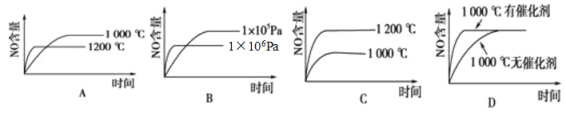
【题目】已知:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),△H=-1025kJ·mol-1。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是
4NO(g)+6H2O(g),△H=-1025kJ·mol-1。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
【题目】下列说法中错误的是
A.根据对角线规则,铍和铝的性质具有相似性
B.在H3O+、NH4+ 和[Cu(NH3)4]2+中都存在配位键
C.元素电负性越大的原子,吸引键合电子的能力越强
D.P4和CH4都是正四面体分子且键角都为109o28ˊ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中的一定量混合气体发生反应aA(g)+bB(g)![]() cC(g);平衡时测得B的浓度为0.6mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得B的浓度降低为0.4mol/L。下列有关判断正确的是
cC(g);平衡时测得B的浓度为0.6mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得B的浓度降低为0.4mol/L。下列有关判断正确的是
A.a+b<c B.平衡向正反应方向移动
C.A的转化率降低 D.C的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对一定温度下的恒容容器中的可逆反应A(g)+3B(g) ![]() 2C(g),下列叙述不能作为平衡标志的是
2C(g),下列叙述不能作为平衡标志的是
①C的生成速率与C的分解速率相等
②单位时间内生成amolA,同时生成3amolB
③A、B、C的浓度不再变化
④A、B、C的压强不再变化
⑤混合气体的总压强不再变化
⑥混合气体的物质的量不再变化
⑦单位时间内消耗amolA,同时生成3amolB
⑧A、B、C的分子数之比为1:3:2
A.②⑧ B.①⑥ C.②④ D.③⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资料得知:Ag+ + 2NH3· H2O ![]() Ag(NH3)2 + 2H2O。下列分析不正确的是
Ag(NH3)2 + 2H2O。下列分析不正确的是
A.浊液中存在沉淀溶解平衡:AgCl (s) ![]() Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)
B.实验可以证明NH3结合Ag+能力比Cl-强
C.实验表明实验室可用氨水洗涤银镜反应后的试管
D.由资料信息可推知:加浓硝酸后生成的沉淀为AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有如下微粒:
①I2 ②Br- ③Na+ ④Fe2+ ⑤H+ ⑥Fe3+
⑦Mg ⑧Cl2 ⑨HCl ⑩H2O S SO2
其中在反应中只能作还原剂的有________,只能作氧化剂的有________,既可作氧化剂又可作还原剂的有________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】被誉为“太空金属”的钛(Ti),在自然界中主要以金红石(TiO2)的形式存在.由于金红石熔点高,为金属Ti的直接制备带来了困难.在工业上常常采用将其先转化成熔沸点较低的TiCl4后再进行还原的方法.金红石转化成TiCl4的反应方程式如下:
TiO2+2C+2Cl2═TiCl4+2CO
(1)指出该反应的氧化剂 ,氧化产物 ;
(2)用双线桥法标出电子转移;
(3)当有6mol电子转移,则有 mol还原剂被氧化.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。
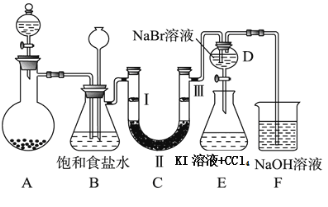
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为: 。装置B中饱和食盐水的作用是 ;
(2)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为 色,打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是 。
(3)装置F中用足量的NaOH溶液吸收余氯,试写出相应的化学方程式: 。
(4)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入 。
a | b | c | d | |
Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 无水氯化钙 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com