
����Ŀ�����ô�������Ӧ��SO2ת��ΪSO3�ǹ�ҵ����������Ĺؼ�������
��1��T1��ʱ����2L�ܱ������г���0.6molSO3��ͼ1��ʾSO3���ʵ�����ʱ��ı仯���ߡ�

��ƽ��ʱ��SO3��ת����Ϊ______������һλС��������T1���·�Ӧ2SO2(g)+O2(g) ![]() 2SO3(g) ��ƽ�ⳣ��Ϊ____________���������������䣬��8minʱѹ�������������1L����n(SO3)�ı仯����Ϊ_______������ĸ����
2SO3(g) ��ƽ�ⳣ��Ϊ____________���������������䣬��8minʱѹ�������������1L����n(SO3)�ı仯����Ϊ_______������ĸ����
���±�Ϊ��ͬ�¶�(T)�·�Ӧ2SO2(g)+O2(g) ![]() 2SO3(g) ��H��0�Ļ�ѧƽ�ⳣ����K����
2SO3(g) ��H��0�Ļ�ѧƽ�ⳣ����K����
T/�� | T2 | T3 |
K | 20.5 | 4.68 |
�ɴ���֪������������ͬ����T1��T2��T3���ֲ�ͬ�¶��£���Ӧ�ӿ�ʼ���ﵽƽ��ʱ����Ҫ��ʱ������� _____________��������T1������T2������T3����
��2������ϵ��ѹ�������½��з�Ӧ��2SO2(g)+O2(g) ![]() 2SO3(g)��ԭ������SO2��O2�����ʵ���֮����k����ͬʱ��SO2��ƽ��ת�������¶���t���Ĺ�ϵ��ͼ2��ʾ��ͼ��k1��k2��k3�Ĵ�С˳��Ϊ____________��
2SO3(g)��ԭ������SO2��O2�����ʵ���֮����k����ͬʱ��SO2��ƽ��ת�������¶���t���Ĺ�ϵ��ͼ2��ʾ��ͼ��k1��k2��k3�Ĵ�С˳��Ϊ____________��

���𰸡� 66.7% 2.5 c T2 k1>k2>k3
��������(1)���ݻ�Ϊ2L�ܱ������г���0.6molSO3����ͼ1ƽ��ʱSO3���ʵ���Ϊ0.2mol��
2SO2(g)+O2(g) 2SO3(g)��
��ʼ��(mol)0 0 0.6
�仯��(mol) 0.4 0.2 0.4
ƽ����(mol) 0.4 0.2 0.2
��SO3��ת����Ϊ=![]() ��100%��66.7%��K=
��100%��66.7%��K=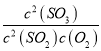 =
=![]() =2.5�������������䣬��8minʱѹ�����������0.5L��ƽ��������Ӧ�����ƶ���n(SO3)���Ϊͼ��c���ʴ�Ϊ��66.7%��2.5�� c��
=2.5�������������䣬��8minʱѹ�����������0.5L��ƽ��������Ӧ�����ƶ���n(SO3)���Ϊͼ��c���ʴ�Ϊ��66.7%��2.5�� c��
����Ϊ��ӦΪ���ȷ�Ӧ���¶�Խ�ͣ�ƽ��Խ������Ӧ�����ƶ���ƽ�ⳣ��Խ�������¶���͵�ΪK���ģ���T2���ʴ�Ϊ��T2��
(2)��ͬ�¶Ⱥ�ѹǿ�£�KԽС������Ũ��Խ��ƽ�������ƶ�������������ת����Խ����k1��k2��k3���ʴ�Ϊ��k1��k2��k3��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������X��Y��Z����Ԫ�أ���֪��
�� X��Y��Z�ĵ����ڳ����¾�Ϊ���塣
�� X�ĵ�����Z�ĵ�����ȼ�գ�����XZ ��ȼ��ʱ����Ϊ��ɫ��
�� XZ��ˮ��Һ��ʹ��ɫʯ����Һ��졣
�� ������X�ĵ�����һ����Y�ĵ��ʻ��ϣ�����������X2Y��X2Y������ΪҺ�塣
�� Z�ĵ�������X2Y�У�������Һ����Ư���ԡ�
�ݴ��ƶϣ�
��1�� X__________��Y____________��Z___________ (дԪ�ط���)��
��2��д���ݵķ�Ӧ����ʽ________________________________________ .
��3��Z�ĵ��ʹ�ҵ�Ʒ��Ļ�ѧ����ʽ��___________________________ .
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������̼����ȼ�ϵ��ԭ��ʾ����ͼ�������йظõ�ص�˵����ȷ������ ��

A. ��ӦCH4+H2O![]() 3H2+CO,ÿ����1molCH4ת��8mol����
3H2+CO,ÿ����1molCH4ת��8mol����
B. �缫A��H2����ĵ缫��ӦΪ��H2+CO32--2e-=H2O+CO2
C. ��ع���ʱ��CO32-��缫B�ƶ�
D. �õ�����ÿͨ��4mol���ӣ��缫B�ϲμӷ�Ӧ��O2Ϊ22.4L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.��1��298Kʱ��0.5 mol C2H4 (g)��ȫȼ�����ɶ�����̼��Һ̬ˮ���ų�705.5kJ����������д���÷�Ӧ���Ȼ�ѧ����ʽ______________________��
��2��Na2SO3���л�ԭ������ˮ��Һ��������Cl2(g)�����ٻ�����Ⱦ��
��֪��Ӧ�� Na2SO3(aq)+Cl2(g)+H2O(l)��Na2SO4(aq)+2HCl(aq) ��H1=a kJ��mol1
Cl2(g)+H2O(l)��HCl(aq)+HClO(aq) ��H2=b kJ��mol1
��д��Na2SO3(aq)��HClO(aq)��Ӧ���Ȼ�ѧ����ʽ��________________________��
��.�췯�ƣ�Na2Cr2O7��2H2O������Ҫ�Ļ���ԭ�ϣ���ҵ���ø�������Ҫ�ɷ���FeO��Cr2O3���Ʊ��췯�ƵĹ����лᷢ�����·�Ӧ��4FeO(s)��4Cr2O3(s)��8Na2CO3(s)��7O2(g) ![]() 8Na2CrO4(s)��2Fe2O3(s)��8CO2(g)����H<0
8Na2CrO4(s)��2Fe2O3(s)��8CO2(g)����H<0

��1����д��������Ӧ�Ļ�ѧƽ�ⳣ������ʽ��K��_____________________��
��2����ͼ1��ʾ����0~2min��CO2��ƽ����Ӧ����Ϊ____________________��
��3��ͼ1��ͼ2��ʾ������Ӧ��2minʱ�ﵽƽ�⡢��4minʱ��ı�ij�������������仯�����ߡ���ͼ1�жϣ���Ӧ������4minʱ�����߷����仯��ԭ����______________�������ֱ���������ͼ2�жϣ�4min��6min�����߱仯��ԭ�������________����д�������
a.�����¶� b���Ӵ��� c��ͨ��O2 d����С�������
��4����ҵ�Ͽ���������Ӧ�еĸ�����CO2�������״���CO2(g)��3H2(g) ![]() CH3OH(g)��H2O(g)��
CH3OH(g)��H2O(g)��
��֪�÷�Ӧ���Է����У�������ͼ����ȷ����____________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʾ�Ϊ�������ʻ����ǵ���Һ������ AΪ����ɫ���壬 C��X ��Ϊ��ɫ���壬ZΪdz��ɫ��Һ��DΪһ�ֳ�����ǿ���������֮���ת����ϵ(��ͼ)���ش��������⣺ (���ַ�Ӧ���������ʡ��)

��1��д���������ʵĻ�ѧʽ�� A______B________ D________
��2��A �� SO3(g)�ķ�Ӧ������ A �� X �ķ�Ӧ����д�� A �� SO3(g)��Ӧ�Ļ�ѧ����ʽ������÷�Ӧ����ת�Ƶķ������Ŀ��___________________��
��3����Z ��Һ��ͨ��������Cl2��д������Z �������������Լ�___________��
��4���� 10g D ����Һ��ͨ��һ������ X����ȫ��Ӧ���ڵ��������������ᾧ�����յõ� 14.8g ���塣
�����������ᾧ�ڵ��������½��е����ɣ�______________���ñ�Ҫ�����ֻش�
�����ù����к��е����ʼ������ǵ����ʵ���֮��Ϊ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�ص��������ʣ���ԭ�������ĵ������������Ա仯����( )
A.���ԭ������
B.���ϼ�
C.ԭ�Ӱ뾶
D.Ԫ�صĻ�ѧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(Te)�㷺���ڲ�ɫ�������մɡ���ҵ���þ����ֵ�������(��Ҫ����TeO2������Ag�� Au)Ϊԭ���Ʊ������ڵ�һ�ֹ����������£�

��֪Te02����ˮ�������ڽ�Ũ��ǿ���ǿ�
(1)�������ʱ���õ��Լ��� ___���ѧʽ����
(2)�����ġ�������������____��
(3)�����ڡ�ʱ����������H2SO4�������Ͻ��衣Ϊ����TeO2�����������Һ��pHΪ4.5��5��0����ԭ����____��
(4)�����ܡ���SO2ͨ��TeC14������Һ�н��С���ԭ���õ��ڣ��÷�Ӧ�Ļ�ѧ����ʽ��____��
(5) 25��ʱ��������(H2Te03)��Kal=lxl0-3��Ka2=2��l0-8
��0.lmol/L��NaHTe03����Һ��c(TeO32-) - c(H2TeO3)= ____��������Ũ�ȱ���ʽ����
��0.lmol��L-1��NaHTe03��Һ��__________����ԡ��������ԡ��������ԡ���������____��д������ƽ�ⳣ��֭�㼰��������).
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ӹ���ķ�����Һ�к���2%��5%��NaNO2������һ�ֻ�����Ⱦ�������NH4Cl��Һ�������˷�����Һ��ʹ��������ת��Ϊ�����ʡ��÷�Ӧ���������У�
��һ����NaNO2+NH4Cl��NaCl+NH4NO2
�ڶ�����NH4NO2![]() N2��+2H2O
N2��+2H2O
���жԵڶ�����Ӧ����������ȷ����
��NH4NO2����������
��NH4NO2���ǻ�ԭ��
��NH4NO2�����˷ֽⷴӦ
��ֻ�е�Ԫ�صĻ��ϼ۷����˱仯
��NH4NO2�������������ǻ�ԭ��
A. �٢� B. �٢�
C. �ڢۢ� D. �ۢܢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com