
【题目】1,4-环己二酮是一种重要的医药、液晶中间体。以工业原料乙烯为基础的1,4-环已二酮(G)合成线路如图所示:
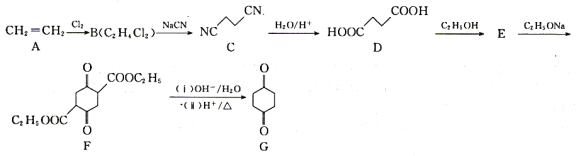
已知:2RCH2COOC2H5![]() +C2H5OH
+C2H5OH
(1)B和E的结构简式分别为________、________。
(2)B→C的反应类型为________。
(3)碳原子上连有4个不同的原子或基团时,该碳称为手性碳,用星号(*)标出F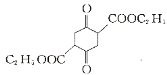 中的手性碳________。
中的手性碳________。
(4)由E→F的化学方程式为________。
(5)同时满足下列条件的G的同分异构体的结构简式________(不考虑立体异构)。
①能发生银镜反应;
②核磁共振氢谱显示为2个峰,且峰面积之比为3:1。
(6)设计由乙烯(CH2=CH2)和乙醇(C2H5OH)制备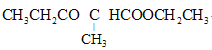 的合成路线________(无机试剂任选)
的合成路线________(无机试剂任选)
【答案】ClCH2CH2Cl C2H5OOCCH2CH2COOC2H5 取代反应 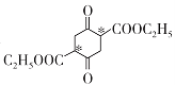 2
2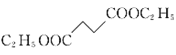
![]()
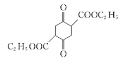 +2C2H5OH
+2C2H5OH ![]() 、
、
![]()
![]()
![]()

【解析】
乙烯与氯气发生加成反应,生成1,2-二氯乙烷;1,2-二氯乙烷与氰化钠发生取代反应,生成![]() ;
;![]() 与水在酸性条件下,生成
与水在酸性条件下,生成![]() ;D与乙醇发生酯化反应生成C2H5OOCCH2CH2COOC2H5;C2H5OOCCH2CH2COOC2H5与乙醇钠反应生成
;D与乙醇发生酯化反应生成C2H5OOCCH2CH2COOC2H5;C2H5OOCCH2CH2COOC2H5与乙醇钠反应生成![]() 。
。
(1)根据乙烯和B的分子式,可推出乙烯到B发成了加成反应,可推知B的结构为ClCH2CH2Cl;根据D的结构简式和D→E的反应,分析D→E属于酯化反应,E的结构为C2H5OOCCH2CH2COOC2H5。
(2)B为ClCH2CH2Cl,C为![]() ,B→C的另一个反应物为NaCN,分析可发现,ClCH2CH2Cl中氯原子被氰基取代了,因此反应类型为取代反应。
,B→C的另一个反应物为NaCN,分析可发现,ClCH2CH2Cl中氯原子被氰基取代了,因此反应类型为取代反应。
(3)F的结构为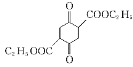 ,根据题目手性碳的定义可判断出,含双键的碳一定不是手性碳,CH2的C也不是手性碳,可判断出手性碳如答案图所示:
,根据题目手性碳的定义可判断出,含双键的碳一定不是手性碳,CH2的C也不是手性碳,可判断出手性碳如答案图所示: ;
;
(4)根据E→F的条件和E的结构式,可推出该反应发生了已知中所提供信息反应:2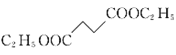
![]()
 +2C2H5OH;
+2C2H5OH;
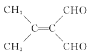
(5)G为![]() ,不饱和度为3,条件限定了能发生银镜反应,说明有机物含有醛基;核磁共振氢谱显示为2个峰,且峰面积之比为3:1,说明有机物呈现高度对称结构,含有2个对称的甲基和2个对称的醛基,还有一个不饱和度,应为中间的碳碳双键,同分异构为:
,不饱和度为3,条件限定了能发生银镜反应,说明有机物含有醛基;核磁共振氢谱显示为2个峰,且峰面积之比为3:1,说明有机物呈现高度对称结构,含有2个对称的甲基和2个对称的醛基,还有一个不饱和度,应为中间的碳碳双键,同分异构为:![]() 、
、![]() 。
。
(6)设计合成路线,根据题目合成路线,目标产物与G相似,需利用已知的酯缩合反应,可利用逆推法分析得到上一步产物为CH3CH2COOCH2CH3,属于酯类物质,由丙酸和乙醇酯化得到,进一步可逆推丙酸上一步为丙腈(CH3CH2CN),最后逆推至所给原料乙烯,具体流程如下:![]()
![]()
![]()
 。
。


科目:高中化学 来源: 题型:
【题目】现以CO、O2、熔融盐Z(Na2CO3)组成的燃料电池,采用电解法处理CO同时制备N2O5,
装置如图所示,其中Y为CO2。下列说法合理的是( )
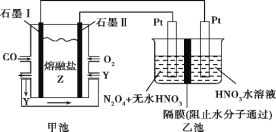
A.石墨Ⅰ是原电池的正极,发生氧化反应
B.甲池中的CO32-向石墨Ⅱ极移动
C.乙池中左端Pt极电极反应式:N2O4-2e-+2HNO3=2N2O5+2H+
D.若甲池消耗标准状况下的氧气2.24L,则乙池中一定能产生氢气0.02mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组使用甲烷燃料电池(如图甲所示)作为SO2传感器(如图乙所示)的电源,检测空气中SO2的含量。下列说法错误的是( )
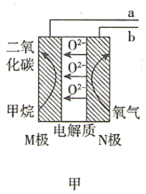
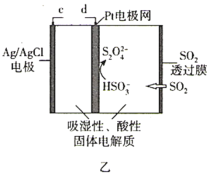
A.甲烷燃料电池M极的电极反应式为CH4-8e-+4O2-=CO2+2H2O
B.甲烷燃料电池的b端连接SO2传感器的c端
C.标准状况下,当甲烷燃料电池的N极消耗2.24L的O2时进入传感器的SO2为4.48L
D.每转移1mol电子,传感器中Ag/AgCl电极质量增加35.5g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三位同学各设计了一个实验,结果各自都认为自己的试样中含有SO42-离子。
甲的实验为:
![]()
(1)乙认为甲的实验不严谨,因为试样A中若含有________离子(仅填一种)也会有此现象。
乙的实验为:
![]()
(2)丙认为乙的实验也不严谨,因为试样B中若含有________离子(仅填一种)也会有此现象。
丙的实验为:
![]()
若丙方案合理,回答:
(3)若丙实验合理,则其中试剂Ⅰ是___________,现象Ⅰ是__________;试剂Ⅱ是___________,现象Ⅱ是__________。(若你认为丙方案不合理,以上四空可以不填)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟磷灰石是常见的钙氟磷酸盐矿物,其化学式为Ca5(PO4)3F,由氟磷灰石制取黄磷(P4)的化学式为4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)=3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g),请回答下列问题:
(1)基态Ca原子电子所占据最高能级的电子云轮廓图为________,基态P原子的价电子轨道表达式为________。
(2)由氟磷灰石制取黄磷(P4)产物中属于极性分子的化合物是________,与其互为等电子体的分子为________。
(3)黄磷(P4)晶体的空间结构如图甲所示,P的杂化轨道类型为________,磷的一种硫化物P4S3的空间结构如图乙所示,每个S原子中含有孤电子对的数目为________。


(4)SiO2的沸点________(填“大于”或“小于”)CO2的沸点,其原因为________。
(5)Ca与Ti、O元素形成的化合物的晶胞结构如图所示,则该晶体的化学式为________,若晶胞密度为ρgcm-3,阿伏加德罗常数的值为NA,则该晶胞中两个距离最近的O原子之间的距离为________pm(用含ρ、NA的表达式表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各2 mol充入某10 L恒容密闭容器中,发生反应X(g)+Y(g) ![]() 2Z(g) △H<0,—段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) △H<0,—段时间后达到平衡。反应过程中测定的数据如下表:
t/min | 2 | 4 | 10 | 12 |
n(Y)/mol | 1.40 | 1.10 | 0.40 | 0.40 |
下列说法正确的是
A. 反应前2 min 的平均速率v(Z)=3.0xl0-2 mol L-1min-1
B. 该温度下此反应的平衡常数K=64
C. 平衡后其他条件不变,再充入2 mol Z,新平衡时X的体积分数增大
D. 反应进行到10 min时保持其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无色的混合气体甲中可能含有NO、CO2、NO2、NH3、N2中的几种,将100mL气体甲经过如图所示实验处理,结果得到酸性溶液,而几乎无气体剩余,则气体甲的组成可能为( )
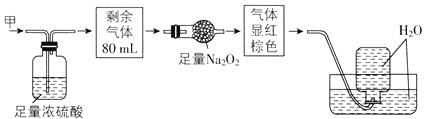
A.NO2、NH3、N2B.NH3、NO、CO2
C.NH3、NO2、CO2D.NO、CO2、N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A. 聚乙烯、植物油都是混合物,都能使溴的四氯化碳溶液褪色
B. 向氯乙烷中加入硝酸银溶液,可以鉴定其中的氯原子
C. 将等体积的苯、汽油和水在试管中充分振荡后静置,现象如图所示:
![]()
D. 可用灼烧的方法鉴别蛋白质和纤维素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含有淀粉的 KIO3 酸性溶液滴加 NaHSO3 溶液,溶液先变蓝后褪色。下列说法错误的是
A.溶液先变蓝的原因:2IO![]() +5HSO
+5HSO![]() =I2+5SO
=I2+5SO![]() +H2O+3H+
+H2O+3H+
B.溶液恰好褪色时 n(KIO3):n(NaHSO3)=1:3
C.还原性 I-> HSO![]() >I2
>I2
D.若向含有淀粉的 NaHSO3 溶液中滴加过量 KIO3 酸性溶液,则溶液变蓝不褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com