
【题目】甲、乙、丙三位同学各设计了一个实验,结果各自都认为自己的试样中含有SO42-离子。
甲的实验为:
![]()
(1)乙认为甲的实验不严谨,因为试样A中若含有________离子(仅填一种)也会有此现象。
乙的实验为:
![]()
(2)丙认为乙的实验也不严谨,因为试样B中若含有________离子(仅填一种)也会有此现象。
丙的实验为:
![]()
若丙方案合理,回答:
(3)若丙实验合理,则其中试剂Ⅰ是___________,现象Ⅰ是__________;试剂Ⅱ是___________,现象Ⅱ是__________。(若你认为丙方案不合理,以上四空可以不填)
科目:高中化学 来源: 题型:
【题目】α-氰基丙烯酸异丁酯可用作医用胶,其结构简式如下。下列关于α-氰基丙烯酸异丁酯的说法错误的是
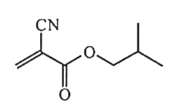
A.其分子式为 C8H11NO2
B.分子中的碳原子有3种杂化方式
C.分子中可能共平面的碳原子最多为6个
D.其任一含苯环的同分异构体中至少有4种不同化学环境的氢原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在足量浓硝酸中加入3.84gCu片,反应完全后,将产生的气体(只含有一种气体)通入800mLH2O中充分反应,设反应前后溶液体积不变。
(1)写出产生的气体通入水中的化学反应方程式,并指出氧化剂与还原剂质量之比___;
(2)试求将气体通入水中充分反应后得到的溶液的物质的量浓度___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外小组用图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
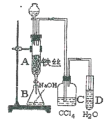
(1)写出A中反应的化学方程式_______________。
(2)观察到A中的现象是_____________________。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是________,写出有关的化学方程式______________________________。
(4)C中盛放CCl4的作用是________________。
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入_______,现象是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质间纷繁复杂的转化关系是化学的魅力所在,下列选项中物质的转化在一定条件下不能一步实现的是( )
A.Si![]() SiO2
SiO2![]() SiB.NO2
SiB.NO2![]() HNO3
HNO3![]() NO2
NO2
C.Fe![]() FeCl3
FeCl3![]() FeD.S
FeD.S![]() SO2
SO2![]() S
S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,4-环己二酮是一种重要的医药、液晶中间体。以工业原料乙烯为基础的1,4-环已二酮(G)合成线路如图所示:
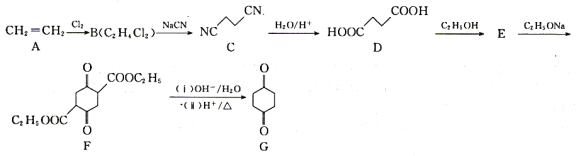
已知:2RCH2COOC2H5![]() +C2H5OH
+C2H5OH
(1)B和E的结构简式分别为________、________。
(2)B→C的反应类型为________。
(3)碳原子上连有4个不同的原子或基团时,该碳称为手性碳,用星号(*)标出F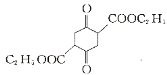 中的手性碳________。
中的手性碳________。
(4)由E→F的化学方程式为________。
(5)同时满足下列条件的G的同分异构体的结构简式________(不考虑立体异构)。
①能发生银镜反应;
②核磁共振氢谱显示为2个峰,且峰面积之比为3:1。
(6)设计由乙烯(CH2=CH2)和乙醇(C2H5OH)制备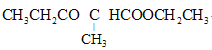 的合成路线________(无机试剂任选)
的合成路线________(无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g)反应过程的能量变化如图所示。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。请回答下列问题:
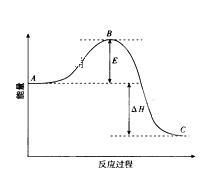
(1)该反应通常用V2O5作催化剂加快反应的进行,加V2O5会使图中B点______(填“升高”或“降低”)。
(2)E的大小对该反应的反应热有无影响_______。
(3)图中A表示SO2(g)和O2(g)的_________。
(4)图中△H的意义是__________。
(5)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物,四价钒化合物再被氧气氧化。写出该催化过程实际发生反应的化学方程式_____,_____;
(6)如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某探究性学习小组欲用酸碱中和滴定法测定市售白醋的总酸量(g·100mL-1)。有关操作如下:
Ⅰ.实验步骤
(1)用________(填仪器名称)量取10.00mL食用白醋,在烧杯中用水稀释后转移到100mL容量瓶中定容,摇匀即得待测白醋溶液。
(2)用酸式滴定管取待测白醋溶液20.00mL于锥形瓶中,向其中滴加2滴________作指示剂。
(3)读取盛装0.1000mol·L-1NaOH溶液的碱式滴定管的初始读数。如果液面位置如图所示,则此时的读数为________mL。
![]()
(4)滴定。当__________________________________________________时,停止滴定,并记录NaOH溶液的终读数。重复滴定3次。
Ⅱ.实验记录
滴定次数实验数据(mL) | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理与讨论
(1)处理数据可得:c(市售白醋)=________mol·L-1;市售白醋总酸量=________g·100mL-1。
(2)在本实验的滴定过程中,下列操作会使实验结果偏大的是________填写序号)。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com