
【题目】大苏打(Na2S2O3·5H2O)、苏打、小苏打被称为“苏氏三兄弟”,它们在生活、生产中有广泛应用。
(1)工业上制备苏打是先制备小苏打,写出我国伟大化学家侯德榜提出的制备小苏打的化学方程式___,操作时,往饱和食盐水中先通入气体,先制备小苏打的原因是___。
(2)Na2S2O3标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高,用离子方程式表示其原因__。
(3)工业上,常用纯碱和盐酸除去锅炉中硫酸钙。先用饱和纯碱溶液浸泡锅垢,然后用盐酸清洗。“浸泡”的目的是__。
(4)工业上,将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2。写出该反应的化学方程式__。Na2S溶液在空气中久置,会生成浅黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的化学式为__。
(5)在密闭容器中投入一定量的Na2O2和NaHCO3,在300℃下充分反应。若残留固体为纯净物,则起始时![]() 满足的条件是__。
满足的条件是__。
【答案】NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl NaHCO3溶解度比Na2CO3小,易分离出来 S2O32-+2H+=S↓+SO2↑+H2O 将CaSO4转化成CaCO3 Na2CO3+2Na2S+4SO2=3Na2S2O3+CO2 Na2S2 ≥2
【解析】
(1)NaHCO3溶解度比Na2CO3小,易分离出来;
(2)酸性环境下S2O32-发生歧化反应,消耗的硫代硫酸根钠偏多,测定结果会偏高;
(3)将硫酸钙转化为易除的碳酸钙;
(4)依据题干可知Na2CO3和Na2S以1:2的物质的量之比混合,再通入二氧化硫发生反应生成Na2S2O3和二氧化碳,依据原子个数守恒、得失电子守恒书写方程式;依据过氧化钠结构结合氧原子、硫原子结构解答;
(5)Na2O2与足量的NaHCO3混合后,在密闭容器中充分加热,可能发生的反应有:2NaHCO3![]() Na2CO3+CO2↑+H2O,2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,CO2+2NaOH=Na2CO3+H2O,残留固体为纯净物,则为碳酸钠,由此分析解答。
Na2CO3+CO2↑+H2O,2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,CO2+2NaOH=Na2CO3+H2O,残留固体为纯净物,则为碳酸钠,由此分析解答。
(1)NaHCO3溶解度比Na2CO3小,易分离出来,往饱和食盐水中先通入气体,制备小苏打的化学方程式为NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl;
(2)酸性环境下S2O32-发生歧化反应,离子方程式:S2O32-+2H+=S↓+H2O+SO2↑;
(3)先用饱和纯碱溶液浸泡锅垢,然后用盐酸清洗。“浸泡”的目的是将硫酸钙转化为易除的碳酸钙,发生的离子反应方程式为:CaSO4+CO32-=CaCO3+SO42-;
(4)依据题干可知Na2CO3和Na2S以1:2的物质的量之比混合,再通入二氧化硫发生反应生成Na2S2O3和二氧化碳,反应中S元素的化合价从-2价升高到+2价,S的化合价从+4价降低到+2价,依据原子个数守恒、得失电子守恒反应的方程式:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2;Na2S溶液在空气中长期放置,和氧气反应生成与过氧化钠的结构及化学性质相似的物质Na2S2;
(5)Na2O2与足量的NaHCO3混合后,在密闭容器中充分加热,可能发生的反应有:2NaHCO3![]() Na2CO3+CO2↑+H2O,2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,CO2+2NaOH=Na2CO3+H2O,残留固体为纯净物,则为碳酸钠,则n(NaHCO3):n(Na2O2)≥2。
Na2CO3+CO2↑+H2O,2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,CO2+2NaOH=Na2CO3+H2O,残留固体为纯净物,则为碳酸钠,则n(NaHCO3):n(Na2O2)≥2。


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
【题目】黑索金是一种爆炸力极强的烈性炸药,比TNT猛烈1.5倍。可用浓硝酸硝解乌洛托品得到黑索金,同时生成硝酸铵和甲醛(HCHO)。下列说法不正确的是( )
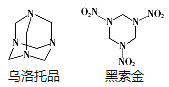
A.乌洛托品的分子式为C6H12N4
B.乌洛托品分子结构中含有3个六元环
C.乌洛托品的一氯代物只有一种
D.乌洛托品得到黑索金反应中乌洛托品与硝酸的物质的量之比为1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在某200mL的稀硫酸和稀硝酸的混合溶液中逐量地加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。(设硝酸只被还原为NO气体,Fe的相对原子质量为56)。下列有关分析错误的是
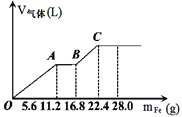
A.原混合酸中NO3-的物质的量为0.2mol
B.原混合酸中H2SO4物质的量浓度为2mol/L
C.OA段与BC段反应中电子转移的物质的量之比为2:1
D.取20mL原混合酸加水稀释至1L后溶液的pH=1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.含0.1molFeI2的溶液中通入0.125molCl2:2Fe2++8I-+5Cl2=2Fe3++4I2+10Cl-
B.浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+![]() Fe3++3NO2↑+3H2O
Fe3++3NO2↑+3H2O
C.Cu溶于稀HNO3:Cu+2H++NO3-=Cu2++NO2↑+H2O
D.氢氧化铁中加入过量氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含MgCl2、AlCl3均为nmol的混合液,向其中滴加NaOH溶液至过量。有关离子沉淀或沉淀溶解与pH的关系如下表。加入NaOH的物质的量与生成沉淀的物质的量的关系正确的是( )
离子 | Mg2+ | Al3+ | 物质 | Al(OH)3 |
开始沉淀pH | 8.93 | 3.56 | 开始溶解pH | 8.04 |
完全沉淀pH | 10.92 | 4.89 | 完全溶解pH | 12.04 |
A. B.
B.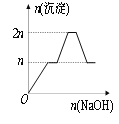
C.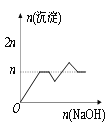 D.
D.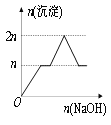
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g))![]() 2SO3(g)反应过程的能量变化如图所示,已知1molSO2(g)被氧化为1molSO3(g)的ΔH=-akJ/mol(a﹥0)。回答下列问题:
2SO3(g)反应过程的能量变化如图所示,已知1molSO2(g)被氧化为1molSO3(g)的ΔH=-akJ/mol(a﹥0)。回答下列问题:
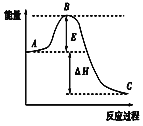
(1)图中A表示:__,E的大小对该反应的反应热ΔH__(填“是”或“否”)有影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点__(填“升高”或“降低”),理由是__。
(2)图中ΔH=__kJ/mol。
(3)在一定温度下,将2molSO2和1molO2放在一密闭容器中,在催化剂作用下充分反应。测得反应放出的热量__(填“等于”、“大于”或“小于”)2akJ。
(4)V2O5的催化循环机理可能为:V2O5氧化SO2时,自己被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:
①__;②4VO2+O2=2V2O5
(5)已知固态单质硫的燃烧热为bkJ/mol,计算由S(s)生成3molSO3(g)的ΔH=___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示。

根据以上条件,回答下列问题:
(1)A与B反应生成C的化学方程式为__;低温下_(填“是”或“否”)有利于该反应自发进行。
(2)一定条件下,在密闭容器中进行上述反应,已知A、B、C的起始浓度分别为0.1mol/L、0.4mol/L、0.2mol/L,当反应达到平衡时,B的浓度范围是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
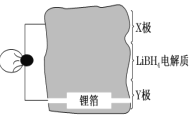
【题目】(1)全固态锂离子电池的结构如图所示,放电时电池反应为 2Li+MgH2=Mg+2LiH。放电时,X 极作_________极。充电时,Y 极反应式为___________。
(2)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子,A-表示乳酸根离子)。
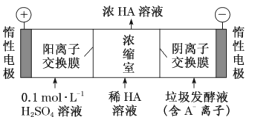
①阳极的电极反应式为 ________________
②简述浓缩室中得到浓乳酸的原理:________________
③电解过程中,采取一定的措施可控制阳极室的 pH 约为 6~8,此时进入浓缩室的OH-可忽略不计。400 mL 10 gL 1 乳酸溶液通电一段时间后,浓度上升为 145 gL 1 (溶液体积变化忽略不计),阴极上产生的 H2 在标准状况下的体积约为_____________L。(乳酸的摩尔质量为90 gmol-1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业中很多重要的原料都是来源于石油化工,回答下列问题
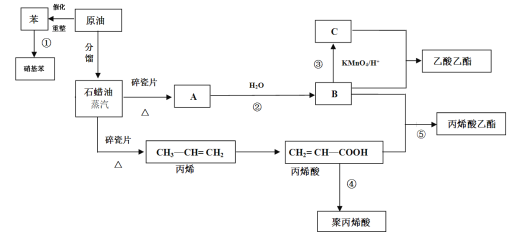
(1)C的结构简式为________。
(2)③④反应的反应类型分别为_____________、___________。
(3)丙烯酸(CH2 = CH — COOH)可能发生的反应有____________(填序号)
A 加成反应 B 取代反应 C 加聚反应 D 中和反应 E 氧化反应
(4)写出下列反应方程式
①反应①的化学方程式__________________________________________________;
②反应②的化学方程式__________________________________________________;
③反应⑤的化学方程式__________________________________________________。
(5)丙烯分子中最多有______个原子共面。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com