
����Ŀ���Ȼ���ͭ(CuCl)�㷺Ӧ���ڻ�����ӡȾ����ҵ������ͭ����Ϊԭ������CuCl�Ĺ�����ͼ��
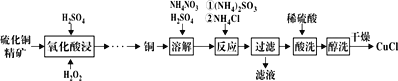
��֪CuCl�����ڴ���ˮ������c(Cl-)�ϴ����ϵ[CuCl(s)+Cl-![]() CuCl2-]����ʪ��������ˮ��������
CuCl2-]����ʪ��������ˮ��������
��1�������������ǰ�Ƚ�ͭ������Ŀ����__���ù���������ɫ��Һ��dz��ɫ��������Ӧ�Ļ�ѧ��Ӧ����ʽΪ__��
��2�����ܽ���ʱ��������Ũ��Ϊ0.3mol��L-1������1L��������Һ����Ҫ98%��1.84g��mL-1Ũ����__mL������1λС�������ܽ�ʱ��Ӧ�����ӷ���ʽ__��
��3������Ӧ��ʱ��Cu+�ij�����������NH4Cl������ϵ��ͼ��ʾ��
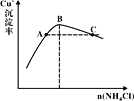
�ٷ�Ӧ������������___��n(������)��n(��ԭ��)=___��
�ڱȽ�c(Cu+)��Դ�С��A��___C�㣨����>������<������=������
����ߴ���C��״̬�Ļ������Cu+�����ʴ�ʩ��___��
��4����������������Һ��������Ҫ�ɷֵĻ�ѧʽΪ__��
��5��������������������������ϴ����������__��
���𰸡�����Ӵ�������ӿ�������ʣ����Cu�Ľ����ʵ� CuS+H2SO4+H2O2=CuSO4+S+2H2O 16.3 3Cu+8H++2NO3-=3Cu2++2NO��+4H2O SO42-��(NH4)2SO4 2��1 > ��ˮϡ�� (NH4)2SO4 HNO3����ǿ�����Ի��CuCl����
��������
����H2O2�����������½�CuS�е�-2��SԪ��������S���ʣ�ͬʱ�ͷ�Cu2+������ϵ�д����õ�Cu���ʣ�Ȼ������NO3-�����������µ�ǿ�����Խ�Cu������Cu2+����������SO32-��Cu2+��ԭ��Cu+��ͬʱ����Cl-��Cu+��������CuCl����ϡ����ϴȥCuCl�����(NH4+)2SO4�����ʣ��������ô�ϴȥ�����������ӣ����������ӷ�����ȥ���õ������CuCl���ݴ˻ش�
��1����������ǰ��һ�㽫���������飬Ŀ���������������Ľ�������һ������Լӿ췴Ӧ���ʣ���һ����ʹ�����е�CuS������ת������߽�ȡ�ʣ����ݳ�������ɫ��Һ��dz��ɫ������֪������Ӧ������CuSO4��S��������CuS+H2SO4+H2O2=CuSO4+S+2H2O���ʴ�Ϊ������Ӵ�������ӿ�������ʣ����Cu�Ľ����ʵȣ�CuS+H2SO4+H2O2=CuSO4+S+2H2O��
��2������c=![]() �ã�Ũ����Ũ��=
�ã�Ũ����Ũ��=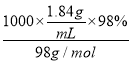 =18.4mol��L-1������C1V1=C2V2�ã�18.4mol��L-1
=18.4mol��L-1������C1V1=C2V2�ã�18.4mol��L-1![]() V=0.3mol��L-1��1L�����V��16.3mL�����ݷ�Ӧ��ΪNH4NO3�����ᣬ��֪������NO3-�����������µ������Խ�Cu�����ܽ⣬�����ķ�ӦΪCu��ϡ���ᷴӦ�������ӷ���ʽΪ��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O���ʴ�Ϊ��16.3��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��
V=0.3mol��L-1��1L�����V��16.3mL�����ݷ�Ӧ��ΪNH4NO3�����ᣬ��֪������NO3-�����������µ������Խ�Cu�����ܽ⣬�����ķ�ӦΪCu��ϡ���ᷴӦ�������ӷ���ʽΪ��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O���ʴ�Ϊ��16.3��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��
��3�������̿�֪������Ӧ������SO32-��Cu2+��ԭ��Cu+��SO32-������Cu2+��������SO42-��SO42-Ϊ�������SO32-������S���ϼ���+4���ߵ�+6��������2��ÿ��Cu2+����ԭ�����ϼ۴�+2���͵�+1��������1������������ԭ��Ӧ�л��ϼ���������=���ϼ۽��������ã�����Cu2+��SO32-�����ʵ���֮��Ϊ2:1��������������ԭ��=2:1���ʴ�Ϊ��SO42-��(NH4)2SO4��2:1��
��B��֮ǰCu+��Cl-�γ�CuCl������B��ʱ������CuCl(s)![]() Cu+(aq)+ Cl-(aq),B��֮��Cl-Ũ��������һ����CuCl�ܽ�[CuCl(s)+Cl-
Cu+(aq)+ Cl-(aq),B��֮��Cl-Ũ��������һ����CuCl�ܽ�[CuCl(s)+Cl-![]() CuCl2-],��CuCl(s)
CuCl2-],��CuCl(s)![]() Cu+(aq)+ Cl-(aq)��֪��CuCl��Ȼ���ܽ���һ���֣�����ƽ�Ⲣû�з����ƶ�������C���B��Cu2+��Ũ������ȵģ�����B��֮ǰCuCl(s)
Cu+(aq)+ Cl-(aq)��֪��CuCl��Ȼ���ܽ���һ���֣�����ƽ�Ⲣû�з����ƶ�������C���B��Cu2+��Ũ������ȵģ�����B��֮ǰCuCl(s)![]() Cu+(aq)+ Cl-(aq)ƽ��һֱ�����ƶ�������B���Cu2+��Ũ��С��A�㣬����������Ϊ��>��
Cu+(aq)+ Cl-(aq)ƽ��һֱ�����ƶ�������B���Cu2+��Ũ��С��A�㣬����������Ϊ��>��
�ۼ�ȻB��֮�������ڷ�����CuCl(s)+Cl-![]() CuCl2-ʹ���������ˣ��������ǿ��Լ�СCl-Ũ�ȣ����������Ƿ��������֮��������ˮϡ�ͣ����Դ�Ϊ����ˮϡ�ͣ�
CuCl2-ʹ���������ˣ��������ǿ��Լ�СCl-Ũ�ȣ����������Ƿ��������֮��������ˮϡ�ͣ����Դ�Ϊ����ˮϡ�ͣ�
��4�����Ͽ�֪����������������Һ��������Ҫ�ɷ�Ϊ(NH4)2SO4�����Դ�Ϊ��(NH4)2SO4��
��5��������ǿ�����ԣ���CuCl���������Բ�����������������������ϴ�����ʴ�Ϊ��HNO3����ǿ�����Ի��CuCl������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��X��Y��Z��W��ԭ��������������P��M��N������������������Ԫ����ɵĻ�������Ǵ���ת����ϵQ![]() P+M+N��P��ʹʪ��ĺ�ɫʯ����ֽ������M�����Ԫ��λ��ͬһ���壬N���³�ѹ��ΪҺ�塣����˵������ȷ���ǣ� ��
P+M+N��P��ʹʪ��ĺ�ɫʯ����ֽ������M�����Ԫ��λ��ͬһ���壬N���³�ѹ��ΪҺ�塣����˵������ȷ���ǣ� ��
A.ԭ�Ӱ뾶��Y��Z��W��X
B.����̬�⻯������ȶ��ԣ�Z��Y
C.����M����Ư����
D.Q������ǿ����Һ��Ӧ��������ǿ����Һ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӵ�����ԭ���γ�sp3�ӻ�����Ҹ����ӵĿռ乹��Ϊ�����ε��ǣ� ��
A.SO42-B.CH3-C.ClO2-D.[PCl4]+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���ᡢ�������������Һ�д�������ƽ�⣺
CH3COOH��H2O | K1��1.75��10��5mol��L��1 |
CH3COO����H2O | K2��5.71��10��10mol��L��1 |
�ֽ� 50 mL 0.2 mol��L��1������ 50 mL 0.2 mol��L��1��������Һ����Ƶ���Һ�ף�����������ȷ����
A.��Һ��pH��7
B.����Һ�����ȣ�K1��K2ͬʱ����
C.������Һ���м��������� NaOH ��Һ����Һ�� pH ��������
D.������Һ���м��� 5 mL 0.1 mol��L��1�����ᣬ����Һ�д���� K1 ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ���ں���Pb2+��Sn2+��ij��Һ�У����������������![]() ����������Ӧ��
����������Ӧ��![]()
![]()
![]() ����ϵ��c��Pb2+����c��Sn2���仯��ϵ����ͼ��ʾ�������ж���ȷ����
����ϵ��c��Pb2+����c��Sn2���仯��ϵ����ͼ��ʾ�������ж���ȷ����
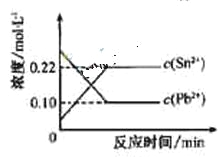
A.��ƽ����ϵ�м�����������Ǧ��c��Pb2+������
B.��ƽ����ϵ�м�������![]() �����c��Sn2-����С
�����c��Sn2-����С
C.�����¶ȣ�ƽ����ϵ��c��Pb2+������˵���÷�Ӧ![]()
D.25��ʱ���÷�Ӧ��ƽ�ⳣ��K=2.2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���ʢ50mL0.100mol��L-1����������ձ��и������ٵμ�50mL������ˮ��0.100mol��L-1�������Һ�������ҺpH��ʱ��仯��ͼ��ʾ����֪Ka(CH3COOH)=1.8��10-5��Kb(NH3��H2O)=1.8��10-5������˵����ȷ���ǣ� ��
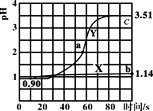
A.����X������μ�����ˮ��pH�仯ͼ���μӹ�������Һ��������Ũ����С
B.����Y�ϵ�����һ����Һ�о�����c(CH3COO-)<c(NH4+)
C.a����Һ��n(Cl-)��n(CH3COO-)��n(OH)-n(NH4+)=0.01mol
D.b����Һ��ˮ�����c(H+)��c���102.37��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����dz����Ĺ��ɽ���֮һ,�о��������ʾ�����Ҫ���塣

��1������ͼװ���У��۲쵽װ�ü�ͭ�缫�ϲ�����������ɫ���壻 ��װ������ͭ�缫����������������缫�ϲ�����������ɫ���塣�ɴ˿ɵõ��Ľ�����__________________��
��2����ҵ��ʹ����ͼװ�ã�����ʯī���缫���Na2CrO4��Һ��ʹNa2CrO4ת��ΪNa2Cr2O7,��ת��ԭ��Ϊ_____________________________________��

��3��CrO3��K2Cr2O7��������ˮ�������ǹ�ҵ��ˮ��ɸ���Ⱦ����Ҫԭ��Ҫ��Cr(��)ת��ΪCr (��) �����Ĵ��������ǵ�ⷨ���������巨��
����ⷨ�� ����Cr2O72- �ķ�ˮͨ������ڣ������������������Ի����У�����������NaCl ���е�⣬ʹ�������ɵ�Fe2+��Cr2O72- ������Ӧ�������ӷ���ʽΪ_______________��������Cr2O72- ��H+��Fe3+�����ܷŵ硣��Cr2O72- �ŵ磬�������ĵ缫��ӦʽΪ_________; ��H+�ŵ磬���������γ�Fe(OH)3��Cr(OH)3��������֪��Cr3+![]() Cr(OH)3
Cr(OH)3![]() CrO2-,����������ҺpH �ķ�ΧΪ_________��
CrO2-,����������ҺpH �ķ�ΧΪ_________��
���������巨�� �ں�Cr (��) �ķ�ˮ�м����̷�����pH<4ʱ������ӦʹCr (��) ת��ΪCr (��),������ҺpH Ϊ6~8,ʹ��Һ�е�Fe (��)��F e(��)��Cr (��)��������൱��Fe(��) [Fe(��)x��Cr (��)2-x] O4(��������) �ij�����������������x=_________�� ����ˮ��Cr (��) ��CrO3��,�ø÷���ȥ��ˮ�е�Cr (��),�����FeSO4��7H2O ��CrO3��������Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����Ȼ�ѧ����ʽ�У���H1>��H2����
��C(s)��O2(g)=CO2(g) ��H1 C(s)��![]() O2(g)=CO(g) ��H2
O2(g)=CO(g) ��H2
��S(s)��O2(g)=SO2(g) ��H1 S(g)��O2(g)=SO2(g) ��H2
��H2(g)��![]() O2(g)=H2O(l) ��H1 2H2(g)��O2(g)=2H2O(l) ��H2
O2(g)=H2O(l) ��H1 2H2(g)��O2(g)=2H2O(l) ��H2
��CaCO3(s)=CaO(s)��CO2(g) ��H1 CaO(s)��H2O(l)=Ca(OH)2(s) ��H2
A.��B.��C.�ڢۢ�D.�٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ּס�������ѧС�鰲װ������ͼ��ʾ����ͬװ�ã�����̽��Ӱ��H2O2�ֽ����ʵ����ء�

��1������a������___��
��2��MnO2����H2O2�ֽ�Ļ�ѧ����ʽ��___��
��3����С��������ʵ����Ʒ����������������ɱ�����δ��֡�
ʵ���� | ʵ��Ŀ�� | T/K | ���� | Ũ�� |
����ʵ��� | ��ʵ����� | 298 | 3��FeCl3��Һ | 10mL2%H2O2 |
����ʵ��� | ��__ | 298 | ��__ | 10mL5%H2O2 |
��4���ס�����С��ó���ͼ���ݡ�
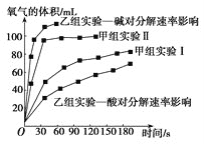
���ɼ���ʵ�����ݿɵó����ֽ���__��
���������о����ᡢ���H2O2�ֽ�Ӱ�����ص�������ͬ�����£�Na2O2��K2O2����ˮ�ų��������ʽϿ����__���������������BaO2������H2SO4��Һ��Ӧ��H2O2���仯ѧ��Ӧ����ʽΪ_��֧����һ������������_��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com