
【题目】丹参醇是一种中药成分,结构简式如图所示。下列关于丹参醇的描述正确的是

A.能与浓硫酸共热后发生消去反应
B.能与NaHCO3溶液反应放出气体
C.分子中含有2个手性碳原子
D.1 mol丹参醇最多能与5 mol H2发生加成反应
科目:高中化学 来源: 题型:
【题目】有一种瓦斯分析仪能够在煤矿巷道中的甲烷达到一定浓度时,通过传感器显示出来。该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动。下列有关叙述正确的是

A.电极a的反应式为:CH4+4O2--8e-=CO2+2H2O
B.电极b是正极,O2-由电极a流向电极b
C.瓦斯分析仪工作时,电池内电路中电子由电极a流向电极b
D.当固体电解质中有1 mol O2-通过时,电子转移4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A.0.1 mol·L-1 CaCl2溶液中:Ag+、Cu2+、SCN-、![]()
B.能使甲基橙变红的溶液中:Na+、Mg2+、![]() 、Cl-
、Cl-
C.![]() =1×10-12 mol·L-1的溶液:K+、Na+、
=1×10-12 mol·L-1的溶液:K+、Na+、![]() 、
、![]()
D.0.1 mol·L-1 FeSO4溶液中:Na+、![]() 、ClO-、
、ClO-、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.将纯水加热后,水的电离程度增大,pH不变
B.反应2H2(g)+O2(g)=2H2O(l)在一定条件能自发进行的原因是ΔS<0
C.常温下,向0.1 mol·L-1 NH4Cl溶液中通入少量HCl,溶液中![]() 增大
增大
D.常温下,向CaCO3悬浊液中加入少量水,所得新悬浊液中c(Ca2+)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,两体积均为1 L的容器中发生反应:CO(g)+2H2(g) ![]() CH3OH(g) ΔH。容器中起始各物质的物质的量如下表所示,两容器中c(H2)随时间t的变化如下图所示。
CH3OH(g) ΔH。容器中起始各物质的物质的量如下表所示,两容器中c(H2)随时间t的变化如下图所示。
容器 | 温度 | CO | H2 | CH3OH |
Ⅰ | T1℃ | a mol | 2 mol | 0 mol |
Ⅱ | T1℃ | 0.5 mol | 1 mol | 0 mol |

下列说法正确的是
A.0~5 min时,容器Ⅰ中v(CO)=0.1 mol·L-1·min-1
B.a>1
C.若容器Ⅱ温度改变为T2(T2>T1)时,平衡常数K=1,则ΔH<0
D.T1℃时,若向容器Ⅰ中充入CO、H2、CH3OH各1 mol,反应将向逆反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D最高价氧化物对应水化物分别为X、Y、Z、W,A是短周期中原子半径最大的元素,常温下X、Z、W均可与Y反应,A、C、D的原子序数及0.1mol/L X、Z、W溶液的pH如图所示(已知lg2=0.3).下列说法正确的是( )
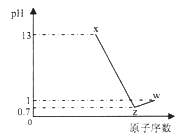
A. A的离子半径小于B的离子半径
B. W、X两物质含有的化学键类型相同
C. D氢化物稳定性小于C氢化物稳定性
D. B的简单离子会影响水的电离平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项叙述中,正确的是
A.价电子排布为ns1的元素,不一定是s区元素
B.配合物Fe(CO)n内中心原子价电子数与配体提供电子总数之和为18,则n=5
C.光卤气(COCl2)、甲醛分子的立体构型和键角均相同
D.某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE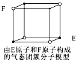
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com