
【题目】下列说法正确的是( )
A.核外电子的排布应优先排布在能量最低的电子层
B.对于主族元素而言,若最外层电子数为m,电子层数为n,则![]() 值越大,金属性越强
值越大,金属性越强
C.同一周期中,随着核电荷数的增加,阴离子半径逐渐增大
D.第三、四周期中,同族元素原子的核电荷数相差一定为8
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】环氧乙烷常用于一次性口罩生产过程中灭菌和新冠病毒的消杀,工业上常利用乙烯直接氧化法生产环氧乙烷(![]() ),发生的反应如下。
),发生的反应如下。
主反应Ⅰ:2CH2=CH2(g)+O2(g)![]() 2
2![]() (g) ΔH1=-210kJ·mol-1
(g) ΔH1=-210kJ·mol-1
副反应Ⅱ:CH2=CH2(g)+3O2(g)![]() 2CO2(g)+2H2O(l) ΔH2=-1324kJ·mol-1
2CO2(g)+2H2O(l) ΔH2=-1324kJ·mol-1
副反应Ⅲ:2![]() (g)+5O2(g)
(g)+5O2(g)![]() 4CO2(g)+4H2O(g) ΔH3
4CO2(g)+4H2O(g) ΔH3
已知:环氧乙烷选择性是指乙烯进行反应Ⅰ生成环氧乙烷的优势。
(1)ΔH3=__kJ·mol-1。
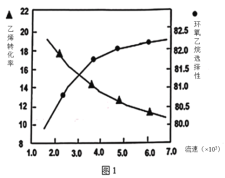
(2)①图1是乙烯转化率、环氧乙烷选择性与流速关系的图象,图中随进料气的流速加快,乙烯的转化率下降,其可能原因是__。
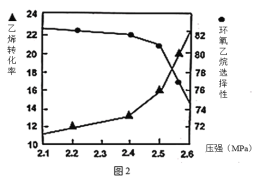
②图2是乙烯转化率、环氧乙烷选择性与压强关系的图象,图中当反应体系的压强高于2.4MPa,环氧乙烷选择性下降,其可能原因是__。
(3)实验测得反应Ⅰ中,υ正=K正·x2(CH2=CH2)·x(O2),υ逆=K逆·x2(![]() ),(式中x为物质的量分数;K正、K逆为速率常数,只与温度有关)。
),(式中x为物质的量分数;K正、K逆为速率常数,只与温度有关)。
①若在1L的密闭容器中充2molCH2=CH2(g)和1molO2(g),在一定温度下只发生反应I,达到平衡时CH2=CH2的转化率为75%,则该反应平衡常数的值为__。
②若平衡后仅升高温度,则下列说法正确的是___。
A.x(CH2=CH2)增大,x(![]() )减小
)减小
B.K正与K逆的比值增大
C.υ正减小,υ逆增大
D.K正与K逆的比值减小
(4)将乙烯与饱和食盐水的电解产物反应,转化为氯乙醇[CH2(OH)CH2Cl],氯乙醇进一步反应生成环氧乙烷,其电解简易装置如图所示。
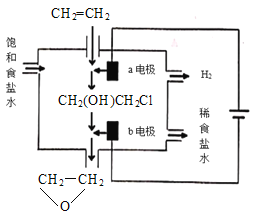
已知:CH2=CH2+H2O+Cl2→CH2(OH)CH2Cl+HCl
①a电极为__(选填“阴极”或“阳极”),其电极反应式为:__。
②b电极区域生成环氧乙烷的化学方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。因此,将氯化氢转化为氯气的技术成为科学研究的热点。请回答:
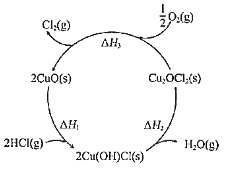
(1)如图表示在CuO存在下HCl催化氧化的反应过程,则总反应的化学方程为______。
(2)研究HCl催化氧化反应中温度、![]() 和
和![]() 等因素对HCl转化率的影响,得到如下实验结果:
等因素对HCl转化率的影响,得到如下实验结果:
①利用Na2S2O3溶液和KI溶液测定反应生成Cl2的物质的量,若消耗V1mLc1mol·L-1的Na2S2O3溶液,则生成Cl2____________mol(已知2S2O![]() +I2=S4O
+I2=S4O![]() +2I-)。
+2I-)。
②![]() 表示催化剂的质量与HCl(g)流速之比,是衡量反应气体与催化剂接触情况的物理量。当
表示催化剂的质量与HCl(g)流速之比,是衡量反应气体与催化剂接触情况的物理量。当![]() =4、
=4、![]() =50g·min·mol-1时,每分钟流经1g催化剂的气体体积为_____L(折算为标准状况下)。
=50g·min·mol-1时,每分钟流经1g催化剂的气体体积为_____L(折算为标准状况下)。
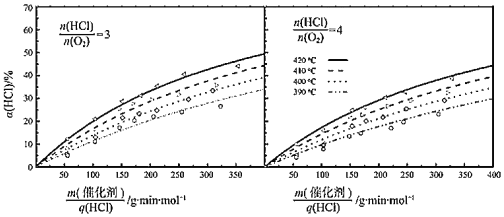
③在420℃、![]() =3、
=3、![]() =200g·min·mol-1条件下,α(HCl)为33.3%,则O2的反应速率为_______mol·g-1·min-1。
=200g·min·mol-1条件下,α(HCl)为33.3%,则O2的反应速率为_______mol·g-1·min-1。
④比较在下列两种反应条件下O2的反应速率:vⅠ_______vⅡ(填“>”“=”或“<”)。
Ⅰ.410℃、![]() =3、
=3、![]() =350g·min·mol-1;
=350g·min·mol-1;
Ⅱ.390℃、![]() =4、
=4、![]() =350g·min·mol-1。
=350g·min·mol-1。
(3)在101.325kPa时,以含N2的HCl和O2的混合气体测定不同温度下HCl催化氧化反应中HCl的平衡转化率,得到如图结果
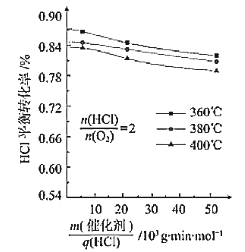
①360℃时反应的平衡常数K360与400℃时反应的平衡常数K400之间的关系是K360_________K400。(填“>”“=”或“<”)。
②一定温度下随着![]() 的增大,HCl的平衡转化率_______(填“增大”“减小”或“不变”),原因为___________________。
的增大,HCl的平衡转化率_______(填“增大”“减小”或“不变”),原因为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:(不考虑溶液混合所引起的体积缩小)
实验 序号 | 实验温度/K | 参加反应的物质 | 溶液颜色褪至无色时所需时间/s | ||||
KMnO4溶液(含硫酸) | H2C2O4溶液 | H2O | |||||
V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | |||
A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | 6 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t1 |
(1)通过实验A、B,可探究出浓度的改变对反应速率的影响,其中V1=_________,T1=_______;通过实验___________可探究出温度变化对化学反应速率的影响。
(2)C组实验中液褪色时间t1______(填“>”或“<”)8s,C组实验的反应速率v(KMnO4) = _________________。(用含有t1的式子表示)
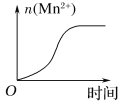
(3)该小组的一位同学通过查阅资料发现,上述实验过程中n(Mn2+)随时间变化的趋势如图所示,并以此分析造成n(Mn2+)突变的可能的原因是:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法,不正确的是( )
A.ClO2具有强氧化性,可用于自来水的杀菌消毒
B.氮肥包括铵态氮肥、硝态氮肥和尿素
C.电解法冶炼铝时,加入冰晶石可降低氧化铝熔融温度,减少能耗
D.生物炼铜,是指在某些细菌作用下,利用空气中的氧气将不溶性铜矿转化为铜单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“三室法”制备烧碱和硫酸示意图如下,下列说法正确的是( )
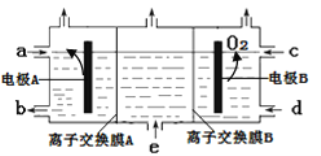
A.电极A为阳极,发生氧化反应
B.离子交换膜A为阴离子交换膜
C.稀硫酸从c处进,浓![]() 溶液从b处出,浓
溶液从b处出,浓![]() 溶液从e处进
溶液从e处进
D.![]() 和
和![]() 迁移的数量和等于导线上通过电子的数量
迁移的数量和等于导线上通过电子的数量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,定容密闭容器中0.4mol/LN2,1mol/LH2进行反应:N2(g)+ 3H2(g)![]() 2NH3(g),10min反应达到平衡,此时测得N2浓度为0.2mol/L。
2NH3(g),10min反应达到平衡,此时测得N2浓度为0.2mol/L。
(1)10min内,用H2浓度变化来表示的反应速率为___,平衡时NH3的物质的量浓度为____;
(2)能判断该反应达到化学平衡状态的依据是____
A.容器中密度不随时间变化而变化 B.容器中各物质的浓度保持不变
C.N2和NH3的消耗速率之比为2∶1 D.N2消耗速率与H2生成速率之比为3:1
(3)平衡时N2和H2的转化率之比为____;该反应的平衡常数表达式为K=____,该温度下反应的平衡常数是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO,制备流程如下图所示
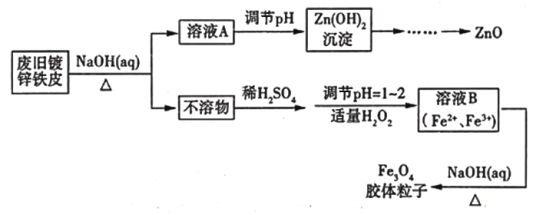
(1)从流程图可知,Zn、Fe中能与NaOH溶液反应的是_______________________。
(2)向不溶物中加入稀硫酸发生反应的离子方程式是____________________________________。
(3)加入适量H2O2的目的是__________________________________。
(4)如何证明已生成了Fe3O4胶体?_____________________________________________________。
(5)流程中所需的硫酸溶液由焦硫酸(H2SO4·SO3)溶于水配制而成,其中的SO3都转化为硫酸,若将445g焦硫酸溶于水配成4.00L硫酸,该硫酸的物质的量浓度为__________________mol/L。
(6)稀硫酸也可以用浓硫酸和水配制。已知4 mol/L的硫酸溶液密度为ρ1g/cm3,2 mol/L的硫酸溶液密度为ρ2g/cm3。100g物质的量浓度为4 mol/L的硫酸溶液与___________mL水混合,使硫酸的物质的量浓度减小到2 mol/L(用含ρ1、ρ2的式子表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品。至今已被多个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义。其主要成分是青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),结构如图所示。有关该化合物的叙述正确的是( )
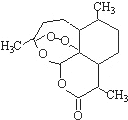
A.分子式为:C16H22O5
B.该化合物在一定条件下不能与NaOH溶液反应
C.该化合物中含有过氧键,一定条件下有氧化性
D.青蒿素与维生素一样是水溶性的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com