
����Ŀ��һ���¶��£������ܱ�������0.4mol/LN2��1mol/LH2���з�Ӧ��N2(g)+ 3H2(g)![]() 2NH3(g)��10min��Ӧ�ﵽƽ�⣬��ʱ���N2Ũ��Ϊ0.2mol/L��
2NH3(g)��10min��Ӧ�ﵽƽ�⣬��ʱ���N2Ũ��Ϊ0.2mol/L��
��1��10min�ڣ���H2Ũ�ȱ仯����ʾ�ķ�Ӧ����Ϊ___��ƽ��ʱNH3�����ʵ���Ũ��Ϊ____��
��2�����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������____
A���������ܶȲ���ʱ��仯���仯 B�������и����ʵ�Ũ�ȱ��ֲ���
C��N2��NH3����������֮��Ϊ2��1 D��N2����������H2��������֮��Ϊ3:1
��3��ƽ��ʱN2��H2��ת����֮��Ϊ____���÷�Ӧ��ƽ�ⳣ������ʽΪK=____�����¶��·�Ӧ��ƽ�ⳣ����___��
���𰸡�0.06mol/( L��min) 0.4mol/L B 5:6 ![]() 12.5(L/mol)2
12.5(L/mol)2
��������
��1����������ʽ��֪��N2(g)+ 3H2(g)![]() 2NH3(g)
2NH3(g)
��ʼʱ��Ũ��(mol/L) 0.4 1 0
�ı��Ũ��(mol/L) 0.2 0.6 0.4
ƽ��ʱ��Ũ��(mol/L) 0.2 0.4 0.4
��10min�ڣ���H2Ũ�ȱ仯����ʾ�ķ�Ӧ����Ϊ![]() =0.06 mol/( L��min)��ƽ��ʱNH3�����ʵ���Ũ��Ϊ0.4mol/L��
=0.06 mol/( L��min)��ƽ��ʱNH3�����ʵ���Ũ��Ϊ0.4mol/L��
��2��A�������Ǻ���������������������������䣬���������ܶȱ��ֲ��䣬�������ܶȲ���ʱ��仯���仯������Ϊ�жϸ÷�Ӧ��ƽ������ݣ�ѡ��A����
B�������и����ʵ�Ũ�ȱ��ֲ��䣬��Ӧ�ﵽƽ��״̬��ѡ��B��ȷ��
C��N2��NH3����������֮��Ϊ2��1��ӦΪ1��2������˵�����淴Ӧ���ʲ���ȣ���Ӧû�дﵽƽ��״̬��ѡ��C����
D��N2����������H2��������֮��Ϊ3:1��ӦΪ1��3������˵�����淴Ӧ���ʲ���ȣ���Ӧû�дﵽƽ��״̬��ѡ��D����
��ѡB��
��3�����ݣ�1�������ݿ�֪��ƽ��ʱN2��H2��ת����֮��Ϊ![]() ����ӦN2(g)+ 3H2(g)
����ӦN2(g)+ 3H2(g)![]() 2NH3(g)��ƽ�ⳣ������ʽΪK=
2NH3(g)��ƽ�ⳣ������ʽΪK=![]() �����¶��·�Ӧ��ƽ�ⳣ��K=
�����¶��·�Ӧ��ƽ�ⳣ��K=![]() =12.5(L/mol)2��
=12.5(L/mol)2��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڿ��淴ӦN2��g��+3H2��g��![]() 2NH3��g����H��0�������о�Ŀ�ĺ�ʾ��ͼ�������
2NH3��g����H��0�������о�Ŀ�ĺ�ʾ��ͼ�������
A | B | C | D | |
�о�Ŀ�� | ѹǿ�Է�Ӧ��Ӱ��P2��P1 | �¶ȶԷ�Ӧ��Ӱ�� | ƽ����ϵ���ӵ����Է�Ӧ��Ӱ�� | �����Է�Ӧ��Ӱ�� |
ͼʾ |
|
|
|
|
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ƻ���к��е��ۡ������Ǻ����εȣ�ij������ȤС�������һ��ʵ��֤��ijЩ�ɷݵĴ��ڣ�������벢Э������������ʵ�顣
��1����С�Թ�ȡ������ƻ��֭������_________����Һ��������ƻ���к��е��ۡ�
��2����С�Թ�ȡ������ƻ��֭����������Cu(OH)2����Һ�������ȣ�����ש��ɫ�ij�������ƻ���к���____________��д����ʽ����
��3����������һ�������¿��Եõ���ѧʽΪC2H6O�Ļ�����A��
A + CH3COOH������ζ�IJ���
�� ��A���������Ϊ75%��ˮ��Һ��������_____________��
��д��������A��CH3COOH��Ӧ�Ļ�ѧ����ʽΪ______________________���÷�Ӧ������Ϊ_____��
��4��ƻ���к���ƻ���ᣬ�������Է�������Ϊ134��ȡ0.02molƻ���ᣬʹ����ȫȼ�գ���ȼ�պ�IJ����Ⱥ�ͨ����������ˮCaCl2�ͼ�ʯ�ң����߷ֱ�����1.08g �� 3.52g���������C��Hԭ�ӵĸ�����_______��ƻ����ķ���ʽ��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����( )
A.������ӵ��Ų�Ӧ�����Ų���������͵ĵ��Ӳ�
B.��������Ԫ�ض��ԣ�������������Ϊm�����Ӳ���Ϊn����![]() ֵԽ������Խǿ
ֵԽ������Խǿ
C.ͬһ�����У����ź˵���������ӣ������Ӱ뾶������
D.�������������У�ͬ��Ԫ��ԭ�ӵĺ˵�������һ��Ϊ8
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£����淴Ӧ��![]() ��ij�ܱ������дﵽƽ�⣬����˵������ȷ����
��ij�ܱ������дﵽƽ�⣬����˵������ȷ����
A.![]()
B.![]() ����Ӧ�ﵽƽ�⣬�����¶ȣ�������ƽ������
����Ӧ�ﵽƽ�⣬�����¶ȣ�������ƽ������
C.![]() �����ں�����ѹ�������������������粒������������
�����ں�����ѹ�������������������粒������������
D.![]() �����ܱ������дﵽƽ�⣬��������ƽ����Է����������䣬��Ӧһ���ﵽƽ��
�����ܱ������дﵽƽ�⣬��������ƽ����Է����������䣬��Ӧһ���ﵽƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��25ʱ�棬0.2 mol/L��HF��Һ�д�������ƽ�⣺HF![]() H++F-����һ����������ˮ��ƽ�⽫____���������������������������������ƶ�����Һ�е�c(H+)��___������������������С������������������������0.2mol/L�����ᣬ��___�������ٽ���������������HF�ĵ��룬HF�ĵ���ƽ�ⳣ��K��___������������������С����������������
H++F-����һ����������ˮ��ƽ�⽫____���������������������������������ƶ�����Һ�е�c(H+)��___������������������С������������������������0.2mol/L�����ᣬ��___�������ٽ���������������HF�ĵ��룬HF�ĵ���ƽ�ⳣ��K��___������������������С����������������
��2�������������ڵ���ʵ���____�����ڷǵ���ʵ���____���ܵ����������____����ˮ��Һ�ܹ����������____��
��CO2 ��ͭ ���ռ� ��NH3.H2O ��ʯī ��̼���� ��CH3COOH ������ ������ ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڻ�ѧ��Ӧ���ʺͻ�ѧ��Ӧ�ȵ�˵������ȷ���ǣ�������
A.��ѧ��Ӧ�����Ǻ�����ѧ��Ӧ���п����̶ȵ�������
B.��ѧ��Ӧ����ͨ���õ�λʱ�������ɻ�����ij���ʵ������Ķ�������ʾ
C.��һ�����淴Ӧ�ﵽƽ��״̬ʱ������������Ӧ���ܴﵽ���ȣ���ʹ�����ı䣬���ȶ����ı�
D.ƽ��״̬��һ�־�ֹ��״̬����Ϊ��Ӧ����������Ũ���Ѿ����ٸı�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��̽����������(SO2��NO2��Cl2)�����ʣ�ijͬѧ���������ʵ�飺
��1��ʵ��һ������������ƿ�ռ��������������������壬Ȼ���䵹����ˮ���С��ֱ���ͨ������O2��Cl2����ͼ1��ʾ��һ��ʱ���D��Eװ�õļ���ƿ�г�����Һ��Fװ�õļ���ƿ�л�������ʣ�ࡣ
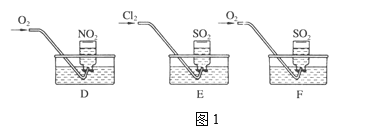
(����ƿ��Һ�岻��ɢ)��
��д��װ��E�з�Ӧ�����ӷ���ʽ��____________________.
�ڼ����ʵ������Ϊ��״������װ��D�ļ���ƿ��������Һ���ʵ����ʵ���Ũ��Ϊ____________.
��ͨ������ǰ��Fװ�õ�ˮ����μӼ�����ɫʯ����Һ���۲쵽��������Fװ�ü���ƿ����Һ��dz��ɫ��ͨ���������ܹ۲쵽��ʵ�������� _____________________________��д����Ӧ���ܻ�ѧ����ʽ��________________.
��2��ʵ������ֱ�������ͼ��ʾװ��̽�������������ԡ�
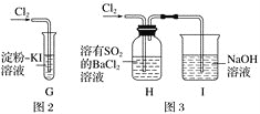
��G�е�������_______________��ԭ���� ________________________(�û�ѧ����ʽ��ʾ)��
��H�������_________________________.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ�жϣ�����˵����ȷ����(����)
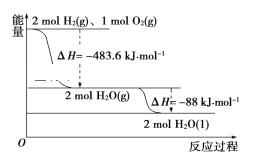
A. ������ȼ������H����241.8 kJ��mol��1
B. 2 mol H2(g)��1mol O2(g)�������������2 mol H2O(g)�������������
C. Һ̬ˮ�ֽ���Ȼ�ѧ����ʽΪ2H2O(l)=2H2(g)��O2(g)����H����571.6 kJ��mol��1
D. H2O(g)����H2O(l)ʱ���ϼ����յ�����С�ڳɼ��ų�������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com