
| m |
| M |
| m |
| M |
| m |
| M |
| 1g |
| 2g/mol |
| m |
| M |
| 16g |
| 64g/mol |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
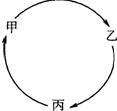 甲、乙、丙三种物质有如图所示的转化关系.
甲、乙、丙三种物质有如图所示的转化关系.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等浓度、等体积的NaOH 和二元弱酸H2A 混和溶液中:c(Na+)+c(H+)=c(HA-)+c(OH-)+c(A2-) |
| B、1 L 0.1 mol?L-1 CuSO4?(NH4)2SO4?6H2O 的溶液中:c(NH4+)>c(SO42-)>c(Cu2+)>c(H+)>c(OH-) |
| C、物质的量浓度相等的Na2CO3 和NaHCO3 溶液等体积混合后的溶液中:3c(H2CO3)+2c(H+)+c(HCO3-)=2c(OH-)+c(CO32-) |
| D、已知两种弱酸HA、HB 的电离平衡常数Ka(HA)>Ka(HB),常温下0.1 mol?L-1的HA、HB、NaA、NaB 溶液中:pH(NaA)>pH(NaB)>pH(HA)>pH(HB) |
查看答案和解析>>
科目:高中化学 来源: 题型:
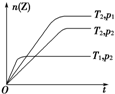 反应2X(g)+Y(g)?2Z(g),△H<0在不同温度(T1和T2)及压强(p1和p2)下,产物Z的物质的量n与反应时间t的关系如图所示.下列判断正确的是( )
反应2X(g)+Y(g)?2Z(g),△H<0在不同温度(T1和T2)及压强(p1和p2)下,产物Z的物质的量n与反应时间t的关系如图所示.下列判断正确的是( )| A、T1<T2,p1<p2 |
| B、T1<T2,p1>p2 |
| C、T1>T2,p1>p2 |
| D、T1>T2,p1<p2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 | B、2 | C、3 | D、4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、①③ | C、②③ | D、③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纯碱溶液去油污 |
| B、铁在潮湿的环境下生锈 |
| C、向氯化铁溶液中滴入氢氧化钠溶液产生红褐色沉淀 |
| D、浓硫化钠溶液有臭味 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com