
【题目】T℃时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列描述正确的是( )
A.平衡时X、Y的转化率相同
B.达到平衡后,将容器体积压缩为1L,平衡向正反应方向移动
C.T℃时,该反应的化学方程式为:X(g)+Y(g) ![]() 2Z(g),平衡常数K=40
2Z(g),平衡常数K=40
D.T℃时,若起始时X为0.71mol,Y为1.00mol,则平衡时Y的转化率约为60%
【答案】D
【解析】根据图知,X、Y是反应物而Z是生成物,达到平衡状态时,△n(X)= n(1.20-0.40) mol=0.80mol、△n(Y)=n(1.00-0.20)mol=0.80mol、△n(Z)= n(1.60-0.00)mol=1.60mol,同一可逆反应同一时间段内各物质物质的量变化量之比等于其计量数之比,所以该反应方程式中X、Y、Z的计量数之比为0.80mol:0.80mol:1.60mol=1:1:2,则该反应方程式为X(g)+Y(g) ![]() 2Z(g),
2Z(g),
A.X、Y的转化率分别为:(0.80mol÷1.20mol)×100%=67%、 (0.80mol÷1.00mol)×100%=80%,错误;
B.该反应前后气体计量数之和不变,则压强不影响平衡移动,所以将容器体积压缩为1L,平衡不移动,错误;
C.反应达到平衡状态时,c(X)=0.40mol÷2L=0.20mol/L,c(Y)=0.20mol÷2L=0.10mol/L、c(Z)=1.60mol÷2L=0.80mol/L,该反应平衡常数K=c2(Z)/c(X)·c(Y)=(0.80×0.80)÷(0.20×0.10)=32,错误;
D.温度不变,化学平衡常数不变,设参加反应的Y的物质的量为amol,根据方程式知,参加反应的X物质的量为amol,生成Z的物质的量为2amol,平衡时c(X)= (0.71a)÷2mol/L、c(Y)= (1.00a)÷2mol/L、c(Z)=(2a÷2)mol/L=amol/L。A2÷ [(0.71a)/2× (1.00a)/2]=32,a=0.60,Y转化率为 (0.60mol÷1.00mol)×100%=60%,正确。
所以答案是:D
【考点精析】认真审题,首先需要了解化学平衡常数的含义(指在一定条件下的可逆反应里,正反应和逆反应的速率相等,反应混合物中各组分的浓度不变的状态),还要掌握化学平衡状态本质及特征(化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效))的相关知识才是答题的关键.


科目:高中化学 来源: 题型:
【题目】25℃时,溶质浓度均为0.1mol/L的下列溶液中粒子浓度关系正确的是已知:H2C2O4属于二元弱酸.( )
A.Na2S溶液:c(Na+)>c(S2﹣)>c(HS﹣)>c(OH﹣)>c(H2S)
B.Na2CO3溶液:c(Na+)+c(H+)=c(CO ![]() )+c(HCO
)+c(HCO ![]() )+c(OH﹣)
)+c(OH﹣)
C.Na2C2O4溶液:c(OH﹣)=c(H+)+c(HC2O ![]() )+2c(H2C2O4)
)+2c(H2C2O4)
D.CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO﹣)+c(CH3COOH)+2c(Cl﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由2﹣溴丙烷为主要原料制取1,2﹣丙二醇时,需要经历的反应依次是( )
A.加成→消去→取代
B.消去→加成→取代
C.取代→消去→加成
D.取代→加成→消去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH3﹣CH═CH2+HBr﹣﹣→CH3﹣CHBr﹣CH3(主要产物),1mol某烃A充分燃烧后可以得到8mol CO2和4mol H2O.该烃A在不同条件下能发生如下面所示的一系列变化. 
(1)A的化学式: , A的结构简式 .
(2)上述反应中,①是反应,⑦是反应.(填反应类型)
(3)写出C,D,E,H物质的结构简式:C , D , E , H .
(4)写出⑥反应的化学方程式 ![]() . 写出⑦反应的化学方程式
. 写出⑦反应的化学方程式 ![]() .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)海水中含有大量的氯化钠。氯化钠中的金属元素位于元素周期表第________族。
(2)目前国际上使用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是________(填“物理变化”或“化学变化”)。
(3)工业上利用电解饱和食盐水可制得重要化工产品,反应方程式为:2NaCl+2H2O2NaOH+H2↑+Cl2↑,利用电解所得气体制36.5%的浓盐酸1000 t,最少需要消耗食盐________t。
(4)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下:
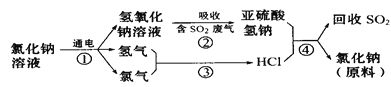
写出②④的化学反应方程式______________________________、 _________________。
(5)上述亚硫酸氢钠与甲醛经过一定反应,可以合成俗称“吊白块”的物质。因吊白块对人体有害,不能用于食品漂白。其结构简式为HOCH2SO3Na,根据其结构特点,“吊白块”能发生的反应有________。
A.皂化反应 B.聚合反应 C.与金属钠反应 D.氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu3N的晶胞结构如图,N3﹣的配位数为 , Cu+半径为acm,N3﹣半径为bcm,Cu3N的密度为gcm﹣3 . (阿伏加德罗常数用NA表示,Cu、N相对分子质量为64、14) 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定工业纯碱中Na2CO3的质量分数(含少量NaCl),甲、乙两位学生分别设计了一套方案。学生甲的实验流程如图所示:
学生乙设计的实验步骤如下:
①称取样品,为1.150g;
②溶解后配成250mL溶液;
③取20mL上述溶液,加入甲基橙 2~3滴;
④用0.1140mol/L的标准盐酸进行滴定;
⑤数据处理.
回答下列问题:
(1)甲学生设计的方案中试剂A可以选用(填编号)
a.CaCl2 b.BaCl2 c.AgNO3
(2)操作Ⅱ后还应对滤渣依次进行①②两个实验操作步骤.其中,证明前面一步的操作已经完成的方法是。
(3)学生乙某次实验开始滴定时,盐酸溶液的刻度在0.00mL处,当滴至时达到滴定终点,此时盐酸溶液的刻度在14.90mL处,乙同学以该次实验数据计算此样品中Na2CO3的质量分数是(保留两位小数).乙同学的这次实验结果与老师给出的理论值非常接近,但老师最终认定他的实验方案设计不合格,你认为可能的原因是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表格中各项分类都正确的一组是( )
纯净物 | 混合物 | 电解质 | 非电解质 | |
A | 冰水混合物 | CuSO45H2O | 液态KNO3 | 蔗糖 |
B | CaO | 海水 | 铜 | 酒精 |
C | 液氯 | 铝合金 | AgCl | CO2 |
D | 氢氧化钠 | 空气 | Na2SO4溶液 | 食醋 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com