
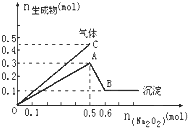
【题目】向一定量的Mg2+、NH4+、Al3+混合溶液中加入Na2O2的量与生成沉淀和气体的量(纵坐标)的关系如图所示,则溶液中Mg2+、NH4+、Al3+三种离子的物质的量之比为( )
A.1:1:2B.2:2:1C.1:2:2D.9:2:4
【答案】C
【解析】
根据图象分析,A点时沉淀的量最大,所以沉淀是氢氧化铝和氢氧化镁,从A点到B点,沉淀的质量减少,减少的量是氢氧化铝,为0.2mol,沉淀不溶解的量是氢氧化镁,物质的量是0.1mol,根据原子守恒确定镁离子、铝离子的物质的量;当沉淀的量最大时,根据过氧化钠的物质的量计算生成氧气的物质的量,根据气体总的物质的量计算生成氨气的物质的量,根据氮原子守恒从而计算铵根离子的物质的量。
由图可知,沉淀中含0.1mol Mg(OH)2和0.2 molAl(OH)3,即原溶液中含Mg2+0.1mol,含Al3+0.2mol,Mg2++2OH-=Mg(OH)2↓,Al3++3OH-=Al(OH)3↓,沉淀2种金属阳离子共需NaOH的物质的量为0.1mol×2+0.2mol×3=0.8mol,由图中横坐标知与3种阳离子恰好完全反应时需Na2O20.5mol,而0.5molNa2O2与水反应生成1molNaOH和0.25molO2,则与铵根反应的氢氧根离子为1mol-0.8mol=0.2mol,由NH4++OH-![]() NH3↑+H2O,则可得原溶液中含0.2molNH4+,所以Mg2+、NH4+、Al3+之比=0.1mol:0.2mol:0.2mol=1:2:2;
NH3↑+H2O,则可得原溶液中含0.2molNH4+,所以Mg2+、NH4+、Al3+之比=0.1mol:0.2mol:0.2mol=1:2:2;
综上所述,C项正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】某研究性学习小组为了探究醋酸的电离情况,进行了如下实验:
(1)取冰醋酸配制250mL 0.4 mol·L-1的醋酸溶液,用0.4mol·L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
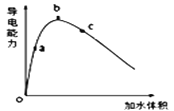
①将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示。则稀释过程中溶液的pH由大到小的顺序____(填字母)。
②为标定该醋酸溶液的准确浓度,用0.2000mol·L-1的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
该醋酸溶液的准确浓度为_____________(保留小数点后四位),上述标定过程中,造成测定结果偏高的原因可能是_____________(多选、错选不得分)。
a.未用标准液润洗碱式滴定管
b.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
c.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
d.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
(2)该小组同学探究浓度对醋酸电离程度的影响时,用pH计测定25℃时不同浓度的醋酸的pH,其结果如下:
醋酸浓度( mol·L-1) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
①根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是___________。
②简述用pH试纸测 0.1mol·L-1 醋酸溶液pH的方法___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
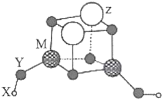
【题目】短周期元素X、Y、Z、M的原子序数依次增大,它们组成一种团簇分子Z2M2Y4(YX)2,其结构如图所示,其中X、M的族序数均等于周期序数,Y原子核外最外层电子数是其电子总数的3/4。下列说法正确的是
A.简单离子半径:Z > M > Y > X
B.Z和M的单质均能溶于NaOH溶液
C.X和Y形成的X2Y2是离子化合物
D.Z的最高价氧化物的水化物是中强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是核电荷数依次增大的五种短周期主族元素。A元素的原子核内只有1个质子;B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应的水化物的化学式为HBO3;C元素原子的最外层电子数比次外层电子数多4;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E元素同主族。
(1)B在元素周期表中的位置是_________。
(2)E元素形成的最高价氧化物对应的水化物的化学式为______,由A、B、C三种元素形成的离子化合物的化学式为______。
(3)C、D、E形成的简单离子的半径大小关系是_________(用离子符号表示)。
(4)用电子式表示化合物A2C的形成过程:__________________,化合物D2C2中含有的化学键是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下述转化关系,回答问题:
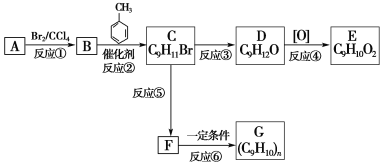
已知:①+CH3Br![]() CH3+HBr;
CH3+HBr;
②C物质苯环上一卤代物只有两种。
(1)写出B物质的名称__________;D物质的结构简式________。
(2)写出反应②的类型________;反应⑤的条件________。
(3)写出反应⑥的化学方程式:________________________________。
(4)写出D+E反应的化学方程式:_______________。
(5)反应②还有可能生成一种C16H18的有机物,其苯环上一卤代物也只有两种,写出它的结构简式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是人体必需的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:
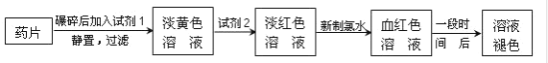
试回答下列问题:
(1)试剂1是__,试剂2是__,加入新制氯水后溶液中发生的离子反应方程式是__、_____。
(2)加入试剂2后溶液中颜色由淡黄色转变为淡红色是因为__,写出+2价Fe在空气中转化为+3价Fe的化学方程式__。
(3)该同学猜想红色溶液变为无色溶液的原因是溶液中的+3价铁被还原为+2价铁,你认为该同学的猜想合理吗?__。若你认为合理,请说明理由(若你认为不合理,该空不作答);若你认为不合理请提出你的猜想并设计一个简单的实验加以验证(若你认为合理,该空不作答)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是硫酸试剂标签上的部分内容。请回答下列问题:

(1)该浓硫酸中溶质、溶剂分子数目之比为___,现用该浓H2SO4来配制480mL、0.3mol·L-1的稀H2SO4,需量取该浓H2SO4的体积为___mL。
(2)配制时,下列仪器中必须使用___(填代号),还缺少的仪器是___、___。
①托盘天平(带砝码) ②10mL量筒 ③20mL量筒 ④烧杯 ⑤玻璃棒 ⑥100mL容量瓶 ⑦漏斗 ⑧烧瓶
(3)在配制过程中,下列操作中能使所配溶液的浓度偏高的有___(填代号)。
①用量筒量取98%的硫酸时俯视
②洗涤量取浓硫酸的量筒,并将洗涤液转移到容量瓶中
③未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
④转移前,容量瓶中含有少量蒸馏水
⑤定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
⑦定容时,仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟碳铈矿(主要成分为CeFCO3)是提取稀土化合物、冶炼铈的重要矿物原料,根据如图以氟碳铈矿为原料提取铈的工艺流程图,回答问题:
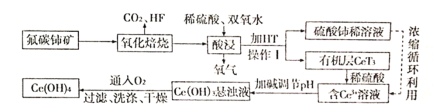
(1)CeFCO3中Ce的化合价为_____;氧化焙烧时不能使用陶瓷容器,原因是______。
(2)氧化焙烧后的产物之一为CeO2,则酸浸时发生反应的离子方程式为_________。
(3)HT是一种难溶于水的有机溶剂,则操作I的名称为________。
(4)为了提高酸浸率,可以适当提高反应温度,但温度偏高浸出率反而会减小,其原因是__________。
(5)已知有机物HT能将Ce3+从水溶液中萃取出来,该过程可表示为:Ce3+(水层)+3HT(有机层)![]() CeT3(有机层)+3H+(水层)。向CeT3(有机层)中加入稀硫酸能获得较纯的含Ce3+水溶液,从平衡角度解释其原因:________。
CeT3(有机层)+3H+(水层)。向CeT3(有机层)中加入稀硫酸能获得较纯的含Ce3+水溶液,从平衡角度解释其原因:________。
(6)写出向Ce(OH)3悬浊液中通入氧气得到产品Ce(OH)4的化学方程式:________。
(7)298K时,向c(Ce3+)=0.02 mol/L的溶液中加入氢氧化钠来调节溶液的pH,若反应后溶液pH=10,此时Ce3+是否沉淀完全?______。(要求列式计算,已知:Ksp[Ce(OH)3]=1.0×10-20,c(Ce3+)<1.0×10-5 mol/L视为沉淀完全)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液氨与水性质相似,也存在微弱的电离:2NH3![]() NH4++NH2—,其离子积常数K=c(NH4+)·c(NH2—)=2×l0-30,维持温度不变,向液氨中加入少量NH4Cl固体或NaNH2固体,不发生改变的是
NH4++NH2—,其离子积常数K=c(NH4+)·c(NH2—)=2×l0-30,维持温度不变,向液氨中加入少量NH4Cl固体或NaNH2固体,不发生改变的是
A. 液氨的电离平衡 B. 液氨的离子积常数
C. c(NH4+) D. c(NH2—)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com