
【题目】某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示。
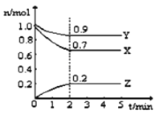
(1)由图中所给数据进行分析,该反应的化学方程式为 。
(2)反应从开始至2分钟,用Z的浓度变化表示的平均反应速率为v(Z)= 。
(3)2min反应达平衡容器内混合气体的平均相对分子质量比起始时 (填增大、减小或不变),混合气体密度比起始时 (填增大、减小或不变)。
(4)下列措施能加快反应速率的是 。
A.恒容时充入X B.及时分离出Z C.降低温度 D.选择高效的催化剂
(5)下列说法正确的是 。
A.升高温度可以改变化学反应的平衡状态
B.已知正反应是吸热反应,升高温度平衡向右移动,正反应速率加快,逆反应速率减慢
C.达到化学反应的平衡状态与时间长短无关
D.化学反应的平衡状态是不可能改变的
E.增大Y的浓度,正反应速率加快,逆反应速率减慢
【答案】(1)3X(g)+Y(g) ![]() 2Z(g);(2)0.05mol/(Lmin);(3)增大;(4)AD;(5)A。
2Z(g);(2)0.05mol/(Lmin);(3)增大;(4)AD;(5)A。
【解析】
试题分析:(1)由图象可以看出,反应中X、Y的物质的量减少,应为反应物,Z的物质的量增多,应为生成物,当反应进行到2min时,△n(X)=0.3mol,△n(Y)=0.1mol,△n(Z)=0.2mol,则△n(X):△n(Y):△n(Z)=3:1:2,参加反应的物质的物质的量之比等于化学计量数之比,则反应的方程式为:3X+Y![]() 2Z;
2Z;
(2)反应开始至2min末,Z的反应速率为:v(Z)= △c(Z)÷△t= 0.2mol÷2L÷2min= 0.05mol/(Lmin);
(3)该反应的正反应是气体体积减小的反应,由于气体的质量不变,气体的物质的量减小,所以平均摩尔质量增大;
(4)A.恒容时充入X,物质的浓度增大,反应速率加快,正确;B.及时分离出Z,使物质的浓度降低,反应速率减小,错误;C.降低温度,物质的内能减小,反应速率减慢,错误;D.选择高效的催化剂,化学反应速率大大加快,正确;
(5)A.化学反应过程中都伴随着能量变化,所以升高温度可以改变化学反应的平衡状态,使化学平衡发生移动,正确;B.已知正反应是吸热反应,升高温度化学平衡向吸热的正反应方向移动,正反应速率加快,逆反应速率也加快,错误;C.化学反应速率越快,达到化学反应的平衡状态所需的时间就越短,所以达到化学反应的平衡状态与时间长短有关,错误;D.化学反应的平衡状态是一定条件下的平衡,外界条件改变,平衡被破坏,会建立新的条件下的平衡状态,所以化学平衡是可以改变的,错误;E.增大Y的浓度,正反应速率加快,逆反应速率也加快,错误。


科目:高中化学 来源: 题型:
【题目】下列有关能量的叙述错误的是( )
A.化学反应均伴随着能量的变化
B.物质的化学能可以在一定条件下转化为热能、电能,为人类利用
C.吸热反应中由于反应物总能量小于生成物总能量,因而没有利用价值
D.需要加热才能发生的反应不一定是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化工厂用软锰矿(含MnO2及少量Al2O3)和闪锌矿(含ZnS及少量FeS)联合生产Zn、MnO2,其部分生产流程如下:

已知:过滤(Ⅱ)所得滤液是MnSO4、ZnSO4、Fe2(SO4)3、Al2(SO4)3的混合液。相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)如下表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Zn(OH)2 | Mn(OH)2 |
开始沉淀时的pH | 2.7 | 4.0 | 6.4 | 7.7 |
完全沉淀时的pH | 3.7 | 5.2 | 8.0 | 10.4 |
(1)加热、浸取时所加矿石均需粉碎,其目的是 。
(2)写出FeS和MnO2和稀硫酸反应的离子方程式: 。
(3)试剂X的作用是调节溶液的pH以生成Fe(OH)3、Al(OH)3。pH调节的范围是 ,试剂X可以选用 (填选项字母)。
A.MnCO3 B.Na2CO3 C.Zn2(OH)2CO3 D.NH3·H2O
(4)电解(Ⅴ)中阳极的电极反应式为 。
(5)Zn和MnO2是制作电池的原料。某锌-锰碱性电池以KOH溶液为电解质溶液,其电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)。该电池的正极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
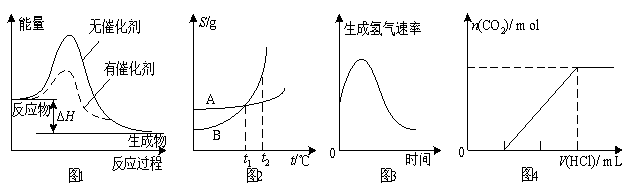
A.图1表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
B.图2表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数B>A
C.图3表示镁条放入盐酸中生成氢气速率随时间的变化,起初反应速率加快的原因可能是该反应为放热反应
D.图4表示在含等物质的量NaOH、Na2CO3的混合溶液中滴加0.1 mol·L-1盐酸至过量时,产生气体的体积与消耗盐酸的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.加入硫酸铜可使锌与稀硫酸的反应速率加快,说明Cu2+具有催化作用
B.向某溶液中滴加硝酸酸化的BaCl2溶液产生白色沉淀,则该溶液中含有SO2-4
C.在电解精炼铜过程中,阳极质量的减少多于阴极质量的增加
D.298 K时,2H2S(g)+SO2(g)=3S(s)+2H2O(l)能自发进行,则其ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的KOH溶液时,下列操作对实验结果没有影响的是( )
A. 容量瓶中原有少量蒸馏水 B. 洗涤烧杯和玻棒的溶液未转入容量瓶中
C. 定容时观察液面俯视 D. 定容时观察液面仰视
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化钠主要用于皮革、毛纺、高档纸张、染料等行业。生产硫化钠大多采用无水芒硝(Na2SO4)—炭粉还原法,其流程示意图如下:

(1)上述流程中“碱浸”后,物质A必须经过 (填写操作名称)处理后,方可“煅烧”;若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生的总的化学反应方程式为 。
(2)上述流程中采用稀碱液比用热水更好,理由是稀碱液能 Na2S水解(选促进或抑制)
(3)取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌。若反应后测得溶液的pH=4,则此时溶液中c( S2-)= mol·L-1。(已知:常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20)

(4)①皮革工业废水中的汞常用硫化钠除去,汞的去除率与溶液的pH和x(x代表硫化钠的实际用量与理论用量的比值)有关(如右图所示)。为使除汞效果最佳,应控制的条件是x控制 、pH控制 。
②某毛纺厂废水中含0.001 mol·L-1的硫化钠,与纸张漂白后的废水(含0.002 mol·L-1 NaClO)按1:2的体积比混合,能同时较好处理两种废水,处理后的废水中所含的主要阴离子有 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S废气资源化利用途径之一是回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)═S2(s)+2H2O(l)△H=﹣632kJmol﹣1.如图为质子膜H2S燃料电池的示意图.下列说法正确的是( )

A.电极a为电池的正极
B.电极b上发生的电极反应为:O2+2H2O+4e﹣=4 OH﹣
C.电路中每流过4mol电子,电池内部释放632kJ热能
D.每17gH2S参与反应,有1mol H+经质子膜进入正极区
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com