
【题目】能正确表示下列反应的离子方程式是
A.向氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl-
B.向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
C.碳酸氢钠溶液与硫酸氢钠溶液反应:HCO3-+H+=CO2↑+H2O
D.硫酸铝溶液中加入过量氨水: Al3++3OH-=Al(OH)3↓
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】三种正盐的混合溶液中含有0.2 molNa+、0.25molMg2+、0.4mol Cl-,则SO42-离子的物质的量为
A. 0.1 mol B. 0.3 mol C. 0.5mol D. 0.15mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律.图2中,A,B,C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸.已知常温下浓盐酸与高锰酸钾能反应生成氯气.
(1)甲同学实验(如图1)中选用的三种物质名称分别为:; 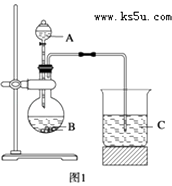
(2)乙同学实验(如图2)中:A处反应的离子方程式为:; B处的实验现象为:;该实验不能完全证明卤素性质的递变规律,请简述原因: . 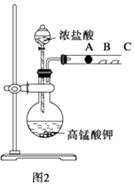
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据陶瓷的生产原理,可以得出硅酸盐工业的一般特点是( )
①以含硅物质作为原料 ②主要产物是硅酸盐 ③反应条件是高温 ④反应原理是复杂的物理和化学变化
A.①③
B.①②③
C.①②③④
D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知醋酸在水溶液中建立如下电离平衡: CH3COOH![]() H++ CH3COO-,若只改变一个条件,一定可以使c(CH3COOH)/c(H+)减小的是
H++ CH3COO-,若只改变一个条件,一定可以使c(CH3COOH)/c(H+)减小的是
A. 通氯化氢气体 B. 加入少量醋酸钾固体
C. 加入少量氢氧化钠固体 D. 通入少量冰醋酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气阴极祛制备H2O2是一种环境友好型制备方法,装置如图所示,下列说法错误的是
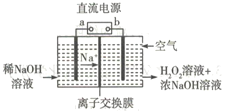
A. b为直流电源的负极
B. 本装置使用的交换膜为阳离子交换膜
C. 通入空气的电极反应式可能为O2+2e-+2H2O=H2O2+2OH-
D. 若生成17g双氧水,则需要通入含11.2 LO2 的空气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组用如图所示装置A,B分别探究金属锌与稀硫酸的反应,实验过程中A烧杯内的溶液温度升高,B烧杯的电流计指针发生偏转,请回答以下问题. 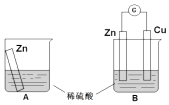
(1)A烧杯中反应的离子方程式为 .
(2)B中Zn板是极,发生的电极反应是 , Cu板上的现象是 , 发生的电极反应是 .
(3)从能量转化的角度来看,A,B中反应物的总能量(填“大于”、“小于”或“等于”)生成物总能量,A中是将化学能转变为 , B中主要是将化学能转变为 .
(4)该小组同学反思原电池的原理,其中观点正确的是(填字母序号).
A.原电池反应的过程中一定有电子转移
B.原电池装置需要2个电极
C.电极一定不能参加反应
D.氧化反应和还原反应可以拆开在两极发生.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组用CO还原Fe2O3 , 并在实验结束后用磁铁吸出生成的黑色粉末X进行探究. [探究目的]分析黑色粉末X的组成,并进行相关实验.
[查阅资料]
I.CO还原Fe2O3的实验中若温度不同、受热不均时会生成Fe3O4 , 也能被磁铁吸引.
II.Fe3O4+8H+=2Fe3++Fe2++4H2O
(1)[猜想假设]黑色粉末X的组成可能是、 , 或二者的混合物. [实验探究]
编号 | 实验操作 | 实验现象 |
① | 取少量黑色粉末X放入试管中,注入足量的一定浓度的盐酸,微热 | 黑色粉末逐渐溶解,同时有气泡产生,溶液呈浅绿色. |
② | 向上述试管中滴加几滴KSCN溶液,振荡 | 溶液没有呈现红色 |
实验①中产生气泡的离子方程式为 .
(2)根据②中溶液未呈红色,不能推断出黑色粉末X中无Fe3O4 , 请用离子方程式解释原因: .
(3)为了证明黑色粉末X中是否含有Fe3O4 , 该小组进行如图所示实验: 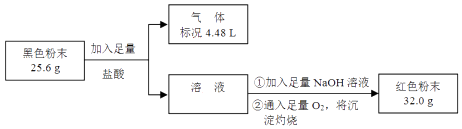
请根据数据分析说明黑色粉末X中是否含有Fe3O4 . .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 27gAl与NaOH完全反应,转移的电子数为0.1NA
B. 1L0.1mol/LNaHCO3溶液中,HCO3-的数量为0.1NA
C. 标准状况下,11.2L乙烷中含有的共用电子对数目为3NA
D. 0.1mol18O中含有的中子数为1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com