

| A、待KNO3热饱和溶液冷却 |
| B、用工业酒精制取无水乙醇结晶后进行快速过滤 |
| C、实验室收集SO2气体 |
| D、实验室干燥氨气 |


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
| 催化剂 |
| △ |
 | 0.1MPa | 0.5MPa | 1MPa | 10MPa |
| 400℃ | 99.2% | 99.6% | 99.7% | 99.9% |
| 500℃ | 93.5% | 96.9% | 97.8% | 99.3% |
| 600℃ | 73.7% | 85.5% | 89.5% | 96.4% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2(g)的消耗速率与I2(g)的生成速率始终相等 |
| B、反应过程中,H2(g)和I2(g)的转化率始终相等 |
| C、平衡前,正、逆反应速率的比值恒定 |
| D、反应开始至2min末,v(H2)=0.3mol?L-1?min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可逆反应在一定条件下有一定的限度,当反应进行到一定限度后,反应物不再转化为生成物 |
| B、决定化学反应速率的主要因素是参加反应的物质的性质 |
| C、化学反应的速率和限度均可通过改变化学反应条件而改变 |
| D、化学反应达到平衡状态时,只要条件不改变,各物质的浓度就不再改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
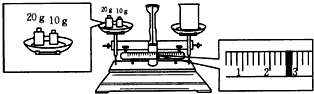
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
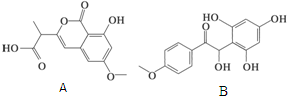
| A、二者都能与Br2发生反应,等物质的量A和B最多消耗的Br2的比例为2:3 |
| B、有机物A和B既可以与FeCl3溶液发生显色反应,又可以和NaHCO3溶液反应 |
| C、1 mol B最多能与6 mol氢气反应 |
| D、等物质的量A和B最多消耗的氢氧化钠质量比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com