
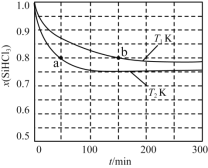
【题目】恒容条件下,1 mol SiHCl3发生如下反应:2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g)。已知:v正=v消耗(SiHCl3)=k正x2(SiHCl3),v逆=2v消耗(SiH2Cl2)=k逆x(SiH2Cl2)x(SiCl4),k正、k逆分别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(SiHCl3)随时间的变化。下列说法正确的是
SiH2Cl2(g)+SiCl4(g)。已知:v正=v消耗(SiHCl3)=k正x2(SiHCl3),v逆=2v消耗(SiH2Cl2)=k逆x(SiH2Cl2)x(SiCl4),k正、k逆分别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(SiHCl3)随时间的变化。下列说法正确的是
A. 该反应为放热反应,v正,a<v逆,b
B. 化学平衡状态时2v消耗(SiHCl3)=v消耗(SiCl4)
C. 当反应进行到a处时,v正/v逆=16/9
D. T2 K时平衡体系中再充入1 mol SiHCl3,平衡正向移动,x(SiH2Cl2)增大
【答案】C
【解析】
A.因两曲线对应的状态只是温度不同,由图像知达到平衡所需时间T2K小于T1K,温度越高反应速率越快,所以温度T2>T1。又T2K下达到平衡时SiHCl3的物质的量分数比T1K平衡时小,说明升温平衡向正反应方向移动,由此推知该反应为吸热反应,选项A错误;
B. 化学平衡状态时v消耗(SiHCl3)=2v消耗(SiCl4),选项B错误;
C. 2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g)反应前后分子数不变,即反应开始至达平衡的过程中混合气体总物质的量始终为1mol,由图像知T2K下达到平衡时SiHCl3的物质的量分数为0.75,则此时SiH2Cl2和SiCl4的物质的量分数均为0.125,因为平衡时V正=V逆,V正=k正x2(SiHCl3)=0.752k正,V逆=k逆x(SiH2Cl2)x(SiCl4)=0.1252k逆,则0.752k正=0.1252k逆,
SiH2Cl2(g)+SiCl4(g)反应前后分子数不变,即反应开始至达平衡的过程中混合气体总物质的量始终为1mol,由图像知T2K下达到平衡时SiHCl3的物质的量分数为0.75,则此时SiH2Cl2和SiCl4的物质的量分数均为0.125,因为平衡时V正=V逆,V正=k正x2(SiHCl3)=0.752k正,V逆=k逆x(SiH2Cl2)x(SiCl4)=0.1252k逆,则0.752k正=0.1252k逆,![]() =
=![]() ,因k正和k逆只与温度有关,反应进行到a点处时V正= k正x2(SiHCl3)=0.82k正,V逆= k逆x(SiH2Cl2)x(SiCl4)=0.12k逆。
,因k正和k逆只与温度有关,反应进行到a点处时V正= k正x2(SiHCl3)=0.82k正,V逆= k逆x(SiH2Cl2)x(SiCl4)=0.12k逆。![]() ×
×![]() =
=![]() ×
×![]() =
=![]() 。选项C正确;
。选项C正确;
D.恒容条件下再充入1molSiHCl3,相当于增大压强,而2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g)反应前后气体体积不变,所以平衡不移动,x(SiH2Cl2)不变,选项D错误;
SiH2Cl2(g)+SiCl4(g)反应前后气体体积不变,所以平衡不移动,x(SiH2Cl2)不变,选项D错误;
答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】实验室用如图所示装置来制备乙炔,并验证乙炔的某些化学性质,制备的乙炔气体中往往含有少量的H2S气体,请按下列要求填空:
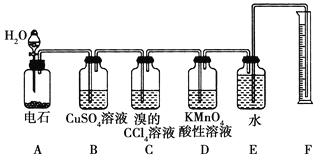
(1)实验室制乙炔的化学方程式是____________________________;为了得到较为平稳的乙炔气流,装置A的分液漏斗中常用________________来代替水。
(2)装置B中CuSO4溶液的作用是________________。
(3)装置C中观察到的现象是_________________,反应的化学方程式是___________________。
(4)装置D中观察到的现象是_________________,该反应的类型是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯:
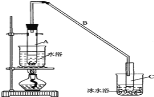
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | -103 | 83 | 难溶于水 |
已知: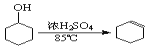 +H2O
+H2O
(1)制备粗品:将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是__,导管B除了导气外还具有的作用是__。
②试管C置于冰水浴中的目的是__。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在__层(填“上”或“下”),分液后用__(填入编号)洗涤。
A.KMnO4溶液 B.稀H2SO4 C.Na2CO3溶液
②如再将环己烯进行蒸馏,冷却水应从__口进入(填“上”或“下”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种优良的消毒剂,常将其制成NaClO2固体,以便运输和贮存,过氧化氢法备NaClO2固体的实验装置如图所示。
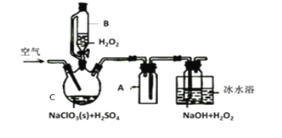
已知:①2NaC1O3+H2O2+H2SO4=2C1O2↑+O2↑+Na2SO4+2H2O
2ClO2+H2O2+2NaOH=2NaClO2+O2↑+2H2O
②ClO2熔点-59℃、沸点11℃,浓度过高时易发生分解;
③H2O2沸点150℃
(1)冰水浴冷却的目的是___。
(2)空气流速过快或过慢,均降低NaClO2产率,试解释其原因,空气流速过慢时,__。
(3)Cl-存在时会催化ClO2的生成。反应开始时在C中加入少量盐酸,ClO2的生成速率大大提高,并产生微量氯气。该过程可能经两步完成,请将其补充完整:
①___(用离子方程式表示)②H2O2+Cl2=2Cl-+O2+2H+
(4)NaClO2纯度测定:
①准确称取所得NaClO2样品10.0g于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(C1O2-的产物为Cl-),将所得混合液配成250mL待测溶液;
②取25.00mL待测液,用2.0mol·L-1Na2S2O3标准液滴定(I2+2S2O32-=2I-+S4O62-),以淀粉溶液做指示剂,达到滴定终点时的现象为__,重复滴定3次,测得Na2S2O3标准液平均用量为20.00mL,则该样品中NaClO2的质量分数为___。(M(NaClO2)=90.5g/mol)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为比较卤素单质的氧化性进行以下实验:①将新制氯水滴入溴化钠溶液中,溶液变黄色;②将新制氯水滴入碘化钾溶液中,溶液变褐色。下列有关说法不合理的是( )
A.①中发生的离子反应为![]()
B.向②所得溶液中再加入![]() 振荡,静默,下层溶液呈紫红色
振荡,静默,下层溶液呈紫红色
C.将①、②可得出结论:氧化性![]()
D.将②中新制氯水换成溴水,若实验现象相同,即可得出氧化性![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组的两物质作用时,反应条件或反应物用量的改变对生成物没有影响的是
A.Na2O2与CO2B.Na与O2C.NaOH与AlCl3D.C与O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ. 砷化镓为第三代半导体,以其为材料制造的灯泡寿命长.耗能少。已知砷化镓的晶胞结构如图所示。请回答下列问题:
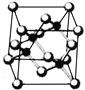
(1)下列说法正确的是__________(填序号)
A.砷化镓晶胞结构与NaCl相同 B.第一电离能 As>Ga
C.电负性 As>Ga D.原子半径 As>Ga
(2)砷化镓可由(CH3)3Ga和AsH3在700℃下反应制得,反应的方程式为_____________________________;
(3)AsH3空间形状为___________;已知(CH3)3 Ga为非极性分子,则其中镓原子的杂化方式为____________;
Ⅱ. 金属铜的导电性仅次于银,居金属中的第二位,大量用于电气工业。
(4)请解释金属铜能导电的原因_______________________, Cu2+的核外电子排布式为_______________________。
(5)在硫酸铜溶液中通入过量的氨气,小心蒸发,最终得到深蓝色的[Cu(NH3)4]SO4晶体,晶体中含有的化学键除普通共价键外,还有_________和_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH3CH2CH2CH2OH![]() CH3CH2CH2CHO;利用如图装置用正丁醇合成正丁醛相关数据如表:
CH3CH2CH2CHO;利用如图装置用正丁醇合成正丁醛相关数据如表:
物质 | 沸点/℃ | 密度 / gcm-3 | 水中溶解性 |
|
正丁醇 | 117.2 | 0.8109 | 微溶 | |
正丁醛 | 75.7 | 0.8017 | 微溶 |
下列说法中,不正确的是
A.为防止产物进一步氧化,应将酸化的Na2Cr2O7溶液逐滴加入正丁醇中
B.当温度计1示数为90~95℃,温度计2示数在76℃左右时,收集产物
C.反应结束,将馏出物倒入分液漏斗中,分去水层,粗正丁醛从分液漏斗上口倒出
D.向获得的粗正丁醛中加入少量金属钠,检验其中是否含有正丁醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种物质之间的相互转换关系如图所示。已知:A为单质,可用于制造计算机芯片,E为无色有毒气体。
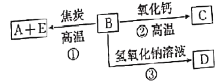
回答下列问题:
(1)B在物质分类上属于___(填“酸性氧化物”或“碱性氧化物”)。
(2)反应①的化学方程式为___。
(3)反应②的化学方程式为___。
(4)在D的溶液中通入过量CO2气体的离子方程式为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com