
【题目】某大学实验室对煤矸石(主要含Al2O3、SiO2及Fe2O3)制备聚合氯化铝{[Al2(OH)nCl6-n]m(1≤n≤5,m≤10),简称PAC,是一种新型、高效的絮凝剂和净水剂}。其工艺流程如下:

请回答下列问题:
(1)用浓盐酸配制20%的盐酸所需的玻璃仪器有______________________________。
(2)加20%的盐酸酸浸,有关反应的离子方程式为_____________________________。
(3)残渣2的主要成分是,设计实验证明你的结论(填操作、现象):_____________________。
(4)由澄清的PAC稀溶液获得聚合氯化铝固体,该实验操作是_________________,得到的PAC粗产品中可能含有的杂质离子是____________。
(5)从不引入杂质的角度来考虑,调节溶液pH的试剂可改为________(填字母)。
A.NaOH B.Al C.氨水 D.Al2O3
【答案】
(1)量筒、烧杯、玻璃棒
(2)Al2O3+6H+=2Al3++3H2O、Fe2O3+6H+=2Fe3++3H2O
(3)Fe(OH)3;取少量残渣2于小试管中,加入稀盐酸使其完全溶解,再加入KSCN溶液,溶液呈血红色
(4)蒸发浓缩,冷却结晶;Ca2+
(5)BD
【解析】
试题分析:(1)一定物质的量浓度溶液的配制中必须要使用的玻璃仪器是“量筒、烧杯、玻璃棒”,故答案为:量筒、烧杯、玻璃棒;
(2)盐酸只与煤矸石中的氧化铝和氧化铁反应,反应的化学方程式为Al2O3+6H+=2Al3++3H2O、Fe2O3+6H+=2Fe3++3H2O,故答案为:Al2O3+6H+=2Al3++3H2O、Fe2O3+6H+=2Fe3++3H2O;
(3)调节适当pH保留Al3+,就要除去Fe3+,故残渣2只能是Fe(OH)3,可以加盐酸溶解沉淀后再加硫氢化钾溶液进行检验,故答案为:Fe(OH)3;取少量残渣2于小试管中,加入稀盐酸使其完全溶解,再加入KSCN溶液,溶液呈血红色;
(4)从澄清的PAC稀溶液获得聚合氯化铝固体,可以采用蒸发浓缩,冷却结晶的方法,加入氢氧化钙调节溶液的pH过程中,引进的钙离子会混入PAC粗产品中,故答案为:蒸发浓缩,冷却结晶;Ca2+;
(5)从不引入杂质角度去考虑,加入NaOH和氨水会引入钠离子和铵根离子,故选BD。


 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:
【题目】研究发现,NOx和SO2是雾霾的主要成分。
(一)NOx主要来源于汽车尾气。
已知:N2(g)+O2(g)![]() 2NO(g)△H=+180.50kJmol-1
2NO(g)△H=+180.50kJmol-1
2CO(g)+O2(g)![]() CO2(g)△H=-566.00kJmol-1
CO2(g)△H=-566.00kJmol-1
(1)为了减轻大气污染,人们提出在汽车尾气排气管口采用催化剂将NO和CO转化成无污染气体参 与大气循环.写出该反应的热化学方程式___________________________;
(2)T℃时,将等物质的量的NO和CO充人容积为2L的密闭容器中,保持温度和体积不变,反应过程(0-15min)中NO的物质的量随时间变化如下图所示.
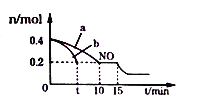
①T℃时该化学反应的平衡常数K=____________;平衡时若保持温度不变,再向容器中充入CO、N2各0.8mol,平衡将__________移动;(填“向左”、“向右”或“不”)
②图1中a、b分别表示在一定温度下,使用质量相同但表面积不同的催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是_______(填“a”或“b”)
③15min时,若改变外界反应条件,导致n(NO)发生如图所示的变化,则改变的条件可能是____________;
(二)SO2主要来源于煤的燃烧.燃煤烟气的脱硫减排是减少大气中含硫化合物污染的关健。
(3)用纯碱溶液吸收SO2可将其转化为HSO3-,该反应的离子方程式是________________;
(4)如图所示的电解装罝可将雾霾中的NO、SO2分别转化为NH4+和SO42-。
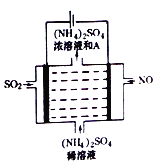
①写出物质A的化学式_________,阳极的电极反应式是________________;
②该电解反应的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年10月5日,从瑞典斯德哥尔摩传来令人振奋的消息:中国女科学家屠呦呦获得2015年诺贝尔生理学或医学奖。理由是她发现了青蒿素,这种药品可以有效降低疟疾患者的死亡率。青蒿素的一种化学合成部分工艺流程如下:

已知:羰基![]() H可发生反应应
H可发生反应应![]()
回答下列问题:
(1)青蒿素的含氧官能团名称: 和过氧基;
(2)写出A发生加聚反应的化学方程式 ;
(3)反应B→C,实际上可看作两步进行,依次发生的反应类型是 ;
(4)写出由苯甲醛和氯乙烷为原料,制备苄基乙醛(![]() CH2CH2CHO)的合成路线流程图;无机试剂任用,合成路线流程图示例如下:CH3CH2OH
CH2CH2CHO)的合成路线流程图;无机试剂任用,合成路线流程图示例如下:CH3CH2OH![]() H2C=CH2
H2C=CH2![]() H2C Br-CH2 Br
H2C Br-CH2 Br
。
(5)写出E发生水解反应的化学方程式 。
(6)写出HC(OCH3)3只属于醇的同分异构体的结构简式(同一个碳原子上不能同时连接两个羟基) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强。25℃时氯气-氯水体系中存在以下平衡关系:
Cl2(g) ![]() Cl2(aq) K1=10-1.2
Cl2(aq) K1=10-1.2
Cl2(aq)+ H2O ![]() HClO + H+ +Cl- K2=10-3.4
HClO + H+ +Cl- K2=10-3.4
HClO ![]() H+ + ClO- Ka=?
H+ + ClO- Ka=?
其中,Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。下列表述正确的是

A.氯处理饮用水时,在夏季的杀菌效果比在冬季好
B.用氯处理饮用水时,pH=7.5时杀菌效果比pH=6.5时好
C.在氯处理水体系中,c(HClO) +c(ClO-) =c(H+)-c(OH-)
D.Cl2(g)+ H2O ![]() 2H+ + ClO- + Cl- ,K=10-12.1
2H+ + ClO- + Cl- ,K=10-12.1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组采用类似制乙酸乙酯的装置(如下图),以环己醇制备环己烯,
已知:
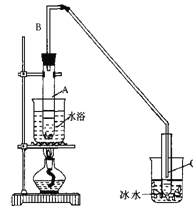
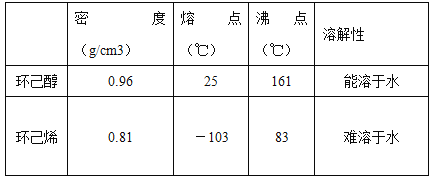
(1)制备粗品:将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是_______,导管B除了导气外还具有的作用是_________。
②试管C置于冰水浴中的目的是_______________________________________
(2)制备精品
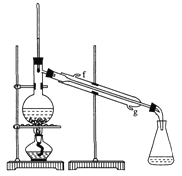
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_______层(填“上”或“下” ),分液后用______(填入编号)洗涤。
A.KMnO4溶液 B.稀H2SO4 C.Na2CO3溶液
②再将环己烯按右图装置蒸馏,冷却水从_______口进入。蒸馏时要加入生石灰,目的是________________________。
③收集产品时,控制的温度应在_________℃左右。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修2:化学生活与技术]
分析下列水处理方法,完成下列问题:
(1)处理含Cr2O72-工业废水的工艺:
①工艺一:含Cr2O72-的工业废水![]() Cr3+、SO42-
Cr3+、SO42-![]() 。
。
为了进一步除去上述流程中生成的Cr3+,请你设计一个处理方案:________________。
②工艺二:向废水中加入过量的FeSO4溶液,经过一系列反应后,FeSO4溶液和Cr2O72-可形成铁氧体沉淀,从而除去铬元素。若使含1mol Cr2O72-的废水中的Cr2O72-完全转化为一种化学式为Cr0.5Fe2.5O4的铁氧体(其中的铬元素为+3价),理论上需要绿矾(FeSO4·7H2O)的质量不少于
g,上述得到的铁氧体中,Fe3+和Fe2+的个数之比 。
(2)如下是处理含氰(主要以CN—形式存在)废水工艺流程的一部分:
含氰废水![]() 。发生上述转化后CN—中碳元素转化为+4价,氮元素转化为0价,氯元素转化为-1价,若废水中CN—的浓度为300mg/L,含氰废水的流量为0.8m3/h,为保证安全,实际投放的ClO2为理论值得1.3倍,则为了完成上述过程每小时实际应该投入的ClO2的质量为__________kg(结果保留两位有效数字)。
。发生上述转化后CN—中碳元素转化为+4价,氮元素转化为0价,氯元素转化为-1价,若废水中CN—的浓度为300mg/L,含氰废水的流量为0.8m3/h,为保证安全,实际投放的ClO2为理论值得1.3倍,则为了完成上述过程每小时实际应该投入的ClO2的质量为__________kg(结果保留两位有效数字)。
(3)监测水中氯化物含量可采用硝酸汞滴定法,酸化的水样用硝酸汞滴定时可生成难电离的氯化汞,滴定到终点时过量的汞离子可与指示剂作用使溶液显示紫色。饮用水中的其他物质在通常浓度下对滴定不产生干扰,但水的色质、高价铁、六价铬、硫化物(如S2-)对实验有干扰。
①滴定前常用氢氧化铝悬浊液处理水样,其目的是__________________。
②若水中含有Cr2O72—,常在滴定前向水样中加入一定量的对苯二酚,其目的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用下图装置制备家用消毒液,并探究其性质。

(1)写出装有浓盐酸的仪器名称 ,A中烧瓶内进行的反应中浓盐酸体现出的化学性质是 。
(2)写出装置B中发生的所有反应化学方程式 。
(3)装置c的作用是 。反应停止后,各取洗气瓶中无色溶液5mL分别进行了如下实验:
操作 | 现象 |
A.测溶液pH, 并向其中滴加2滴酚酞 | pH = 13, 溶液变红,5min后褪色 |
B. 向其中逐滴加入盐酸 | 溶液逐渐变成黄绿色 |
(4)查阅资料:酚酞的变色范围为8.2~10,且酚酞在强碱性溶液中红色会褪去,为探究操作A中溶液褪色的原因,又补充了如下实验:
操作 | 现象 |
取 NaOH溶液,向其中滴加2滴酚酞 | 溶液变红,30min后褪色 |
获得结论:此实验小组制备的消毒液具有漂白性。
(5)操作B中溶液变成黄绿色的原因: (用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常见金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,
它们之间存在如下转化关系(图中有些反应的产物和反应的条件没有全部标出)。其中B是地壳中含量居第一的金属元素,C是当今产量和用量最多的金属。请回答下列问题:
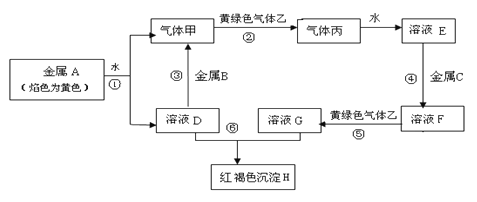
(1)写出金属B和气体丙的化学式 、 。
(2)写出反应①的化学反应方程式 。
(3)沉淀H的化学式为 。
(4)往溶液G中滴入KSCN溶液,现象是——————————————————
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是前四周期原子序数依次增大的五种元素。A元素原子的核外电子数等于其电子层数,B元素基态原子有三个能级且各能级电子数相同,A与D可形成两种常见液态化合物G、H,其原子数之比分别为1:1和2:1。E元素原子的K、L层电子数之和等于其M、N层电子数之和。请回答下列各题(涉及元素请用相应化学符号表示):
(1)BCD三种元素中电负性最大的元素其基态原子的电子排布图为____________;
(2)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用____________形象化描述。在B的基态原子中,核外存在____________对自旋相反的电子。
(3)由E和D形成的晶胞如图1所示,晶体中E2+周围等距且最近的E2+有______个;ED的焰色反应为砖红色,许多金属或它们的化合物都可以发生焰色所对应,其原因是____________;E和B可形成的晶体的晶胞结构与NaCl晶体的相似(如图2所示),但该晶体中含有的哑铃形B22-的存在,使晶胞沿一个方向拉长。晶体中E2+的配位数为_______。该化合物的电子式为_______。

(4)用高能射线照射液态H时,一个H分子能释放出一个电子,同时产生一种阳离子。①释放出来的电子可以被若干H分子形成的“网”捕获,你认为H分子间能形成“网”的原因____________;
②由H分子释放出电子时产生的一种阳离子具有较强的氧化性,请写出该阳离子与SO2的水溶液所对 应的离子方程式________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com