
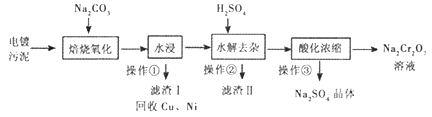
【题目】工业上“中温焙烧——钠化氧化法”回收电镀污泥中的铬已获技术上的突破。其工艺流程如下:
【查阅资料】
①电镀污泥中含有Cr(OH)3、Al203、ZnO、CuO、NiO等物质;水浸后溶液中含有Na2CrO4、NaAlO2、Na2ZnO2等物质;
②Na2CrO4转化成Na2Cr2O7离子反应方程式为:2 CrO42-+2H+=Cr2O72-+H2O;③Na2SO4、Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表:

请回答:
(1)操作①的名称是_______,“水浸”后的溶液呈_______性;
(2)“焙烧氧化”过程中Cr(OH)3转化成Na2CrO4的化学方程式为___________;
(3)滤渣II的主要成分有Zn(OH)2和X,生成X的离子反应方程式__________;
(4)“酸化浓缩”时,需继续加入H2SO4,然后_______、结晶、过滤。继续加入H2SO4目的是__________;
(5)以铬酸钠为原料,电化学法制备重铬酸钠的实验装置如图所示。
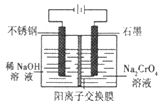
①阴极发生的电极反应式为:_____________;
②若测定阳极液中Na与Cr的物质的量之比值为d,则此时铬酸钠的转化率为___________。
【答案】过滤碱4Cr(OH)3+ 4 Na2CO3+ 3O2![]() 4Na2CrO4+4CO2+6H2OAlO2–+H++ H2O
4Na2CrO4+4CO2+6H2OAlO2–+H++ H2O![]() Al(OH)3↓蒸发浓缩促使反应2CrO42-+2H+
Al(OH)3↓蒸发浓缩促使反应2CrO42-+2H+![]() Cr2O72-+H2O平衡向正方向移动2H2O+2e-=2OH-+H2↑(或2H++2e-=H2↑)2-d
Cr2O72-+H2O平衡向正方向移动2H2O+2e-=2OH-+H2↑(或2H++2e-=H2↑)2-d
【解析】分析:(1)本题主要考查物质分离的方法,从盐类水解的规律角度解答;
(2)根据氧化还原反应的规律,氧化焙烧过程中铬元素化合价升高,所以一定有氧气参加反应,结合质量守恒定律完成方程式;
(3)根据流程图,水浸后溶液中存在Na2CrO4、NaAlO2、Na2ZnO2等物质,加入硫酸调节溶液的pH可得到硫酸钠和Na2Cr2O7溶液,所以还应该生成Zn(OH)2、Al(OH)3沉淀;
(4)根据已知条件,加入硫酸发生CrO42-+2H+Cr2O72-+H2O,从平衡移动的角度分析;
(5)根据电解原理,阴极得电子发生还原反应。
解答:(1)操作①是从溶液中分离出滤渣,属于固液分离,操作①是的名称是过滤;水浸后溶液中存在Na2CrO4、NaAlO2、Na2ZnO2等都为强碱弱酸盐,水解后呈碱性;
(2)氧化焙烧过程中有氧气参加反应,根据质量守恒可知还应生成水,反应的方程式为4Cr(OH)3+ 4 Na2CO3+ 3O2![]() 4Na2CrO4+4CO2+6H2O
4Na2CrO4+4CO2+6H2O
(3)Zn(OH)2、Al(OH)3具有两性,水浸后溶液中存在Na2CrO4、NaAlO2、Na2ZnO2等物质,加入硫酸调节溶液的pH可得到Zn(OH)2、Al(OH)3沉淀,NaAlO2加入酸生成Al(OH)3沉淀的离子方程式为AlO2–+H++ H2O![]() Al(OH)3↓;(4)水浸后溶液中存在Na2CrO4,加入硫酸发生CrO42-+2H+Cr2O72-+H2O,加入硫酸可使平衡向正反应方向移动,将溶液蒸发浓缩、冷却结晶可得到晶体,(5)以铬酸钠为原料,电化学法制备重铬酸钠,阴极发生还原反应,电极反应为2H2O+2e-=2OH-+H2↑,
Al(OH)3↓;(4)水浸后溶液中存在Na2CrO4,加入硫酸发生CrO42-+2H+Cr2O72-+H2O,加入硫酸可使平衡向正反应方向移动,将溶液蒸发浓缩、冷却结晶可得到晶体,(5)以铬酸钠为原料,电化学法制备重铬酸钠,阴极发生还原反应,电极反应为2H2O+2e-=2OH-+H2↑,
根据铬元素守恒,设开始Na2CrO4的物质的量为a mol,生成Na2Cr2O7的物质的量为x mol
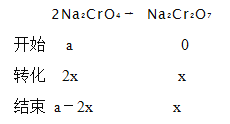
反应结束钠元素的物质的量为2(a-2x)+2x,铬元素的物质的量为(a-2x)+2x,则![]() = d;x=
= d;x=![]() ,所以铬酸钠的转化率为
,所以铬酸钠的转化率为![]() = 2-d。
= 2-d。


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:
【题目】下列各组物质中所含原子数相同的是
A.2 L CO和2 L O2
B.同温同压下,2LO2和N2与NO的混合气体2L
C.0.2 mol H2和4.48 L HCl
D.标准状况下2 mol CO2和44.8 L水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表,思考扇形元素周期表的填充规律,并回答下列问题:

(1)L元素在常见周期表中所处的位置是________,其单质与A2E反应的化学方程式为____________。
(2)元素F、G、J、K、M对应简单离子的离子半径由大到小的顺序是(用离子符号表示)___________。
(3)用电子式表示MO2的形成过程:_______________。
(4)B、F、G三种元素最高价氧化物对应的水化物碱性最强的是__________(填化学式)。比较元素C和J的非金属性强弱:C______J(填“强于”或“弱于”)。
(5)向元素B和N形成的化合物的水溶液中,加入元素K的单质,所发生的反应的离子方程式为_____;反应后,向溶液中加入C、K形成的化合物,现象为___________。
(6)均由A、B、E、J四种元素组成的两种化合物可相互反应,写出反应的化学方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究生活中两种常见的有机物的性质,某同学设计如下实验,请根据题目要求填写下列空格:
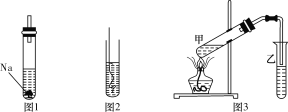
(1)如上图1所示,试管中装乙醇产生的气体为__________(填名称);
(2)如上图2所示,把加热的铜丝插入到装有乙醇的试管中,闻到有刺激性气味,该反应中产生的有机物为___________(填名称);
(3)用食醋浸泡有水垢(主要成分CaCO3)的水壶,可以清除水垢,说明醋酸的酸性___________碳酸的酸性(填“强于”或“弱于”);
(4)按如图3所示装置,甲试管中装有乙酸、乙醇、浓硫酸,则在装有饱和碳酸钠溶液的乙试管上方可闻到有特殊香味的物质,该物质为_____________(填名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,A、B、C、D、E是元素周期表中的5种主族元素。下列说法不正确的是( )

A. A、E原子序数之差可能为2
B. D、E原子序数之差可能是8、18或32
C. B、C原子序数之差一定是2
D. B、D原子序数之差不可能是7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液 A中可能含有如下离子:Na+、NH4+、Ba2+、Mg2+、SO42-、SO32-、Cl-、OH-。某同学设计并完成了如下的实验:

下列说法正确的是
A. 溶液 A 中一定存在 NH4+、 SO42-、 SO32-,可能存在 Na+
B. 溶液 A 中一定存在 NH4+、 Mg2+、 SO42-、 SO32-,可能存在 Cl-
C. 溶液 A 中可能存在 Cl-,且 c(Na+) ≥ 0.20 mol·L-1
D. 如果气体 F 能使湿润的蓝色石蕊试纸变红,说明溶液中一定含有 NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对乙酰氨基酚,俗称扑热息痛(Paracetamol),具有很强的解热镇痛作用,工业上通过下列方法合成(图中B1和B2、C1和C2分别互为同分异构体,无机产物略去):
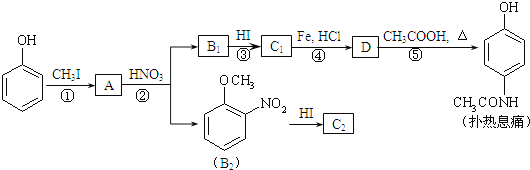
已知:![]() ,请按要求填空:
,请按要求填空:
⑴写出A分子中官能团名称:_________;C1的结构简式为:________________。
⑵写出由D生成扑热息痛的化学方程式:_______________________。
⑶写出反应③和④的反应类型:③______________,④__________。
⑷工业上设计反应①、②、③,而不是只通过反应②得到C1、C2,其目的是:______________________。
⑸扑热息痛有很多同分异构体,符合下列要求的同分异构体有5种:(I)是对位二取代苯;(II)苯环上两个取代基一个含氮不含碳、另一个含碳不含氮;(III)两个氧原子与同一原子相连。其中2种的结构简式是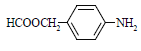 和
和![]() ,写出另3种同分异构体的结构简式____________、____________、____________。
,写出另3种同分异构体的结构简式____________、____________、____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com