
����Ŀ����1��SO2�Ĵ����������Ṥҵ����Ҫ��Ӧ֮һ�����б�״̬��22.4LSO2���壬��500�桢V2O5����ת��ΪSO3����SO2��ת����Ϊ50%���ų�����ΪQKJ,��÷�Ӧ���Ȼ�ѧ����ʽΪ____________.
��2����֪��SO2������ǰ���������и��ɷֵ����������ͼ����SO2��ת����Ϊ_______________��

��3�����¡���ѹ�£���һ���ݻ��ɱ���ܱ������з�����A��g��+ 2B��g��![]() C��g������ʼ����3molA��5molB����ϵ���ΪV����ƽ��ʱ������amolC��ͬ�������£�Ҫʹƽ��ʱ����CΪ3.5amol����ʼʱ������5.5molB�������___________molA��_________molC��
C��g������ʼ����3molA��5molB����ϵ���ΪV����ƽ��ʱ������amolC��ͬ�������£�Ҫʹƽ��ʱ����CΪ3.5amol����ʼʱ������5.5molB�������___________molA��_________molC��
���𰸡� 500 �� ��2SO2(g)+O2(g)![]() 2SO3(g) ��H=-4Q kJ��mol-1 95.3% 4.5 6
2SO3(g) ��H=-4Q kJ��mol-1 95.3% 4.5 6
��������(1). ���б�״̬��22.4LSO2���壬SO2��ת����Ϊ50%���ų�����ΪQkJ��2molSO2�ų�4QKJ��500 �� ��2SO2(g)+O2(g)![]() 2SO3(g) ��H=-4Q kJ��mol-1 ��
2SO3(g) ��H=-4Q kJ��mol-1 ��
��2���跴Ӧǰ�����Ϊ100L����Ӧ�����Ϊ82L/84.8%=96.7L��SO3��ת����SO2Ϊ96.7��6.9%=6.67L��SO2��ת����6.67/7��100%=95.3%��
��3��Ҫʹƽ��ʱ����CΪ3.5amol����Ͷ��A�൱��3mol��3.5=10.5mol��BΪ5mol��3.5=17.5mol��ֻ����5.5molB����17.5mol�D5.5mol=12mol��12molB��Ҫ����6molC���ټ���AΪ10.5mol-6mol=4.5mol��


 ��Ӣ���㿨ϵ�д�
��Ӣ���㿨ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��pOHֵָ������Һ�ļ�ȣ�����Һ��OH-Ũ������ʾ����pH����ʾ����Һ������Ӧ��pOH����OH-��Ũ�ȵĸ����ö�������ͼ�ֱ��ʾ������25���100����ˮ�ĵ���ƽ�����ߡ�����˵������ȷ����

A. ����B��ʾ����25��Cʱˮ�ĵ���ƽ������
B. 25��Cʱ����pH=1��ϡ��������ε���pH=11��ϡ��ˮ����������Ӧ������ˮ�ĵ����ȴٽ�������
C. Q���Ӧ����Һ�У���ͬʱ��������K+��Fe3+��NO3-��SO42-
D. 100��Cʱ����pH = 2��������pH=12������������Һ�������ϣ���Һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������H2��ԭWO3�Ʊ�����W��װ����ͼ��ʾ��Zn������������������ʣ�����ûʳ������Һ������������������������˵����ȷ����

A. �١��ڡ���������ʢװKMnO4��Һ��ŨH2SO4������ûʳ������Һ
B. ��ʽ¯����ǰ�����Թ��ڢܴ��ռ����岢��ȼ��ͨ�������ж����崿��
C. ������Ӧʱ���ȹرջ���K����ֹͣ����
D. װ��Q�����շ�������Ҳ�����ڶ���������Ũ���ᷴӦ�Ʊ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ�д��ڶ��ַ��Ӻ����ӣ������ڲ�ͬ�ķ�Ӧ�б��ָ��Ե����ʣ�����ʵ������ͽ���һ������ȷ����
A. ������ɫ������һ�����ɫ������ɫ��˵����Һ����Cl2����
B. ��Һ�ʻ���ɫ�����д̼�����ζ��˵����HClO���Ӵ���
C. ����AgNO3��Һ������ɫ������˵����Cl-���Ӵ���
D. ����NaOH��Һ����ˮ����ɫ��ʧ��˵����HClO���Ӵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ɽ���Na��Cu��C��N��B��Ԫ����ɵ������������ҵ�����Ź㷺��;��
(1)��̬Cu+����Χ���ӹ��ʽΪ_______��
(2)H3BNH3�Ǵ�����ϣ����Ʊ�ԭ��Ϊ��3CH4+2(HB=NH)3+6H2O��3CO2+6H3BNH3������(HB=NH)3��һ����Ԫ��״�����������H3BNH3��Bԭ�ӵ��ӻ���ʽΪ_______��1��(HB=NH)3�����к��� ___���Ҽ���
(3) B��C��N��Oԭ�ӵĵ�һ�������ɴ�С��˳��Ϊ_____________________��
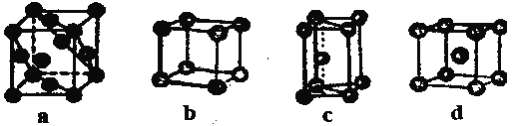
(4)������������ֶѻ�����ͼ�������Ƶľ���ѻ�ģ��Ϊ____(����ĸ)��
(5)��֪NaCl��Ħ������ΪMg��mol-1���ܶ�Ϊpg���M-3�������ӵ�����ΪNA mol-1����NaCl�����У��������������Cl-���ļ�ľ���Ϊ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����գ�
��1����������ʮ�����ʣ������Ǣ�����NaCl��ʯī��ͭ˿��INaOH�����SO2��NaHSO4�����K2O�����Һ̬H2SO4��Һ�� ���������пɵ������________������ţ���ͬ�������������в��ܵ��磬�����ڵ���ʵ���_______________________��
��2��NaHSO4��һ����ʽ�Σ�����д���пհף�
��NaHSO4�����ۻ�ʱ�ĵ��뷽��ʽΪ______________________________��
����0.1 mol��L-1��NaHSO4��Һ�ĵ���������ͬ��������Һ�����ʵ���Ũ��Ϊ��_______________��
��NaHSO4��Һ��NaHCO3��Һ��Ӧ�����ӷ���ʽΪ______________________________��
��3 mol��L-1 NaHSO4��2 mol��L-1 Ba(OH)2��Һ�������ϣ��÷�Ӧ�ܵ����ӷ���ʽΪ________________________________________��
��3��������SO2��SO3�ķ�����֮��Ϊ_____��ͬ��ͬѹ�µ��ܶ�֮��Ϊ_____������ԭ����֮��Ϊ____��
��4��ijǿ���Է�Ӧ��ϵ�У���Ӧ��������ﹲ�������ʣ�O2��MnO4-��H2O��Mn2+��H2O2��H+����֪�÷�Ӧ��H2O2ֻ���������¹��̣�H2O2��O2��д���÷�Ӧ�����ӷ���ʽ��_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±��������ʾ��������ȫ����ȷ��һ���ǣ� ��
ԭ�Ӿ��� | ���Ӿ��� | ���Ӿ��� | |
A | ʯī | ���� | ������ |
B | ������ | �� | ���� |
C | ���ʯ | ���� | �� |
D | �� | �������� | ������ |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С��ģ���������е�ԭ�������������볱ʪ������̼��Ӧ�����������ͼ��ʾ����������ȡ���������������������ͼ��EΪ����װ�á�

��ʵ��ɹ�ѡ�õ�ҩƷ���У�ϡ���ᡢϡ���ᡢ�������ơ�����ʯ��ˮ��
��֪��2 Na2O2+2H2O=4NaOH+O2�� 2Na2O2+2CO2=2Na2CO3+O2 �Իش�
��1��ͼ��װ�õ�����˳���ǣ���װ�õ���ĸ��ţ����������ӽ��ܼ�֧��װ�þ�ʡ�ԣ�_________��
��2��װ��C�з���ķ�Ӧ����________��_________________����д��ѧʽ��
��3��װ��A��������__________________��װ��B��������_____________________________��
��4��Ϊ�˽�ȷ�ز�����������������˱���������װ�õ�������֮�⣬�ڶ���Ӧǰ�����Һ��Ķ��������ֵ�Ĺ����У�Ӧע��_____________________________��
a.�����밼Һ����ʹ���ƽ
b.�ȴ�Ƭ�̣����ҹ���Һ�治������ʱ�����̶�����
c.����ʱӦ�����ƶ��ҹܣ�ʹ�ס�������Һ����ƽ��
d.����ʱ��һ��ʹ�ס�������Һ����ƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ����( )
A. ������ΪNA��CO��C2H4�����������ԼΪ22.4 L
B. ��״���£�4.48 L��ˮ(D2O)�к��е�������Ϊ2NA
C. ��MnO2��Ũ������ȡCl2ʱ��ÿ����0.5mol Cl2��ת�Ƶ�����ΪNA
D. 0.1 L 3.0 mol��L-1��NH4NO3��Һ�к���NH![]() ����ĿΪ0.3NA
����ĿΪ0.3NA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com