
A、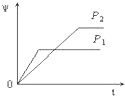 |
B、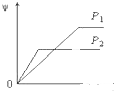 |
C、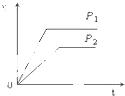 |
D、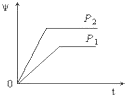 |


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
 已知Ⅰ.N-N键键能为167kJ?mol-1,N≡N键键能为942kJ?mol-1,
已知Ⅰ.N-N键键能为167kJ?mol-1,N≡N键键能为942kJ?mol-1,| A、+1066.4 kJ?mol-1 |
| B、-1066.4 kJ?mol-1 |
| C、+697.6 kJ?mol-1 |
| D、-697.6 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | K1=1.77×10-4 | K1=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| A、中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者 |
| B、相同温度时,等浓度的HCOONa和NaCN溶液的pH前者小于后者 |
| C、2CN-+H2O+CO2=2HCN+CO32- |
| D、2HCOOH+CO32-=2HCOO-+H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N2 (g)+CO2 (g).某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N2 (g)+CO2 (g).某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:浓度/mol?L-1 时间/min | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加催化剂同时升高温度 |
| B、降低温度同时增大压强 |
| C、增大压强同时充入CO |
| D、加催化剂同时增大压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氮氧化铝中氮的化合价是-3 |
| B、反应中每生成5.7g AlON 同时生成1.12 L CO |
| C、反应中氧化产物和还原产物的物质的量之比是2:1 |
| D、反应中氮气作氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、①②③ | B、②④ |
| C、④⑤⑥ | D、③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,将6.72L的NO2通入足量的水中转移电子数为0.3NA |
| B、22.4L二氧化硫分子中电子总数约为32NA |
| C、1mol Na与足量O2反应生成Na2O或Na2O2均失去NA个电子 |
| D、各5.6g铁分别与足量的盐酸、氯气反应,电子转移总数均为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com