
【题目】某化学小组选用酸性高锰酸钾溶液和草酸溶液,探究外界条件对化学反应速率的影响,进行了如下了三组实验:[实验内容及记录]
实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
mol/L H2C2O4溶液 | H2O | 0.05mol/L KMnO4溶液 | 3 mol/L稀硫酸 | ||
1 | 3.0 | 1.0 | 4.0 | 2.0 | 4.0 |
2 | 2.0 | 2.0 | 4.0 | 2.0 | 5.2 |
3 | 1.0 | 3.0 | 4.0 | 2.0 | 6.4 |
请回答:
(1)[实验原理] _________________________________________(写离子方程式)
(2)为完成实验目的,H2C2O4溶液的物质的量浓度不低于__________________
(3)根据上表中的实验数据,可以得到的结论是_______________________________
(4)利用实验1中数据计算,用KMnO4的浓度变化表示的反应速率为:v(KMnO4)=______ 。
(5)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示,但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设。并继续进行实验探究。

①该小组同学提出的假设是_________________________________________。
②请你帮助该小组同学完成实验方案,并填写表中空白。
实验 编号 | 室温下,试管中所加试剂及其用量/mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间/min | |||||
_____mol/L H2C2O4溶液 | H2O | 0.05mol/L KMnO4溶液 | 3 mol/L稀硫酸 | |||||
4 | 3.0 | 1.0 | 4.0 | 2.0 | t | |||
③若该小组同学提出的假设成立,应观察到的现象是__________________________________
【答案】 2MnO4-+5H2C2O4+6H+=== 2Mn2++10CO2↑+8H2O 0.5mol/L 其他条件相同时,增大H2C2O4浓度(或反应物浓度),反应速率增大 0.005mol / (L·min) 生成物中的MnSO4为该反应的催化剂(或Mn2+对该反应有催化作用) MnSO4 与实验1比较,溶液褪色所需时间短或所用时间(t)小于4.0min
【解析】(1)本题的实验原理是酸性高锰酸钾氧化草酸,酸性高锰酸钾褪色生成二价锰离子,草酸中的C被氧化为二氧化碳,化学方程式为:2KMNO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O,故答案为:2KMNO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O;
(2)高锰酸钾的物质的量为:0.05molL-1×0.004L=0.0002mol,根据方程式2KMNO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O,H2C2O4的物质的量至少为0.0002mol×![]() =0.0005mol,在实验③中要保证高锰酸钾完全反应,物质的量浓度至少为
=0.0005mol,在实验③中要保证高锰酸钾完全反应,物质的量浓度至少为![]() =0.5mol/L,故答案为:0.5mol/L;
=0.5mol/L,故答案为:0.5mol/L;
(3)从表中数据可知改变的条件是H2C2O4溶液的浓度;其他条件相同时,增大H2C2O4溶液的浓度,反应速率增大,故答案为:其他条件相同时,增大H2C2O4溶液的浓度,反应速率增大;
(4)实验1中,高锰酸钾的物质的量为:0.05molL-1×0.004L=0.0002mol,混合后高锰酸钾的物质的量浓度为![]() =0.02mol/L,因此v(KMnO4)=
=0.02mol/L,因此v(KMnO4)=![]() =0.005mol / (L·min) ,故答案为:0.005mol/(Lmin);
=0.005mol / (L·min) ,故答案为:0.005mol/(Lmin);
(5)①由图乙可知反应开始后速率增大的比较快,说明生成物中的MnSO4(或Mn2+)为该反应的催化剂,故答案为:生成物中的MnSO4为该反应的催化剂(或Mn2+对该反应有催化作用);
②与实验1作对比实验,则加入的硫酸锰的量不同,其它条件必须相同,所以加入的少量固体为MnSO4,故答案为:MnSO4;
③若该小组同学提出的假设成立,则反应速率加快,溶液褪色的时间小于4min,从而说明Mn2+是催化剂,故答案为:与实验1比较,溶液褪色所需时间短(或所用时间(t)小于4min)。


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
【题目】有关碱金属元素,下列说法正确的是( )
A. 单质沸点随原子序数的递增而升高
B. 周期表第一列是第IA族元素,又称碱金属元素
C. 金属锂在空气中燃烧,产物是Li2O2
D. 金属锂常用于制造锂电池,这跟它还原性强、密度小有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y、Z原子序数之和是W的2倍,X、Z在周期表中的相对位置如图所示,X的最低负价绝对值与其原子最外层电子数相等。下列说法不正确的是

A. 原子半径:Y>Z>W B. 一定条件下,Y可置换出X
C. 气态氢化物稳定性:Z>W D. 熔点YW2>XW4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将6 mol CO2和8 mol H2充入2L恒容密闭容器中,发生反应:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表。
CH3OH(g)+H2O(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表。

(1)反应前4min的平均速率v(CO2)= ________________ mol/(L·min)
(2)达到平衡时速率之比v(CO2):v(H2):v(CH3OH):v(H2O)=_________
(3)达到平衡时,H2的转化率为____________ ;CO2平衡浓度是_____mol/L
(4)该温度下,该反应的平衡常数为_____________
(5)达到平衡时降低温度,平衡向_______________(填正反应或逆反应)方向移动;达到平衡时速率与原平衡速率比较(填变大,不变或减小)_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气和水,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是__________________。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时:负极的电极反应式是_______________________________________ 。
(3)用CO做燃料电池电解CuSO4溶液、FeCl3和FeCl2混合液的示意图如图1所示,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A、B两极上产生的气体体积相同.
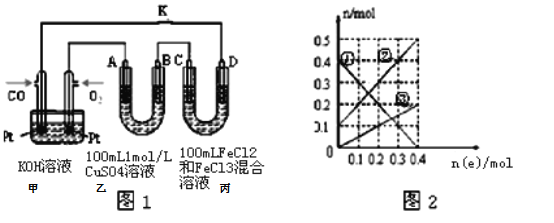
①写出通入CO的电极反应式____________________________________
②乙中B极产生的气体在标准状况下的体积为_____________.
③丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图2所示,则图中③线表示的是____________(填离子符号)的变化;反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要_____________mL 8.0mol·L﹣1 NaOH溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在标况下的四种气体①6.72LCH4 ②3.01×1023个HCl分子 ③13.6克H2S④0.2molNH3用相应的序号填写下列空白:
(1)体积最大的是;
(2)原子数最多的是;
(3)质量最小的是;
(4)含氢原子数最少的是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2013年9月以来,我国很多地区再大面积出现雾霾,特别是华中华北尤其严重,汽车尾气、燃煤废气和冬季取暖排放的CO2等都是形成雾霾的原因。
Ⅰ.用于净化汽车尾气的反应为:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)△H<0,在一定温度下,如图在一体积固定的密闭容器中充入一定量的NO和CO,在t1时刻达到平衡状态。
2CO2(g)+N2(g)△H<0,在一定温度下,如图在一体积固定的密闭容器中充入一定量的NO和CO,在t1时刻达到平衡状态。
(1)能判断该反应达到平衡状态的标志是_______。
A.在单位时间内生成1mol CO2的同时消耗了1mol CO
B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变
D.混合气体的压强不再变化
(2)在t2时刻将容器的容积迅速扩大到原来的2倍,在其他条件不变的情况下,t3时刻达到新的平衡状态,之后不再改变条件.请在图中补充画出从t2到t4时刻正反应速率随时间的变化曲线:___________

Ⅱ.使用石油热裂解的副产物CH4来制取H2,其生产流程如图1所示:
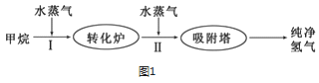
(3)此流程的第Ⅰ步反应为:CH4(g)+H2O(g)![]() CO(g)+3H2(g),一定条件下CH4的平均转化率与温度、压强的关系如图2所示,则P1_____P2(填“>”、“<”或“=”),100℃时,将1molCH4(g)和2molH2O(g)通入容积为100L的恒容的密闭容器中,达到平衡时CH4的转化率为0.5。此时该反应的平衡常数K____________ (写出完整的计算过程)
CO(g)+3H2(g),一定条件下CH4的平均转化率与温度、压强的关系如图2所示,则P1_____P2(填“>”、“<”或“=”),100℃时,将1molCH4(g)和2molH2O(g)通入容积为100L的恒容的密闭容器中,达到平衡时CH4的转化率为0.5。此时该反应的平衡常数K____________ (写出完整的计算过程)

(4)此流程的第Ⅱ步反应的平衡常数随温度的变化情况如下表
温度/℃ | 400 | 500 | 830 |
平衡常数K | 10 | 9 | 1 |
温度/℃ | 400 | 500 | 830 |
平衡常数K | 10 | 9 | 1 |
从表上可以推断该反应是___________(填“吸热”或“放热”)反应,若反应在500℃时进行,设CO(g)和H2O(g)的起始浓度均为0.020mol/L,在该条件下,反应达到平衡时,CO的转化率为________;
(5)图3表反应Ⅱ在t1时达到平衡,在t2时因改变某个条件引起浓度变化的情况,图中t2时改变的条件是降低温度或________________(写一种)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。实验室用足量NaOH溶液吸收从浓盐酸和MnO2反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、NaClO3、NaCl中的两种或三种。下列说法正确的是
MnCl2+Cl2↑+2H2O。实验室用足量NaOH溶液吸收从浓盐酸和MnO2反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、NaClO3、NaCl中的两种或三种。下列说法正确的是
A. 若产物为NaClO、NaCl,则吸收后的溶液中n(ClO-)=n(Cl-)
B. 若产物为NaClO3、NaCl,则参加反应的氧化剂和还原剂的物质的量之比为1∶5
C. 若产物为NaClO、NaClO3、NaCl,则由吸收后的溶液中n(Cl-)和n(ClO-)可计算吸收的n(Cl2)
D. 若产物为NaClO、NaClO3、NaCl,则NaOH与Cl2相互反应的物质的量之比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是( )
A. 乙烯能使酸性KMnO4溶液和溴水褪色,二者反应原理相同
B. 交警用酸性重铬酸钾溶液检查司机是否饮酒过量时乙醇发生取代反应
C. 乙酸的分子式为C2H4O2,属于弱酸
D. 苯分子中没有碳碳双键,因此苯不能发生加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com