
【题目】某有机物A的结构简式如下:  .下列叙述正确的是( )
.下列叙述正确的是( )
A.有机物A属于芳香烃
B.有机物A可以和Br2的CCl4溶液发生加成反应
C.有机物A和浓硫酸混合加热170℃时,可以发生消去反应
D.1mol A和足量的NaOH溶液反应,可以消耗2mol NaOH
【答案】D
【解析】解:A.该物质中除了含有C、H元素外还含有O元素,所以不属于芳香烃,故A错误; B.该分子中不含碳碳不饱和键,所以不能和溴发生加成反应,故B错误;
C.连接醇羟基碳原子的相邻碳原子上 不含氢原子,所以醇羟基不能发生消去反应,故C错误;
D.氯原子水解生成的HCl能和NaOH反应,且含有酚羟基,所以1 mo1A 与足量的NaOH 溶液反应,最多可以消耗2mol NaOH,故D正确;
故选D.
【考点精析】认真审题,首先需要了解有机物的结构和性质(有机物的性质特点:难溶于水,易溶于汽油、酒精、苯等有机溶剂;多为非电解质,不易导电;多数熔沸点较低;多数易燃烧,易分解).


科目:高中化学 来源: 题型:
【题目】(15分)化合物H是一种用于合成γ﹣分泌调节剂的药物中间体,其合成路线流程图如下: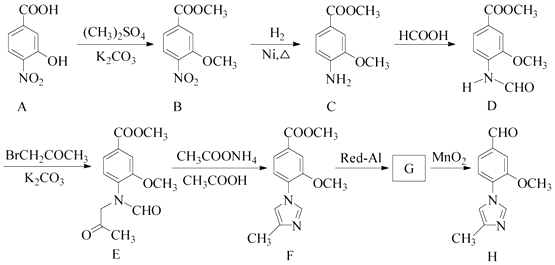
(1)C中的含氧官能团名称为和 .
(2)D→E 的反应类型为 .
(3)写出同时满足下列条件的C的一种同分异构体的结构简式: .
①含有苯环,且分子中有一个手性碳原子;②能发生水解反应,水解产物之一是α﹣氨基酸,另一水解产物分子中只有2种不同化学环境的氢.
(4)G 的分子式为C12H14N2O2 , 经氧化得到H,写出G的结构简式: .
(5)已知: 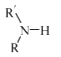
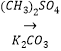
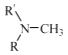 (R代表烃基,R'代表烃基或H) 请写出以
(R代表烃基,R'代表烃基或H) 请写出以 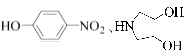 和(CH3)2SO4为原料制备
和(CH3)2SO4为原料制备 ![]() 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某市医学院研发出一种新型的补铁药品.该药品的有效成分是琥珀酸亚铁(暗黄色,难溶于水,易溶于HCl).为了检测该药品中的Fe2+ , 某学习小组设计了如图实验步骤: 
(1)A溶液中溶质的化学式是 . 加入A溶液后,不等加入新制氯水就产生浅红色的原因是 . 加入新制氯水之后的变化用离子方程式表示是 , 因产生Fe3+ , 溶液变成血红色.
(2)生成的血红色溶液放置时间过长,会最终褪色.甲同学猜想是Fe3+被还原成Fe2+导致褪色.证明甲同学的猜想不合理的实验操作是取少量褪色溶液,滴加 , 观察到现象即可证明.
(3)乙同学为检测药品中Fe的含量,设计并进行了如下实验: ①取样、碾碎,精确称取2.0g,加入过量盐酸,搅拌使其完全溶解;
②向所得溶液中加入过量H2O2溶液,再加入氨水至不再产生沉淀;
③将所得固体灼烧至恒重,得到0.8g纯净的红棕色粉末.
则该药品中铁的质量分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实与氢键无关的是( )
A. NH3分子极易溶于水B. 水结成冰体积膨胀,密度变小
C. 水加热到很高的温度都难以分解D. 水的沸点比H2S的沸点高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A由碳、氢、氧三种元素组成.现取3g A与4.48L(标准状况)氧气在密闭容器中充分燃烧,生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余).将反应生成的气体依次通过浓硫酸和碱石灰充分吸收,浓硫酸增重3.6g,碱石灰增重4.4g,剩余气体体积为1.12L(标准状况).回答下列问题:
(1)3g A燃烧后生成物的物质的量分别为:n(H2O)= , n(CO2)= , n(CO)= .
(2)通过计算确定A的分子式.
(3)写出A的一种可能的结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( ) 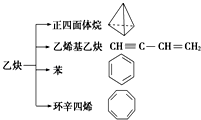
A.正四面体烷的分子式为C4H4 , 其二氯代物有两种
B.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量相同
C.苯为平面六边形结构,分子中存在C﹣C和C═C,能使酸性KMnO4溶液褪色
D.环辛四烯跟苯的结构很像,不能使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是重要的化工原料,用途广泛.
(1)合成氨工厂常用醋酸二氨合铜(由[Cu(NH3)2]+和CH3COO﹣构成)溶液吸收对氨合成催化剂有毒害的CO气体.
①醋酸二氨合铜所含的元素中,第一电离能最大的是 .
②醋酸二氨合铜所含元素的单质,所属的晶体类型有(填序号).
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
③第4周期中,基态原子与基态Cu原子未成对电子数目相同的元素有种(不含Cu).
④铜单质为面心立方晶体,其晶胞边长a nm.列式表示铜单质的密度 gcm﹣3 .
(2)BF3气体与NH3相遇立即生成一种白色晶体:BF3+NH3=F3B﹣NH3 .
①晶体F3B﹣NH3中,B原子的杂化轨道类型为 .
②写出两种与BF3具有相同空间构型的阴离子、 .
(3)NH3可用于合成尿素、硫酸铵等氮肥.某化肥厂从生产的硫酸铵中检出一种组成为N4H4(SO4)2的物质.该物质在水溶液中以SO42﹣和N4H44+两种正四面体构型的离子存在.N4H44+遇碱生成一种形似白磷的N4分子.
①下列相关说法中,正确的是(填序号).
a.N4是N2的同分异构体
b.1mol N4分解生成N2 , 形成了4mol π键
c.白磷的沸点比N4高,是因为P﹣P键键能比N﹣N键大
d.白磷的化学性质比N2活泼,说明P的非金属性比N强
②画出N4H44+的结构(标明其中的配位键) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐是一种常用的食品添加剂。新鲜鱼、肉用食盐腌渍后可以延长保存期,是因为 ( )
A.NaCl中的Cl-有杀菌作用
B.浓食盐水中含O2少,细菌无法生存
C.由于渗透作用使细菌失水死亡
D.由于渗透作用使鱼、肉细胞失水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,将体积为V L充满氨气的圆底烧瓶倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出,所得溶液的密度为ρgcm﹣3 . 下列说法错误的是( ) 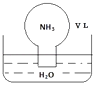
A.水最终会充满整个烧瓶
B.所得溶液的物质的量浓度为 ![]() molL﹣1
molL﹣1
C.所得溶液的质量分数为 ![]() ρ
ρ
D.将氨气换为二氧化氮,所得溶液的物质的量浓度也为 ![]() molL﹣1
molL﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com