
| A、溶液稳定,胶体和浊液都不稳定 |
| B、溶液中的分散质能通过滤纸但不能通过半透膜 |
| C、溶液和胶体的本质区别在于是否能产生丁达尔效应 |
| D、NaCl溶液和CaCO3悬浊液的本质区别是分散质粒子的大小 |


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
| A、Q1+Q2+Q3 |
| B、0.5Q3-Q2+2Q1 |
| C、0.5Q3+Q2-2Q1 |
| D、0.5(Q1+Q2+Q3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碱性氧化物 七氧化二锰 Mn2O7 |
| B、酸性氧化物 干冰 CO |
| C、酸 硫酸 H2S |
| D、盐 纯碱 Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 第一组 | 加入0.5g水 | 很快产生火花 |
| 第二组 | 加入1g胆矾 | 约30s产生火花 |
| 第三组 | 加入1g无水硫酸铜 | 1min内没有明显现象 |
| A、水能加快铝和碘的反应 |
| B、第三组铝和硫酸铜发生了置换反应 |
| C、第一组和第二组实验中均放出热量 |
| D、第一组实验中铝和碘发生反应生成了AlI3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| KMnO4酸性溶液的浓度/mol?L-1[学|科| | 溶液褪色所需时间 t/min | ||
| 第1次 | 第2次 | 第3次 | |
| 0.01 | 14 | 13 | 11 |
| 0.001 | 6 | 7 | 7 |
| 实验编号 | 20℃下,试管中所加试剂及其用量/mL | 20℃下溶液颜色褪至无色所需时间/min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | ||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
| 3 | 3.0 | 4.0 | 1.0 | 2.0 | 6.4 |
| 4 | 4.0 | 1.0 | 3.0 | 2.0 | 4.0 |
| 5 | 2.5 | 2.5 | 3.0 | 2.0 | 4.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
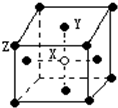 (1)某晶体的晶胞如图所示,X位于体心,Y位于6面心,Z位于顶点,该晶体中 X、Y、Z的粒子个数比为
(1)某晶体的晶胞如图所示,X位于体心,Y位于6面心,Z位于顶点,该晶体中 X、Y、Z的粒子个数比为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、950mL,11.2g |
| B、500mL,117g |
| C、1000mL,117.0g |
| D、任意规格,111.2g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸钡可用于钡餐透视 |
| B、为防止电池中的重金属离子污染土壤和水源,废电池要集中处理 |
| C、明矾可用于水的消毒、杀菌 |
| D、食醋可用于除去热水瓶中的水垢 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com