
ΓΨΧβΡΩΓΩΙΛ“Β…œ“‘ΗθΧζΩσ(÷ς“Σ≥…Ζ÷ΈΣFeOΓΛCr2O3)ΓΔΧΦΥαΡΤΓΔ―θΤχΚΆΝρΥαΈΣ‘≠Νœ…ζ≤ζ÷ΊΗθΥαΡΤ(Na2Cr2O7ΓΛ2H2O)Θ§Τδ÷ς“ΣΖ¥”ΠΈΣΔΌ4FeOΓΛCr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2Θ§ΔΎ2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2OΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ « (ΓΓΓΓ)
8Na2CrO4+2Fe2O3+8CO2Θ§ΔΎ2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2OΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ « (ΓΓΓΓ)
A. Ζ¥”ΠΔΌΚΆΔΎΨυΈΣ―θΜ·ΜΙ‘≠Ζ¥”Π
B. Ζ¥”ΠΔΌΒΡ―θΜ·ΦΝ «O2Θ§ΜΙ‘≠ΦΝ «FeOΓΛCr2O3
C. ΗΏΈ¬œ¬Θ§O2ΒΡ―θΜ·–‘«Ω”ΎFe2O3Θ§»θ”ΎNa2CrO4
D. Ζ¥”ΠΔΌ÷–ΟΩ…ζ≥…1 mol Na2CrO4 ±ΉΣ“ΤΒγΉ”3 mol
ΓΨ¥πΑΗΓΩB
ΓΨΫβΈωΓΩ
A. 4FeOΓΛCr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2÷–”–‘ΣΥΊΜ·ΚœΦέΒΡ±δΜ·Θ§Υυ“‘ «―θΜ·ΜΙ‘≠Ζ¥”ΠΘ§Εχ2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2O÷–ΟΜ”–‘ΣΥΊΜ·ΚœΦέΒΡ±δΜ·Θ§Υυ“‘≤Μ «―θΜ·ΜΙ‘≠Ζ¥”ΠΘ§Ι A¥μΈσΘΜ
8Na2CrO4+2Fe2O3+8CO2÷–”–‘ΣΥΊΜ·ΚœΦέΒΡ±δΜ·Θ§Υυ“‘ «―θΜ·ΜΙ‘≠Ζ¥”ΠΘ§Εχ2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2O÷–ΟΜ”–‘ΣΥΊΜ·ΚœΦέΒΡ±δΜ·Θ§Υυ“‘≤Μ «―θΜ·ΜΙ‘≠Ζ¥”ΠΘ§Ι A¥μΈσΘΜ
B. 4FeOΓΛCr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2÷–Θ§―θΤχ÷–―θ‘ΣΥΊΒΟΒγΉ”Μ·ΚœΦέΫΒΒΆΘ§Υυ“‘―θΜ·ΦΝ «―θΤχΘ§Χζ‘ΣΥΊΚΆΗθ‘ΣΥΊ ßΒγΉ”Μ·ΚœΦέ…ΐΗΏΘ§Υυ“‘ΜΙ‘≠ΦΝ «FeOΓΛCr2O3Θ§Ι B’ΐ»ΖΘΜ
8Na2CrO4+2Fe2O3+8CO2÷–Θ§―θΤχ÷–―θ‘ΣΥΊΒΟΒγΉ”Μ·ΚœΦέΫΒΒΆΘ§Υυ“‘―θΜ·ΦΝ «―θΤχΘ§Χζ‘ΣΥΊΚΆΗθ‘ΣΥΊ ßΒγΉ”Μ·ΚœΦέ…ΐΗΏΘ§Υυ“‘ΜΙ‘≠ΦΝ «FeOΓΛCr2O3Θ§Ι B’ΐ»ΖΘΜ
C. 4FeOΓΛCr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2÷–÷–Θ§―θΜ·ΦΝ «―θΤχΘ§ΜΙ‘≠ΦΝ «FeOΓΛCr2O3Θ§Υυ“‘―θΤχΒΡ―θΜ·–‘¥σ”ΎNa2CrO4ΚΆFe2O3Θ§ΒΪ≤ΜΡή≈–ΕœNa2CrO4ΚΆFe2O3ΒΡ―θΜ·–‘œύΕ‘«Ω»θΘ§Ι C¥μΈσΘΜ
8Na2CrO4+2Fe2O3+8CO2÷–÷–Θ§―θΜ·ΦΝ «―θΤχΘ§ΜΙ‘≠ΦΝ «FeOΓΛCr2O3Θ§Υυ“‘―θΤχΒΡ―θΜ·–‘¥σ”ΎNa2CrO4ΚΆFe2O3Θ§ΒΪ≤ΜΡή≈–ΕœNa2CrO4ΚΆFe2O3ΒΡ―θΜ·–‘œύΕ‘«Ω»θΘ§Ι C¥μΈσΘΜ
D. ”…ΖΫ≥Χ Ϋ4FeOΓΛCr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2 ΉΣ“ΤΒγΉ”Ω…÷ΣΘ§…ζ≥…1 mol Na2CrO4 ±Θ§≤ΈΦ”Ζ¥”ΠΒΡO2ΒΡΈο÷ ΒΡΝΩΈΣ
8Na2CrO4+2Fe2O3+8CO2 ΉΣ“ΤΒγΉ”Ω…÷ΣΘ§…ζ≥…1 mol Na2CrO4 ±Θ§≤ΈΦ”Ζ¥”ΠΒΡO2ΒΡΈο÷ ΒΡΝΩΈΣ![]() Θ§Ζ¥”Π÷–O‘ΣΥΊ”…0ΦέΫΒΒΆΈΣ-2ΦέΘ§ΒγΉ”ΉΣ“ΤΒΡΈο÷ ΒΡΝΩΈΣ≤ΈΦ”Ζ¥”ΠΒΡ―θΤχΒΡΈο÷ ΒΡΝΩΒΡ4±ΕΘ§ΉΣ“ΤΒγΉ”ΒΡΈο÷ ΒΡΝΩΈΣ
Θ§Ζ¥”Π÷–O‘ΣΥΊ”…0ΦέΫΒΒΆΈΣ-2ΦέΘ§ΒγΉ”ΉΣ“ΤΒΡΈο÷ ΒΡΝΩΈΣ≤ΈΦ”Ζ¥”ΠΒΡ―θΤχΒΡΈο÷ ΒΡΝΩΒΡ4±ΕΘ§ΉΣ“ΤΒγΉ”ΒΡΈο÷ ΒΡΝΩΈΣ![]() Θ§Υυ“‘Ζ¥”ΠΔΌ÷–ΟΩ…ζ≥…1 mol Na2CrO4 ±ΒγΉ”ΉΣ“Τ
Θ§Υυ“‘Ζ¥”ΠΔΌ÷–ΟΩ…ζ≥…1 mol Na2CrO4 ±ΒγΉ”ΉΣ“Τ![]() Θ§Ι D¥μΈσΓΘ
Θ§Ι D¥μΈσΓΘ
¥πΑΗ―ΓBΓΘ



| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΫη÷ζΧΪ―τΡήΫΪΙβΫβΥ°÷ΤH2”κΆ―ΝρΫαΚœΤπά¥Θ§Φ»Ρή¥σΖυΕ»ΧαΗΏΙβΫβΥ°÷ΤH2ΒΡ–ß¬ Θ§”÷ΡήΆ―≥ΐSO2Θ§ΙΛΉς‘≠άμ»γœ¬ΆΦΥυ ΨΓΘœ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «
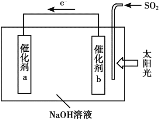
A. ΗΟΉΑ÷ΟΩ…ΫΪΧΪ―τΡήΉΣΜ·ΈΣΜ·―ßΡή
B. ¥ΏΜ·ΦΝbΗΫΫϋΒΡ»ή“ΚpH‘ω¥σ
C. Έϋ ’1mol SO2Θ§άμ¬έ…œΡή≤ζ…ζ1mol H2
D. ¥ΏΜ·ΦΝa±μΟφΖΔ…ζΒΡΖ¥”ΠΈΣΘΚ2H2OΘΪ2eΘ≠=H2ΓϋΘΪ2OHΘ≠
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ…ηNAΈΣΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ÷ΒΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «( )
A.‘Ύ±ξΉΦΉ¥Ωωœ¬Θ§78.0 g±Ϋ÷–Κ§”–ΧΦΧΦΥΪΦϋΒΡ ΐΡΩΈΣ3NA
B.22.4 L(±ξΉΦΉ¥Ωω)κ≤ΤχΚ§”–ΒΡ÷ Ή” ΐΈΣ18NA
C.‘Ύ±ξΉΦΉ¥Ωωœ¬Θ§2.24 L CHCl3÷–ΥυΚ§ΧΦ«βΦϋΒΡ ΐΡΩΈΣ0.1NA
D.0.1 molL-1ΒΡNa2CO3»ή“Κ÷–Θ§![]() ΒΡ ΐΡΩ–Γ”Ύ0.1NA
ΒΡ ΐΡΩ–Γ”Ύ0.1NA
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩXΓΔYΓΔZΓΔW ΨυΈΣΕΧ÷ήΤΎ‘ΣΥΊ Θ§ ΥϋΟ«‘Ύ÷ήΤΎ±μ÷–œύΕ‘ΈΜ÷Ο»γΆΦΥυ ΨΓΘ»τZ‘≠Ή”ΒΡΉνΆβ≤ψΒγΉ” ΐ «K≤ψΒγΉ” ΐΒΡ3±ΕΘ§ œ¬Ν–ΥΒΖ®÷–’ΐ»ΖΒΡ «

A.ΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΥ°Μ·ΈοΒΡΥα–‘Z±»W«Ω
B.÷Μ”…’βΥΡ÷÷‘ΣΥΊ≤ΜΡήΉι≥…”–ΜζΜ·ΚœΈο
C.”κZΒΡΒΞ÷ œύ±»ΫœΘ§YΒΡΒΞ÷ ≤Μ“Ή”κ«βΤχΖ¥”Π
D.XΓΔY–Έ≥…ΒΡΜ·ΚœΈοΕΦ «Έό…ΪΤχΧε
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
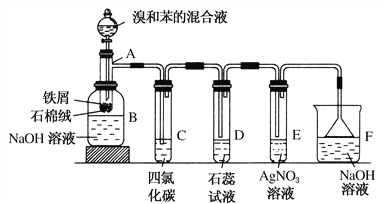
ΓΨΧβΡΩΓΩ(1)±ΫΚΆδεΒΡ»Γ¥ζΖ¥”ΠΒΡ Β―ιΉΑ÷Ο»γΆΦΥυ ΨΘ§Τδ÷–AΈΣΨΏ÷ß ‘ΙήΗΡ÷Τ≥…ΒΡΖ¥”Π»ίΤςΘ§‘ΎΤδœ¬ΕΥΩΣΝΥ“Μ–ΓΩΉΘ§»ϊΚΟ ·Οό»όΘ§‘ΌΦ”»κ…ΌΝΩΧζ–ΦΓΘ
Χν–¥œ¬Ν–Ω’ΑΉΘΚ
ΔΌ ‘ΙήA÷–ΒΡΖ¥”ΠΖΫ≥Χ ΫΈΣ_____________________________________ΓΘ
ΔΎ ‘ΙήC÷–ΥΡ¬»Μ·ΧΦΒΡΉς”Ο «ΘΚ____________________________ΓΘΖ¥”ΠΩΣ ΦΚσΘ§Ιέ≤λDΚΆEΝΫ ‘ΙήΘ§Ω¥ΒΫΒΡœ÷œσΈΣΘΚ________________________________ΓΘ
–¥≥ωE÷–Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ Ϋ__________________________________________ΓΘ
ΔέΖ¥”Π2ΓΪ3 minΚσΘ§‘ΎB÷–ΒΡNaOH»ή“ΚάοΩ…Ιέ≤λΒΫΒΡœ÷œσ «___________ΓΘ
Δή‘Ύ…œ ω’ϊΧΉΉΑ÷Ο÷–Θ§ΨΏ”–ΖάΒΙΈϋΙΠΡήΒΡ“«Τς”–________(ΧνΉ÷ΡΗ)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩοΊΘ®31GaΘ©ΓΔ’ύΘ®32GeΘ©ΕΦ «÷Ί“ΣΒΡœΓ”–Ϋπ τΘ§‘ΎΜ·―ߥΏΜ·ΦΝΓΔΑκΒΦΧε≤ΡΝœΓΔ–¬Ρή‘¥Β»Νλ”ρ”Π”ΟΙψΖΚΘ§Ω…¥”’ύΟΚ»Φ…’ΚσΒΡΖέΟΚΜ“Θ®Κ§ Ga2O3ΓΔGeO2ΓΔSiO2ΓΔAl2O3Θ©÷–Χα»ΓΘ§ ≤ΩΖ÷Νς≥Χ»γœ¬ΘΚ

“―÷ΣΘΚ
Έο÷ | GaCl3 | GeCl4 | AlCl3 |
Ζ–Βψ/Γφ | 201 | 84 | 183Θ®…ΐΜΣΘ© |
Θ®1Θ©¬Υ‘ϋΒΡ÷ς“Σ≥…Ζ÷ΈΣ_____ΓΘ
Θ®2Θ©ΔΌ÷–ΖΔ…ζΒΡΖ¥”Π”– Al2O3+6H+=2Al3++3H2OΓΔGa2O3+6H+=2Ga3++3H2O ΚΆ_____ΓΘ
Θ®3Θ©≤ΌΉς a ΒΡΟϊ≥Τ «_____Θ§ΔΎ÷–ΩΊ÷ΤΈ¬Ε»ΒΡΖΕΈß «_____Θ®ΧνΉ÷ΡΗ–ρΚ≈Θ©ΓΘ
aΘ°20~84Γφ bΘ°84~183Γφ cΘ°84~201Γφ
Θ®4Θ©Δή÷–ΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ «__________________________________________ΓΘ
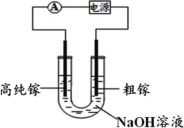
Θ®5Θ©οΊΡή”κΖ–Υ°ΨγΝ“Ζ¥”Π…ζ≥…«βΤχΘ§’ύ‘ΎΦ”»»ΧθΦΰœ¬”κ―ΈΥαΜρœΓΝρΥα≤ΜΖ¥”ΠΓΘ¥”‘≠Ή”ΫαΙΙΫ«Ε»Ϋβ ΆΤδ‘≠“ρΘΚ______________________
Θ®6Θ©”Ο≈®―ΈΥαΥαΜ·ΒΡΝΉΥα»ΐΕΓθΞΘ®TBPΘ©Ω…“‘¥”≤–“Κ÷–ίΆ»Γ Ga3+Θ§œύΙΊΖ¥”ΠΈΣΘΚTBP+GaCl3+HCl![]() TBPH+ΓΛGaCl
TBPH+ΓΛGaCl![]() ΓΘ”ΟœΓ NaOH »ή“ΚΕ‘”–ΜζœύΫχ––Ζ¥ίΆ»ΓΘ§”Ο―ΈΥαΒςΫΎΖ¥ίΆ»Γ“Κ pH ÷Ν 5~6Θ§»ΜΚσ…ΐΈ¬÷Ν 85~95ΓφΥ°ΫβΒΟΒΫ Ga(OH)3Θ§Ψ≠Κσ–χ¥ΠάμΒΟΒΫ¥÷οΊΓΘΫαΚœΜ·―ß”Ο”οΫβ Ά”ΟœΓ NaOH »ή“ΚΕ‘”–ΜζœύΫχ––Ζ¥ίΆ»ΓΒΡ‘≠“ρΘΚ_________________ΓΘ
ΓΘ”ΟœΓ NaOH »ή“ΚΕ‘”–ΜζœύΫχ––Ζ¥ίΆ»ΓΘ§”Ο―ΈΥαΒςΫΎΖ¥ίΆ»Γ“Κ pH ÷Ν 5~6Θ§»ΜΚσ…ΐΈ¬÷Ν 85~95ΓφΥ°ΫβΒΟΒΫ Ga(OH)3Θ§Ψ≠Κσ–χ¥ΠάμΒΟΒΫ¥÷οΊΓΘΫαΚœΜ·―ß”Ο”οΫβ Ά”ΟœΓ NaOH »ή“ΚΕ‘”–ΜζœύΫχ––Ζ¥ίΆ»ΓΒΡ‘≠“ρΘΚ_________________ΓΘ
Θ®7Θ©ΒγΫβΖ®Ω…“‘Χα¥Ω¥÷οΊΘ§ΨΏΧε‘≠άμ»γΆΦΥυ ΨΓΘοΊ‘Ύ―τΦΪ»ήΫβ…ζ≥…ΒΡ Ga3+”κ NaOH »ή“ΚΖ¥”Π…ζ≥… GaO![]() Θ§GaO
Θ§GaO![]() ‘Ύ“θΦΪΖ≈ΒγΒΡΒγΦΪΖ¥”Π Ϋ «_____________________ΓΘ
‘Ύ“θΦΪΖ≈ΒγΒΡΒγΦΪΖ¥”Π Ϋ «_____________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΈ“ΙζΩΤ―ßΦ“―–÷ΤΝΥ“Μ÷÷–¬–ΆΒΡΗΏ±»ΡήΝΩ–ΩΒβδε“ΚΝςΒγ≥ΊΘ§ΤδΙΛΉς‘≠άμ Ψ“βΆΦ»γœ¬ΓΘΆΦ÷–÷ϋ“ΚΤςΩ…¥Δ¥φΒγΫβ÷ »ή“ΚΘ§ΧαΗΏΒγ≥ΊΒΡ»ίΝΩΓΘ
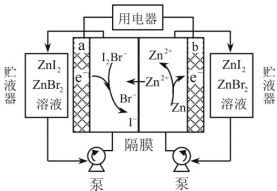
œ¬Ν––π ω≤Μ’ΐ»ΖΒΡ «Θ® Θ©
A.Ζ≈Βγ ±Θ§aΒγΦΪΖ¥”ΠΈΣI2Br-+2e- =2I-+ Br-
B.Ζ≈Βγ ±Θ§»ή“Κ÷–άκΉ”ΒΡ ΐΡΩ‘ω¥σ
C.≥δΒγ ±Θ§bΒγΦΪΟΩΦθ…Ό0.65gΘ§»ή“Κ÷–”–0.02mol I-- ±Μ―θΜ·
D.≥δΒγ ±Θ§aΒγΦΪΫ”ΆβΒγ‘¥’ΐΦΪ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΖ÷Ή” ΫΨυΈΣC5H10O2ΒΡΝΫ÷÷”–ΜζΈοΒΡΫαΙΙΦρ Ϋ»γ”“ΆΦΥυ ΨΘΚ
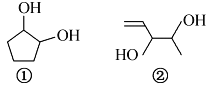
œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
A. Εΰ’ΏΕΦΡή ΙBr2ΒΡCCl4»ή“ΚΆ …Ϊ
B. ΔΌΔΎΖ÷Ή”÷–Υυ”–‘≠Ή”ΨυΩ…Ρή¥Π”ΎΆ§“ΜΤΫΟφ
C. Β»÷ ΝΩΒΡΔΌΚΆΔΎΖ÷±π”κΉψΝΩΡΤΖ¥”Π…ζ≥…Β»÷ ΝΩΒΡH2
D. ”κΤδΜΞΈΣΆ§Ζ÷“λΙΙΧεΒΡθΞ”–8÷÷Θ®≤ΜΩΦ¬«ΝΔΧε“λΙΙΘ©
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘Ύ“ΜΕ®ΧεΜΐΒΡΟή±’»ίΤς÷–Ϋχ––»γœ¬Μ·―ßΖ¥”ΠΘΚCO2(g)ΘΪH2(g)![]() CO(g)ΘΪH2O(g)Θ§ΤδΜ·―ßΤΫΚβ≥Θ ΐ(K)ΚΆΈ¬Ε»(t)ΒΡΙΊœΒ»γœ¬±μΥυ ΨΘΚ
CO(g)ΘΪH2O(g)Θ§ΤδΜ·―ßΤΫΚβ≥Θ ΐ(K)ΚΆΈ¬Ε»(t)ΒΡΙΊœΒ»γœ¬±μΥυ ΨΘΚ
t/Γφ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)ΗΟΖ¥”ΠΒΡΜ·―ßΤΫΚβ≥Θ ΐ±μ¥ο ΫΈΣKΘΫ_________________________ΓΘ
(2)ΗΟΖ¥”ΠΈΣ____________(ΧνΓΑΈϋ»»Γ±ΜρΓΑΖ≈»»Γ±)Ζ¥”ΠΓΘ
(3)Ρή≈–ΕœΗΟΖ¥”Π¥οΒΫΜ·―ßΤΫΚβΉ¥Χ§ΒΡ“άΨί «________ΓΘ
AΘ°»ίΤς÷–―Ι«Ω≤Μ±δ BΘ°ΜλΚœΤχΧε÷–c(CO)≤Μ±δ
CΘ°Π‘’ΐ(H2)ΘΫΠ‘Ρφ(H2O) DΘ°c(CO2)ΘΫc(CO)
(4)Ρ≥Έ¬Ε»œ¬Θ§ΤΫΚβ≈®Ε»ΖϊΚœœ¬ ΫΘΚc(CO2)ΓΛc(H2)ΘΫc(CO)ΓΛc(H2O)Θ§ ‘≈–Εœ¥Υ ±ΒΡΈ¬Ε»ΈΣ________ΓφΓΘ
(5)‘Ύ800 Γφ ±Θ§ΖΔ…ζ…œ ωΖ¥”ΠΘ§Ρ≥“Μ ±ΩΧ≤βΒΟ»ίΤςΡΎΗςΈο÷ ΒΡ≈®Ε»Ζ÷±πΈΣc(CO2)ΈΣ2 molΓΛLΘ≠1Θ§c(H2)ΈΣ1.5 molΓΛLΘ≠1Θ§c(CO)ΈΣ1 molΓΛLΘ≠1Θ§c(H2O)ΈΣ3 molΓΛLΘ≠1Θ§‘ρœ¬“Μ ±ΩΧΘ§Ζ¥”Πœρ________(ΧνΓΑ’ΐœρΓ±ΜρΓΑΡφœρΓ±)Ϋχ––ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com