
【题目】在两个绝热恒容的密闭绝热容器中进行下列两个可逆反应:
甲:C(s)+H2O(g)![]() CO(g)+H2(g)
CO(g)+H2(g)
乙:CO(g)+H2O(g) ![]() CO2(g)+H2(g)现有下列状态:
CO2(g)+H2(g)现有下列状态:
①混合气体平均相对分子质量不再改变;②气体的总物质的量不再改变;③各气体浓度相等;④反应体系中温度保持不变;⑤断裂氢氧键速率是断裂氢氢键速率的2倍;⑥混合气体密度不变;⑦v(H2O):v(H2)=1:1;⑧容器内压强不变。其中能表明甲、乙容器中反应都达到平衡状态的是( )
A.①③④⑥B.④⑤⑥⑦
C.④⑤⑧D.②④⑦⑧
【答案】C
【解析】
①混合气体平均相对分子质量等于气体质量除以气体物质的量,对甲来说,正向反应,气体质量增大,气体物质的量增大,用极限思维,平均相对分子质量减小,当相对分子质量不再改变,则达到平衡;对乙来说,正向反应,气体质量不变,气体物质的量不变,平均相对分子质量始终不变,因此不能作为判断平衡的标志,故①不符合题意;②对甲来说,正向反应,气体的总物质的量增加,当气体的总物质的量不再改变,则达到平衡;对乙来说,气体的总物质的量始终不变,因此不能作为判断平衡的标志,故②不符合题意;③各气体浓度相等都不能作为判断平衡的标志,故③不符合题意;④由于是绝热容器,温度在反应过程中要发生改变,当反应体系中温度保持不变,则都可以作为判断平衡的标志,故④符合题意;⑤断裂氢氧键是正向,断裂氢氢键是逆向,且两者断裂速率之比等于计量系数之比,因此能作为判断平衡的标志,故⑤符合题意;⑥混合气体密度等于气体质量除以容器体积,对甲来说,正向反应,气体质量增大,容器体积不变,密度增大,当密度不变时能作为判断平衡标志;对乙来说,正向反应,气体质量不变,容器体积不变,密度始终不变,因此不能最为判断平衡的标志,故⑥不符合题意;⑦υ(H2O):υ(H2)=1:1,没有说正向和逆向,因此不能作为判断平衡的标志,故⑦不符合题意;⑧由于是绝热恒容容器,温度或物质的量改变,致使容器内压强改变,当压强不变,则达到平衡的标志,故⑧符合题意;因此④⑤⑧符合题意,故C符合题意。
综上所述,答案为C。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】常温下,向50 mL溶有0.1molCl2的氯水中滴加2mol/L的NaOH溶液,得到溶液pH随所加NaOH溶液体积的变化图像如下图所示。下列说法正确的是
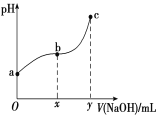
A. 若a点pH=4,且c(Cl-)=m·c(ClO-),则Ka(HClO)=![]()
B. 若x=100,b点对应溶液中:c(OH-)>c(H+),可用pH试纸测定其pH
C. b~c段,随NaOH溶液的滴入,![]() 逐渐增大
逐渐增大
D. 若y=200,c点对应溶液中:c(OH-)-c(H+)=2c(Cl-)+c(HClO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2A(g)+3B(g)![]() 4C(g)+D(g), 已知起始浓度c(A)=4 mol·L-1,c(B)=3 mol·L-1,C、D浓度均等于0,反应开始2 秒后达到平衡状态,此时D 的平衡浓度为0.5 mol·L-1,则下列说法不正确的是( )
4C(g)+D(g), 已知起始浓度c(A)=4 mol·L-1,c(B)=3 mol·L-1,C、D浓度均等于0,反应开始2 秒后达到平衡状态,此时D 的平衡浓度为0.5 mol·L-1,则下列说法不正确的是( )
A. 反应速率v(C)= 1mol/(L·s) B. C的平衡浓度为4mol /L
C. A的转化率为25% D. B的平衡浓度为1.5mol /L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,对于可逆反应N2(g)+3H2(g)![]() 2NH3(g),若N2、H2、NH3起始浓度分别为c1、c2、c3(均不为零),到达平衡时,N2、H2、NH3的浓度分别为0.1mol·L-1、0.3 mol·L-1、0.08mol·L-1,则下列判断正确的是( )
2NH3(g),若N2、H2、NH3起始浓度分别为c1、c2、c3(均不为零),到达平衡时,N2、H2、NH3的浓度分别为0.1mol·L-1、0.3 mol·L-1、0.08mol·L-1,则下列判断正确的是( )
A.c1:c2=3:1
B.平衡时,H2和NH3的生成速率之比为2:3
C.N2和H2的转化率不相等
D.c1的取值范围为0mol·L-1<c1<0.14mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容的密闭容器中通入一定量的A、B,发生反应A、B,发生反应:A(g)+2B(g)![]() 3C(g)+D(l),下图是A的正反应速率v(A)随时间变化的示意图。下列说法正确的是( )
3C(g)+D(l),下图是A的正反应速率v(A)随时间变化的示意图。下列说法正确的是( )
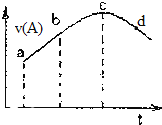
A.反应物A的浓度:a点小于b点
B.可能是某种物质对反应起到的催化作用
C.曲线上的c、d两点都表示达到反应限度
D.平均反应速率:ab段大于bc段
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用0.1000 mol·L1 NaOH溶液滴定20.00 mL 0.1000 mol·L1的H3A溶液的滴定曲线如图所示。己知H3A的pKa1、pKa2、pKa3分别为2、7和12(pKa=-lgKa),下列说法正确的是
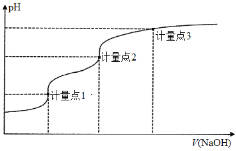
A.滴定前溶液pH值约为3
B.计量点1时,可以用甲基橙作为指示剂
C.到达计量点2时,溶液中存在c(Na+)=c(H2A-)+2c(HA2-)+3c(A3-)
D.到达计量点3时,微热溶液,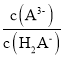 会增大
会增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性条件下,黄铁矿(FeS2)催化氧化的反应方程式为2FeS2 + 7O2+ 2H2O = 2Fe2+ + 4SO42 + 4H+。实现该反应的物质间转化如图所示。下列分析正确的是

A.反应Ⅰ中Fe(NO)2+作氧化剂
B.在酸性条件下,黄铁矿催化氧化中NO作中间产物
C.由反应Ⅱ可知,氧化性:Fe3+>SO42
D.反应Ⅲ的离子方程式为Fe2+ + NO =Fe(NO)2+,该反应是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】滴定实验是化学学科中重要的定量实验,氧化还原滴定实验与酸碱中和滴定类似。测血钙的含量时,进行如下实验:
①可将4mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mL l.0×l0-4mol/L的KMnO4溶液。
(1)写出KMnO4溶液滴定H2C2O4溶液的离子方程式______________________________________;滴定时,KMnO4溶液应装在______(“酸”或“碱”)式滴定管中,滴定终点时滴定现象是_________________________。
(2)下列操作会导致测定结果偏低的是_________。
A.滴定管在装液前未用标准KMnO4溶液润洗
B.滴定过程中,锥形瓶摇荡得太剧烈,锥形瓶内有液滴溅出
C.滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
D.达到滴定终点时,仰视读数
(3)计算:血液中含钙离子的浓度为_________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知几种短周期元素的原子半径、常见的最高价和最低价如下表,下列说法中不正确的是( )
元素编号 | |||||||
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | |
原子半径 | 0.073 | 0.075 | 0.152 | 0.110 | 0.099 | 0.186 | 0.143 |
最高正化合价 | 无 |
|
|
|
|
|
|
最低负化合价 |
|
| 无 |
|
| 无 | 无 |
A.⑦的简单离子不是同周期元素离子半径最小的
B.①元素的氢化物有两种
C.②的气态氢化物浓溶液可用于检验氯气管道的泄漏
D.阴离子的还原性④大于⑤,最高价氧化物的水化物的碱性③小于⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com