
【题目】以炼锌烟尘(主要成分为ZnO,含少量CuO和FeO)为原料,制取氯化锌晶体的工艺流程如下:
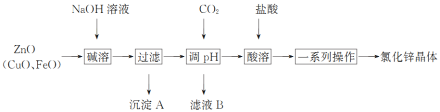
已知:Zn及其化合物的性质与Al及其化合物的性质相似,pH>11时,Zn(OH)2能溶于NaOH溶液生成ZnO22—。
(1)“调pH”步骤中通入过量CO2时发生反应的化学方程式为________;“酸溶”时发生反应的离子方程式为___________。
(2)下列说法不正确的是_______。
A 加入过量NaOH溶液的目的是提高锌元素的浸取率
B 沉淀A的主要成分是CuO、FeO
C 洗涤沉淀时,直接将洗涤剂加入漏斗,并用玻璃棒轻轻搅拌
D 利用结晶法可以从氯化锌溶液中获得氯化锌晶体
(3)流程中需进行蒸发浓缩,在实验室中进行蒸发浓缩的具体操作是_____。
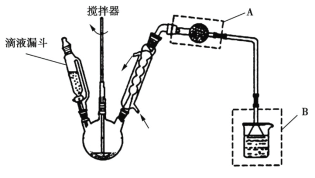
(4)氯化锌晶体是白色晶体,可含1、1.5、2.5、3、4个结晶水,易潮解,易溶于水,溶于乙醇、丙酮。由氯化锌晶体制备无水氯化锌的装置如图,其中滴液漏斗中盛放的是SOCl2(SOCl2熔点为105 ℃、沸点为78.8 ℃、遇水剧烈水解生成两种酸性气体)。
①下列物质中最适合洗涤氯化锌晶体的是_________。
A 冷水 B 浓盐酸 C 乙醇 D 氨水
②仪器A的名称为_______;装置B的作用是_________。
③以ZnCl2·H2O为例,写出三颈烧瓶中发生反应的化学方程式_______。
【答案】2CO2+2H2O+Na2ZnO2=Zn(OH)2↓+2NaHCO3 Zn(OH)2+2H+=Zn2++2H2O C 将溶液转移至蒸发皿中,控制温度加热至溶液表面形成一层晶膜 B 球形干燥管 吸收HCl和SO2,防止倒吸 ZnCl2·H2O+SOCl2=ZnCl2+2HCl↑+SO2↑
【解析】
本题主要考查考生对实验化学相关知识与技能的掌握,意在考查考生的实验能力及分析、判断能力。(1)“调pH”步骤中通入过量CO2时,CO2与Na2ZnO2反应生成Zn(OH)2沉淀和NaHCO3;“酸溶”时,氢氧化锌被盐酸溶解生成氯化锌和水,氢氧化锌难溶于水,在离子方程式中用化学式表示。
(2)选项A,加入过量NaOH溶液能使氧化锌完全溶解,从而提高锌元素的浸取率,正确;选项B,CuO、FeO为碱性氧化物,不能与氢氧化钠溶液反应,所以沉淀A的主要成分是CuO、FeO,正确;选项C,洗涤沉淀时,不能用玻璃棒搅拌,否则会破坏滤纸,错误;选项D,从氯化锌溶液中获得氯化锌晶体主要包括蒸发浓缩、冷却结晶、抽滤等步骤,故可采用结晶法获得氯化锌晶体,正确。故选C。(3)实验室中蒸发浓缩在蒸发皿中进行,加热至溶液表面形成一层晶膜即可。(4)①选项A,氯化锌晶体易溶于水,不能用冷水洗涤,错误;选项B,氯化锌晶体会水解,用浓盐酸洗涤能抑制其水解,同时减少溶解损失,正确;选项C,氯化锌晶体能溶于乙醇,不能用乙醇洗涤,错误;选项D,氯化锌晶体与氨水能发生反应,不能用氨水洗涤,错误。②仪器A为球形干燥管,仪器B中有倒置的漏斗,可以使吸收氯化氢和二氧化硫更充分,且能防止倒吸。③SOCl2利用遇水剧烈水解生成两种酸性气体的性质分析,ZnCl2·H2O和SOCl2反应生成无水氯化锌和盐酸和二氧化硫,方程式为:ZnCl2·H2O+SOCl2=ZnCl2+2HCl↑+SO2↑。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 2.4gMg在空气中燃烧生成MgO和Mg3N2转移的电子数为0.2NA
B. 标准状况下,18gH2O的体积是22.4L
C. 0.1L3mol·L-1NH4NO3溶液中含有的NH4+的数目为0.3NA
D. 1molCl2通入澄清的石灰水中转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知17g H2R中含1mol H,则R的摩尔质量为__________。
(2)同温同压下,等体积的NH3气和H2S气的质量之比为__________。
(3)若由NH3和H2S组成的混合气体的平均相对分子质量为20.4,则混合气中NH3和H2S的分子数之比为__________。
(4)配制500mL 0.2mol/L Na2CO3溶液,需要用托盘天平称量![]() 晶体的质量为__________ g。
晶体的质量为__________ g。
(5)将a L标准状况下的氯化氢气体溶于100mL水中(水的密度近似为1g/mL),得到密度为ρ g/mL的盐酸,则该盐酸的物质的量浓度是____________________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物的转化过程如图所示,下列分析合理的是

A. 催化剂a表面发生了极性共价键的断裂和形成
B. 在催化剂b表面形成氮氧键时,不涉及电子转移
C. N2与H2反应生成NH3的原子利用率为100%
D. 催化剂a、b能提高反应的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用印刷电路的废腐蚀液(含有大量CuCl2、FeCl2和FeCl3)回收Cu,主要流程如下:
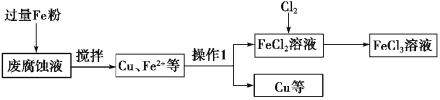
(1)操作1的名称是__________,需要用到的玻璃仪器有________________________。
(2)加入过量铁粉发生的离子反应有_______________。
(3)获得的铜粉中含有杂质,除杂所需的试剂是_______________(填化学式)。
(4)实验室利用如图所示装置制取一定量的FeCl3。
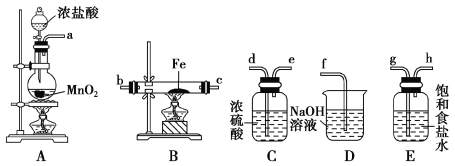
各装置的正确连接顺序为(填写装置代号)A→______→______→______→D。装置C的作用是____________________________,写出装置D中反应的离子方程式:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验。

(1)向A、B溶液中分别滴入几滴KSCN溶液, A溶液颜色:________B溶液颜色_______。
(2)写出上述过程中有关反应的离子方程式:A→B___________________。若有2mol的A参与该反应,则转移______mol电子。A作_____剂
(3)B→C(暴露在空气中)可看到的现象是__________________________________。
(4)将A的饱和溶液制成胶体的操作______________________;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为___________效应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铝土矿主要含Al2O3。某课题组以此为原料回收氧化铝,设计实验流程如下:
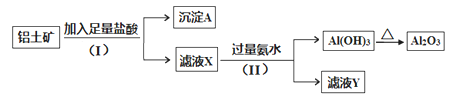
(1)步骤(I)中分离溶液和沉淀的操作名称是______,实验中除了烧杯和玻璃棒外,还需要用到的玻璃仪器是______________。
(2)写出步骤(Ⅱ)中生成Al(OH)3的离子方程式_______________________________。
(3)实验室里用NaAlO2 溶液制取Al(OH)3最好选用________(填序号)。
A.NaOH溶液 B.稀硫酸 C.二氧化碳
(4)取54g铝土矿进行实验,最后得到氧化铝51g,则该铝土矿中铝的含量为______(假设实验过程没有损失)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着石油资源的日趋紧张,天然气资源的开发利用受到越来越多的关注。以天然气(主要成分是CH4)为原料经合成气(主要成分为CO、H2)制化学品,是目前天然气转化利用的主要技术路线。而采用渣油、煤、焦炭为原料制合成气,常因含羰基铁[Fe(CO)5]等而导致以合成气为原料合成甲醇和合成氨等生产过程中的催化剂产生中毒。请回答下列问题:
(1)[Fe(CO)5]中铁的化合价为0,写出铁原子的基态电子排布式:_____________________。
(2)与CO互为等电子体的分子和离子分别为________和________(各举一种即可,填化学式),CO分子的电子式为________,CO分子的结构式可表示成________。
(3)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有___,CH3OH的熔、沸点比CH4高,其主要原因是__________。
(4)CH3CHO分子中,—CH3中的碳原子采取________杂化方式,—CHO中的碳原子采取________杂化方式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察图示,然后回答问题:
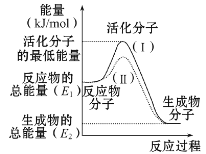
①图中所示反应是________(填“吸热”或“放热”)反应,该反应________ (填“需要”或“不需要”)加热,该反应的ΔH=________ (用含E1、E2的代数式表示)。
②已知热化学方程式:H2(g)+ ![]() O2(g)====H2O(g) ΔH=-241.8 kJ/mol。该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为_____________。
O2(g)====H2O(g) ΔH=-241.8 kJ/mol。该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为_____________。
(2)有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是
A.CH3OH(g)+H2O(g)====CO2(g)+3H2(g) ΔH=+49.0 kJ/mol
B.CH3OH(g)+ ![]() O2(g)====CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol
O2(g)====CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol
另外H2O(l)====H2O(g) ΔH=+44 kJ/mol,请写出32 g 的CH3OH(g)完全燃烧生成液态水的热化学方程式______________________。
(3)已知反应2HI(g)![]() H2(g)+I2(g)的ΔH=+11 kJ·mol-1,1 mol H2(g)、1 mol I2(g)分子中化学键断裂时分别需要吸收436 kJ、151 kJ的能量,则1 mol HI(g)分子中化学键断裂时需吸收的能量为__kJ。
H2(g)+I2(g)的ΔH=+11 kJ·mol-1,1 mol H2(g)、1 mol I2(g)分子中化学键断裂时分别需要吸收436 kJ、151 kJ的能量,则1 mol HI(g)分子中化学键断裂时需吸收的能量为__kJ。
(4)甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)![]() CH3OH(g) ΔH1
CH3OH(g) ΔH1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH2
CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH3
CO(g)+H2O(g) ΔH3
已知反应①中相关的化学键键能数据如下:
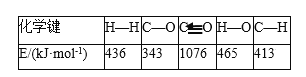
由此计算ΔH1=____kJ·mol-1;已知ΔH2=-58 kJ·mol-1,则ΔH3=____kJ·mol-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com