
| ||


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
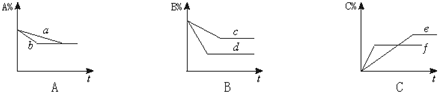
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 元素性质或原子结构信息 |
| Q | 原子核外有6种不同运动状态的电子 |
| R | 最外层电子数是次外层电子数的3倍 |
| X | 气态氢化物的水溶液呈弱碱性 |
| Y | 第三周期元素的简单离子中离子半径最小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:2 | B、2:1 |
| C、1:4 | D、1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
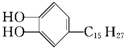 是生漆的主要成分,黄色,能溶于有机溶剂.生漆涂在物体表面能在空气中干燥而转变为黑色漆膜.下列关于漆酚说法错误的是( )
是生漆的主要成分,黄色,能溶于有机溶剂.生漆涂在物体表面能在空气中干燥而转变为黑色漆膜.下列关于漆酚说法错误的是( )| A、可以燃烧,当氧气充分时,产物为CO2和H2O |
| B、与FeCl3溶液发生显色反应 |
| C、能发生取代反应和加成反应 |
| D、不能被酸性KMnO4溶液氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com