
【题目】H2O2是一种常用绿色氧化剂,工业上利用电解法制备H2O2的装置如图所示,初始溶液为氢氧化钠溶液:下列说法正确的是( )

A. a为负极
B. 通入空气的电极反应式为O2+2e﹣+2H+═H2O2
C. 电解一段时间后,左侧溶液pH降低
D. 若生成17g双氧水,则有1molH+从左侧向右侧迁移
科目:高中化学 来源: 题型:
【题目】催化还原CO2是解决温室效应及能源问题的重要手段之一。研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO。反应的热化学方程式如下:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CO2(g)+H2(g)![]() CO(g)+H2O(g)ΔH2 II
CO(g)+H2O(g)ΔH2 II
某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
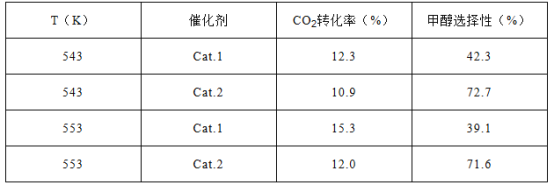
【备注】催化剂.1:Cu/ZnO纳米棒;催化剂.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醇的百分比
已知:①CO和H2的标准燃烧热分别为-283.0kJ·mol-1和-285.8kJ·mol-1
②H2O(l)![]() H2O(g)ΔH3=44.0kJ·mol-1
H2O(g)ΔH3=44.0kJ·mol-1
请回答(不考虑温度对ΔH的影响):
(1)反应I的平衡常数表达式K=_________;反应II的ΔH2=_____________kJ·mol-1。
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有_________________。
A.使用催化剂.1 B.使用催化剂.2 C.降低反应温度
D.投料比不变,增加反应物的浓度 E.增大CO2和H2的初始投料比
(3)表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用电化学法还原CO2是一种使CO2资源化的方法,如图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )
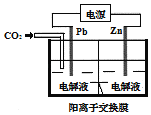
A. Pb与电源的正极相连
B. ZnC2O4在离子交换膜右侧生成
C. 正极反应式为:Zn﹣2e﹣═Zn2+
D. 标准状况下,当11.2 L CO2参与反应时,转移0.5mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列叙述错误的是
A. 回收的地沟油可以用来制造肥皂、提取甘油或生产生物柴油
B. 纳米材料粒子直径一般从几纳米到几十纳米,因此纳米材料属于胶体
C. 纤维素属于多糖,但不是人类的营养物质
D. 绿色化学的核心是应用化学原理从源头上减少和消除工业生产对环境的污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属材料是人类社会发展的重要物质基础。下列说法正确的是
A.钛及钛合金是目前使用量最大的金属材料
B.镁是一种国防金属,电解熔融MgCl2可得到单质镁
C.珠港澳大桥为了防腐蚀可以在钢铁中增加含碳量
D.稀土(钇、钪及镧系)是战略金属,稀土元素均位于ⅡA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O中,若二氧化锰与足量的浓盐酸反应制得3.55gCl2 , 通过计算回答:用双线桥标出反应中电子转移的方向和数目 , 参加反应的HCl的物质的量为 , 其中被氧化的HCl的质量 .
MnCl2+Cl2↑+2H2O中,若二氧化锰与足量的浓盐酸反应制得3.55gCl2 , 通过计算回答:用双线桥标出反应中电子转移的方向和数目 , 参加反应的HCl的物质的量为 , 其中被氧化的HCl的质量 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,在一个容积固定的恒温容器中,有两个可左右滑动的密封隔板,在A、B、C内分别充入等质量的X、H2、Y三种气体,当隔板静止时,A、C内的气体密度相等。下列说法不正确的是
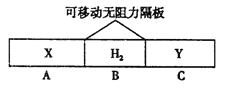
A. 摩尔质量: M(X)=M(Y) B. 分子数目:N(X)=N(Y)
C. 气体的体积:V(X)=V(Y) D. 物质的量: n(X)<n(H2)<n(Y)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,电离平衡常数:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.8×10﹣5 | K1=4.3×10﹣7 K2=5.6×10﹣11 | 3.0×10﹣8 |
回答下列问题:
(1)物质的量浓度为0.1mol/L的下列四种物质:a.Na2CO3,b.NaClO,c.CH3COONa d.NaHCO3;pH由大到小的顺序是: ;(填编号)
(2)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是: ;
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)c(OH﹣) D.c (OH﹣)/ c(H+)
(3)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图.

则HX的电离平衡常数 (填“大于”、“等于”或“小于”)醋酸的平衡常数;理由是 ,
稀释后,HX溶液中水电离出来的c(H+) 醋酸溶液水电离出来c(H+)(填“大于”、“等于”或“小于”)
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO﹣)﹣c(Na+)= .(填准确数值).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com