
����Ŀ�����οɵ��»������еĸֽʴ��Ϊ��ֹ�������еĸֽʴ�����ڻ������������һ���������Һ�������Խ����������������У����Խ�����������ֽ�ֱ������ⲿֱ����Դ�Ӷ���ȥCl-��װ����ͼ������˵���������
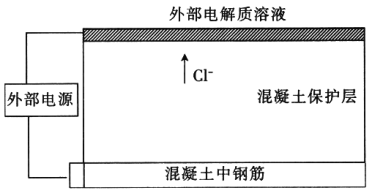
A. �ֽ�ӵ�Դ������
B. �����������Ϸ����ĵ缫��ӦΪ2Cl��2e-=Cl2��
C. �������еĸ�������ֽ���ƶ�
D. ���һ��ʱ���ֽ����Һ��pH����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019��11�¡�Science����־����������������Ŷӷ�������ȡH2O2����ɫ������ԭ����ͼ��ʾ����֪��H2O2![]() H�� + HO2����Ka��2.4��10-12��������˵���������
H�� + HO2����Ka��2.4��10-12��������˵���������

A.a���ĵ��Ƶ���b��
B.YĤΪѡ���������ӽ���Ĥ
C.ÿת��0.4 mol e��������0.1 mol H2O2����
D.b���ĵ缫��ӦΪO2 + 2e�� + H2O = HO2�� + OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���ѧ��Ӧ����ʽ����Ӧ���;���ȷ����
ѡ�� | ��ѧ��Ӧ����ʽ | ��Ӧ���� |
A | CH3COOH��CH3CH2OH | ������Ӧ |
B | CH4��Cl2 | �û���Ӧ |
C | CH2=CH2��Br2 CH3CHBr2 | �ӳɷ�Ӧ |
D |
| ȡ����Ӧ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���¼����Ŀ���Ӧ�ã����������ڸ��ƻ��������������ܳ�ֿ�������������DZ�ڼ�ֵ��
�ش��������⣺
��1�����̵������������ϳɼ״��漰�����¼�����Ӧ��
��CO(g)+2H2(g)=CH3OH(g) ��H=-91kJ��mol-1
��2CO2(g)=2CO(g)+O2(g) ��H=+566kJ��mol-1
��2H2(g)+O2(g)=2H2O(g) ��H=-483.6kJ��mol-1
��CO2(g)+3H2(g)=CH3OH(g)+H2O(g)H=__kJ��mol-1��
��2�����ݻ���Ϊ2L�����������ܱ������з�����ӦCO(g)+H2O(g)![]() CO2(g)+H2(g)���й��������£�
CO2(g)+H2(g)���й��������£�

��800��Cʱ�÷�Ӧ��ƽ�ⳣ��K=__��
������2��x=__��n=___��
����800����ʼʱ����2L�����ܱ������м���CO��H2O��CO2��H2��1mol�����ʱv��__v��(����>����<������=��)��
��3����Ӧ(NH4)2CO3+H2O+CO2![]() 2NH4HCO3OH�����ڲ������е�CO2��Ϊ�о��¶ȶ�(NH4)2CO3����CO2Ч�ʵ�Ӱ�죬��ij�¶�T1�£���һ������(NH4)2CO3��Һ�����ܱ������У�������һ������CO2���壬��tʱ�̣����������CO2�����Ũ�ȡ�Ȼ��ֱ����¶�ΪT2��T3��T4��T5�£�����������ʼʵ���������䣬�ظ�����ʵ�飬������ͬʱ��ⶨCO2�����Ũ�ȣ��õ�������ͼ��ͼ��
2NH4HCO3OH�����ڲ������е�CO2��Ϊ�о��¶ȶ�(NH4)2CO3����CO2Ч�ʵ�Ӱ�죬��ij�¶�T1�£���һ������(NH4)2CO3��Һ�����ܱ������У�������һ������CO2���壬��tʱ�̣����������CO2�����Ũ�ȡ�Ȼ��ֱ����¶�ΪT2��T3��T4��T5�£�����������ʼʵ���������䣬�ظ�����ʵ�飬������ͬʱ��ⶨCO2�����Ũ�ȣ��õ�������ͼ��ͼ��
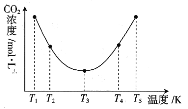
��H__0(����>����<������=��)��T1~T2���䣬c(CO2)�仯��ԭ����___��
����֪������NH3��H2O�ĵ��볣��K=1.8��10-5��̼��ĵ��볣��K1=4.4��10-7��K2=4.7��10-11����ǡ����ȫ��Ӧʱ���õ�NH4HCO3��Һ��c(H+)__c(OH-)(����>����<������=��)��
����ͼ����ʾ�����¶��£��÷�Ӧ��ƽ�ⳣ�������¶���__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ������ȷ���ǣ���H�ľ���ֵ����ȷ����������
A.C2H5OH��1��+3O2��g��=2CO2��g��+3H2O��g����H=��1367.0 kJ��![]() ��ȼ���ȣ�
��ȼ���ȣ�
B.NaOH��aq��+HCl��aq��=NaCl��aq��+H2O��1�� ��H=+57.3 kJ��![]() ���к��ȣ�
���к��ȣ�
C.S��s��+O2��g��=SO2��g�� ��H=��269.8 kJ��![]() ����Ӧ�ȣ�
����Ӧ�ȣ�
D.2NO2=O2+2NO ��H=+116.2 kJ��![]() ����Ӧ�ȣ�
����Ӧ�ȣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о����֣���Ԫ�������˵���ϸ�����ʵ��ز����Ԫ�ؿ�Ԥ����״���״��������Ҳ�ᵼ�¼�״���״���˲������������Ԫ��ʱҲҪ�ʿɶ�ֹ���Իش��������⣺
��1��FeҲ��������Ҫ�����Ԫ��֮һ����д��Fe2+�ĺ�������Ų�ʽ��__��
��2����Alͬһ���ڵ�Na��MgԪ��Ҳ����������Ԫ�أ�Na��Mg��Al��̬ԭ�ӵ�һ�����ܵĴ�С��ϵ��__��
��3���Ȼ������۵���194�棬���������۵���2054�棬���ǹ�ҵ�ϲ����õ�������Ȼ����ķ�����ȡ�����ʣ�������Ϊ__��
��4��F��I��ͬһ�����Ԫ�أ�BeF2��H2O����������ԭ�ӹ��ɵĹ��ۻ�������ӣ����߷����е�����ԭ��Be��O���ӻ���ʽ�ֱ�Ϊ__��__��BeF2���ӵ����幹����___��H2O���ӵ����幹����__��
��5��I2����ľ����ṹ��ͼ��ʾ���þ����к���__��I2���ӣ���þ����ľ�������Ϊacm����I2���ܶ���__g��cm-3��
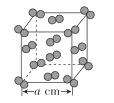
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijNiO�ķ�������FeO��CuO��Al2O3��MgO��SiO2�����ʣ��ô˷�����ȡNiSO4��Ni���������£�
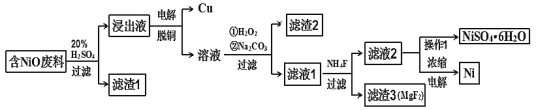
��֪���йؽ���������������������������pH��ͼ��

��1������1����Ҫ�ɷ�Ϊ____��
��2���������ӷ���ʽ���ͼ���H2O2������____��
�ڼ�Na2CO3������Һ��pH��5��������2����Ҫ�ɷ�Ϊ____��
��3������Һ2�л��NiSO4��6H2O��ʵ�������____�����ˡ�ϴ�ӡ����
��4�����Ũ�������Һ2�ɻ�ý��������������Ӧԭ��ʾ��ͼ��ͼ��
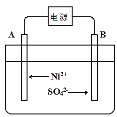
��B������pH��____������������������С������������������ƽ���ƶ�ԭ������B������pH�仯��ԭ��____��
��һ��ʱ�����A��B�������ռ���11.2L����(��״����)���������ܵõ�Ni____g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ֻ��C��H��O����Ԫ�أ�����ӵ����ģ����ͼ��ʾ�������й���12��ԭ��(ͼ��������֮������ߴ���������˫���Ȼ�ѧ��)��

(1)�������к��������ŵĽṹ��ʽΪ________��
(2)���������У�������ʻ�Ϊͬ���칹�����________(�����)��
A��CH3CH2CH2COOH
B��OHCCH(CH3)CHO
C��CH3CH2CH===CHCOOH
D��CH2===CHCOOCH3
(3)�÷����й�ƽ���ԭ�������Ϊ________(��֪�Ȼ����ĸ�ԭ�ӿ��Թ�ƽ��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����仯������������;��������ʵ������������±���ʾ��
H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
�۵�/�� | ��85.5 | 115.2 | ��600(�ֽ�) | ��75.5 | 16.8 | 10.3 |
�е�/�� | ��60.3 | 444.6 | ��10.0 | 45.0 | 337.0 |
�ش��������⣺
��1����̬Feԭ�Ӽ۲���ӵĹ����ʾʽΪ_________����̬Sԭ�ӵ���ռ������ܼ��ĵ���������ͼΪ________�Ρ�
��2�����ݼ۲���ӶԻ������ۣ�H2S��SO2��SO3����̬�����У�����ԭ�Ӽ۲���Ӷ�����ͬ���������ӵ���____________��
��3��ͼ(a)ΪS8�Ľṹ�����۵�ͷе�Ҫ�ȶ���������۵�ͷе�ߺܶ࣬��Ҫԭ��Ϊ___________��
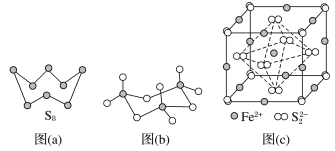
��4����̬���������Ե�������ʽ���ڣ�����ӵ����幹��Ϊ____________�Σ����й��ۼ���������________�֣��������������д�����ͼ(b)��ʾ�����۷��ӣ��÷�����Sԭ�ӵ��ӻ��������Ϊ__________��
��5��FeS2����ľ�����ͼ(c)��ʾ�������߳�Ϊa nm��FeS2���ʽ��ΪM�������ӵ�������ֵΪNA���侧���ܶȵļ������ʽΪ______g��cm��3��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com