
����Ŀ��ij����ֻ��C��H��O����Ԫ�أ�����ӵ����ģ����ͼ��ʾ�������й���12��ԭ��(ͼ��������֮������ߴ���������˫���Ȼ�ѧ��)��

(1)�������к��������ŵĽṹ��ʽΪ________��
(2)���������У�������ʻ�Ϊͬ���칹�����________(�����)��
A��CH3CH2CH2COOH
B��OHCCH(CH3)CHO
C��CH3CH2CH===CHCOOH
D��CH2===CHCOOCH3
(3)�÷����й�ƽ���ԭ�������Ϊ________(��֪�Ȼ����ĸ�ԭ�ӿ��Թ�ƽ��)��
���𰸡���COOH BD 10
��������
�������ʳɼ��ص��֪������4����������C����һ���жϳ�С����ΪH����һ��ΪO��
(1)���ݷ���ģ�Ϳ�֪�������ʵĽṹ��ʽΪCH2===C(CH3)COOH������������Ϊ-COOH����Ϊ��-COOH��
(2) A. CH3CH2CH2COOH��CH2===C(CH3)COOH����ʽ��ͬ��A����
B. OHCCH(CH3)CHO��CH2===C(CH3)COOH����ʽ��ͬ���ṹ��ͬ����Ϊͬ���칹�壬B��ȷ��
C. CH3CH2CH===CHCOOH��CH2===C(CH3)COOH����ʽ��ͬ��C����
D. CH2===CHCOOCH3��CH2===C(CH3)COOH����ʽ��ͬ���ṹ��ͬ����Ϊͬ���칹�壬D��ȷ����Ϊ��BD��
(3)̼̼˫����ƽ��ṹ���Ȼ����ĸ�ԭ�ӿ��Թ�ƽ�棬��ͼ��ʾ���÷����й�ƽ���ԭ�������Ϊ10��(���С�����)��
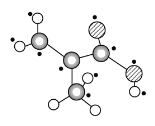
����10��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA ��ʾ�����ӵ�����,������˵������ȷ����
A.2��H2������ԭ����ĿΪNA
B.2molO3��3molO2��������ԭ��������6NA
C.���³�ѹ��,11.2L������ԭ����ΪNA��
D.2.3g�����ƺ��еĵ�����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����οɵ��»������еĸֽʴ��Ϊ��ֹ�������еĸֽʴ�����ڻ������������һ���������Һ�������Խ����������������У����Խ�����������ֽ�ֱ������ⲿֱ����Դ�Ӷ���ȥCl-��װ����ͼ������˵���������
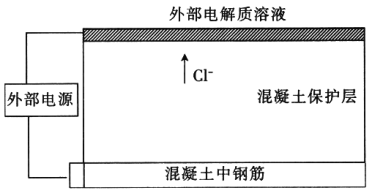
A. �ֽ�ӵ�Դ������
B. �����������Ϸ����ĵ缫��ӦΪ2Cl��2e-=Cl2��
C. �������еĸ�������ֽ���ƶ�
D. ���һ��ʱ���ֽ����Һ��pH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��ȡŨ�Ⱦ�Ϊ0.1000mol/L�Ĵ�����Һ�Ͱ�ˮ��Һ��20.00mL���ֱ���0.1000mol/LNaOH��Һ��0.1000mol/L��������к͵ζ����ζ�������pH��μ���Һ������仯��ϵ��ͼ��ʾ������˵������ȷ���ǣ� ��
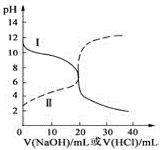
A.�ɵζ����ߣ�25��ʱKa(CH3COOH)=Kb(NH3��H2O)=10-5
B.��NaOH��Һ������μӵ�20.00mLʱ�����ߢ�͢�պó��ֽ���
C.���ߢμ���Һ��10.00mLʱ����Һ��c(CH3COO-)+c(OH-)��c(H+)
D.����μ���NaOH��Һ��������40.00mL�Ĺ����У�ˮ�ĵ���̶���������С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2008����˻ἴ���ڱ������У������й�˵������ȷ���� �� ��
A.���ƻ���ȼ���DZ��飬�����ʽΪ![]()
B.���˻Ὣ�ϲ��˶�Ա�����˷ܼ����������˷ܼ��Ľṹ��ʽΪ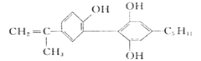 �������ʽΪC20H24O3
�������ʽΪC20H24O3
C.���˻���ʹ�õ�﮵��Ϊ���ܵ�أ��������ص����ṩ��ͬ����ʱ����Ľ�������������С
D.������������������Ļ�ѧ�ɷ���Ҫ�Ǻ�ˮ��þ�����Σ���![]() ���ɱ�ʾΪ
���ɱ�ʾΪ![]() ��
��![]() ��
��![]() ��
��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2008���˼����︣�ޣ������Ϊ����ë�ߣ��ڳ���Ϊ���ľ�����ά(��ͼ)������˵����ȷ����

A. ��ë�������ά�Ļ�ѧ�ɷ���ͬ
B. �þ�����ά�ĵ���Ϊ�Ա���������Ҵ�
C. ������ά����ëһ�������¾���ˮ��
D. ������ά���ڴ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������е��л�������ḻ������ʳס�еȶ��Ӧ�ù㷺�������Ҵ��DZȽϳ������л��
(1)�Ҵ�����ɫ��������ζ��Һ�壬�ܶȱ�ˮ_____��
(2)��ҵ������ϩ��ˮ��Ӧ���Ƶ��Ҵ����÷�Ӧ�Ļ�ѧ����ʽΪ___��(����д��Ӧ����)
(3)���������Ҵ���ͬϵ�����___�������Ҵ���ͬ���칹�����____��(ѡ����)
A��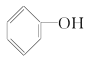 B��
B��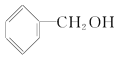 C��CH3CH2��O��CH2CH3
C��CH3CH2��O��CH2CH3
D��CH3OH E��CH3��O��CH3 F��HO��CH2CH2��OH
(4)�Ҵ��ܹ�����������Ӧ��
���Ҵ���ͭ�������������¿ɱ�������������Ӧ�Ļ�ѧ����ʽΪ________��
��46g�Ҵ���ȫȼ������___mol������
������˵����ȷ����___(ѡ����ĸ)��
A���Ҵ����ܺ����Ը��������Һ����������ԭ��Ӧ
B��ʵ��������ϩʱ���¶ȿ�����140��
C���ƾ���ijЩ���ォ�Ҵ�����Ϊ���ᣬ���Ǿƾͱ�����
D������ľƺ�������Ϊ�Ҵ����Ҵ����������ɵ����ᷢ��������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������������ȷ���ǣ� ��
A.10��ʱNaCl�ܽ��Ϊ35.7 g�����ʱ����NaCl��Һ����������С��35.7��
B.��Na2CO3��Һ�м�������NaHCO3���壬��ҺpH��С
C.50 mL1.0 mol��L-1������60 mL 1.0 mol��L-1����ֱ��50 mL 1.1 mol��L-1�� NaOH��Һ���з�Ӧ���к�����ֵ�����
D.һ�������£���ˮ�м�������Na2SO4����ʹˮ�ĵ���̶ȼ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���⼰�仯�����ںϳ�ɱ������ҩ��ȷ�����й㷺��;���ش��������⣺
��1�������ĵ⸻���ں����У���ˮ��ȡ��Ũ��������Ũ��Һ�м�MnO2��H2SO4�����ɵõ�I2���÷�Ӧ�Ļ�ԭ����Ϊ____________��
��2������Ũ��Һ�к���I-��Cl-�����ӣ�ȡһ������Ũ��Һ�������еμ�AgNO3��Һ����AgCl��ʼ����ʱ����Һ��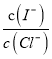 Ϊ��_____________����֪Ksp��AgCl��=1.8��10-10��Ksp��AgI��=8.5��10-17��
Ϊ��_____________����֪Ksp��AgCl��=1.8��10-10��Ksp��AgI��=8.5��10-17��
��3����֪��Ӧ2HI(g) ===H2(g) + I2(g)����H= +11kJmol��1��1mol H2(g)��1mol I2(g)�����л�ѧ������ʱ�ֱ���Ҫ����436kJ��151kJ����������1molHI(g)�����л�ѧ������ʱ�����յ�����Ϊ______________kJ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com