
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是( )
A.100mL 1mol/LFeCl3溶液中含有0.1NA个Fe3+
B.1.06g Na2CO3含有的CO32﹣离子数小于0.01 NA
C.PH=3的醋酸溶液中,含有的H+数为0.001NA
D.2L 0.5mol/L的氨水中,含有NH3H2O、NH4+、NH3的总数为1 NA
科目:高中化学 来源: 题型:
【题目】对铁及其化合物的叙述不正确的是( )
A. 可用KSCN溶液检验Fe3+B. Fe(OH)2能在空气中稳定存在
C. Fe能从CuSO4溶液中置换出CuD. Fe2O3与Al可发生铝热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用海洋资源获得的部分物质如图所示,有关说法正确的是( ) 
A.在化学反应中, ![]() H2O可转变为D2O
H2O可转变为D2O
B.“加碘食盐”生产中碘添加剂为单质I2
C.实验室用带玻璃塞的棕色瓶贮存液Br2
D.电解饱和MgCl2溶液时在阴极得到Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中Cl--浓度由大到小的顺序是( )
①200 mL 2 mol/L MgCl2溶液 ②1000 mL 2.5mol/L NaCl溶液 ③300 mL 5 mol/L KCl溶液 ④250 mL 1 mol/LFeCl3溶液
A. ②③①④ B. ④①②③ C. ①④②③ D. ③①④②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K4[Fe(CN)6]强热可发生反应:3K4[Fe(CN)6] ![]() 2 (CN)2↑+12KCN+N2↑+Fe3C+C
2 (CN)2↑+12KCN+N2↑+Fe3C+C
(1)K4[Fe(CN)6]中Fe2+的配位数为(填数字);Fe2+基态核外电子排布式为 .
(2)(CN)2分子中碳原子杂化轨道类型为;1mol(CN)2分子中含有σ键的数目为 .
(3)O ![]() 与CN﹣互为等电子体,则O
与CN﹣互为等电子体,则O ![]() 的电子式为 .
的电子式为 .
(4)Fe3C的晶胞结构中碳原子的配位数为6,碳原子与紧邻的铁原子组成的空间构型为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 同温同压下,等质量的甲烷比氖气所占有的体积小
B. 3.01×1023个X气体分子的质量为16g,则X气体的摩尔质量是64 g mol-1
C. 0.5L 1 molL-1 FeCl3溶液与0.2L 1 molL-1 KCl溶液中的Cl—的数目之比为15: 2
D. 150ml 1 molL-1NaCl溶液与50ml 1 molL-1AlCl 3溶液中Cl—物质的量浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)在食品加工中常用作防腐剂、漂白剂和疏松剂.焦亚硫酸钠为黄色结晶粉末,150℃时开始分解,在水溶液或含有结晶水时更易被空气氧化.实验室制备焦亚硫酸钠过程中依次包含以下几步反应:
2NaOH+SO2=Na2SO3+H2O …(a)
Na2SO3+H2O+SO2=2NaHSO3…(b)
2NaHSO3 ![]() Na2S2O5+H2O …(c)
Na2S2O5+H2O …(c)
实验装置如下: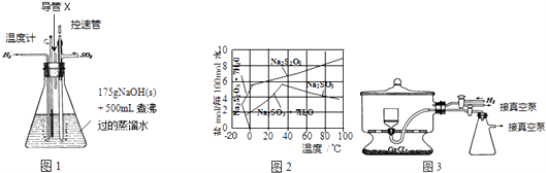
(1)实验室可用废铝丝与NaOH溶液反应制取H2 , 制取H2的离子方程式为 .
(2)图1装置中,导管X的作用是 .
(3)通氢气一段时间后,以恒定速率通入SO2 , 开始的一段时间溶液温度迅速升高,随后温度缓慢变化,溶液开始逐渐变黄.“温度迅速升高”的原因为;
实验后期须保持温度在约80℃,可采用的加热方式为 .
(4)反应后的体系中有少量白色亚硫酸钠析出,参照图2溶解度曲线,除去其中亚硫酸钠固体的方法是;然后获得较纯的无水Na2S2O5应将溶液冷却到30℃左右抽滤,控制“30℃左右”的理由是 .
(5)用图3装置干燥Na2S2O5晶体时,通入H2的目的是;真空干燥的优点是 .
(6)测定产品中焦亚硫酸钠的质量分数常用剩余碘量法.已知:S2O52﹣+2I2+3H2O=2SO42﹣+4I﹣+6H+;2S2O32﹣+I2=S4O62﹣+2I﹣
请补充实验步骤(可提供的试剂有:焦亚硫酸钠样品、标准碘溶液、淀粉溶液、酚酞溶液、标准Na2S2O3溶液及蒸馏水).
①精确称取产品0.2000g放入碘量瓶(带磨口塞的锥形瓶)中.
②准确移取一定体积和已知浓度的标准碘溶液(过量)并记录数据,在暗处放置5min,然后加入5mL冰醋酸及适量的蒸馏水.
③用标准Na2S2O3溶液滴定至接近终点.
④ .
⑤ .
⑥重复步骤①~⑤;根据相关记录数据计算出平均值.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含K+、Al3+、NH4+、SO42﹣ . 取500mL该溶液加入过量的氢氧化钡溶液,经过滤、洗涤、干燥,称重得到9.32g固体1,并收集到224mL(标准状况)气体.在滤液中通入过量的CO2 , 经过滤、洗涤、灼烧,称重得到0.51g固体2.原溶液中K+的浓度为( )
A.0.08mol/L
B.0.04mol/L
C.0.02mol/L
D.0.01mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于“甲烷的存在与用途”的叙述不正确的是( )
A. 我国的天然气主要分布在中西部地区及海底
B. 可燃冰是天然气的水合物,外形似冰,易燃烧
C. 甲烷俗称“天然气”,常用作燃料
D. 天然气和沼气都是理想的清洁能源
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com