
【题目】氯苯是重要的有机化工产品,是染料、医药、有机合成的中间体,工业上常用“间歇法”制取。反应原理、实验装置图(加热装置都已略去)如下:![]() +Cl2
+Cl2![]()
![]() +HCl
+HCl 
已知:氯苯为无色液体,沸点132.2 ℃。
回答下列问题:
(1)A反应器是利用实验室法制取氯气,中空玻璃管B的作用是______。
(2)把干燥的氯气通入装有干燥苯的反应器C中(内有相当于苯量1%的铁屑作催化剂),加热维持反应温度在40~60 ℃为宜,温度过高会生成二氯苯。
①对C加热的方法是________(填字母)。
a.酒精灯加热 b.油浴加热 c.水浴加热
②D出口的气体成分有HCl、________和________。
(3)C反应器反应完成后,工业上要进行水洗、碱洗及食盐干燥,才能蒸馏。碱洗之前要水洗的目的是洗去部分无机物,同时减少碱的用量,节约成本。写出用10%氢氧化钠碱洗时可能发生的化学反应方程式:_____________、__________(写两个即可)。
(4)上述装置图中A、C反应器之间,需要增添一个U形管,其内置物质是________。
(5)工业生产中苯的流失情况如下:
项目 | 二氯苯 | 尾气 | 不确定苯耗 | 流失总量 |
苯流失量(kg·t-1) | 13 | 24.9 | 51.3 | 89.2 |
则1 t苯可制得成品为________t(只要求列式)。
【答案】平衡气压 c Cl2 苯蒸气 HCl+NaOH=NaCl+H2O FeCl3+3NaOH=Fe(OH)3↓+3NaCl 五氧化二磷(或氯化钙) ![]()
【解析】
(1)玻璃管B伸入液面下,装置内压强过大时,可以用于平衡气压;
(2)①反应器C加热控制反应温度在40~60℃,应利用水浴加热,故合理选项是c;
②由于苯沸点低,易挥发,反应产生的HCl气体及还有未反应的氯气都可以从D出口逸出,故D出口气体中含有HCl、苯蒸气、氯气;
(3)该反应的催化剂氯化铁可以与加入的碱溶液中的氢氧化钠反应,生成HCl也会与氢氧化钠反应,溶解的氯气也会与去氧化钠反应,反应方程式为:FeCl3+3NaOH=Fe(OH)3↓+3NaCl、HCl+NaOH=NaCl+H2O、Cl2+2NaOH=NaCl+NaClO+H2O;
(4)A、C反应器之间需要增添U型管,用来干燥生成的氯气,由于氯气可以与碱性物质反应,所以干燥氯气可以用五氧化二磷或氯化钙等;
(5)苯的总流失量为89.2kg/t,故1t苯中参加反应的苯的质量为(1t-0.0892t),由苯与氯苯质量之比为78:112.5,可知生成氯苯质量为m(氯苯)=![]() t。
t。


科目:高中化学 来源: 题型:
【题目】298K(25℃)下,在NaHS溶液中,各离子的浓度随NaHS溶液浓度的变化关系如图所示,下列叙述正确的是
已知:(1)在科学计数法中,为了使公式简便,可以用带“E”的格式表示,例如:1E-4=1×10-4。
(2)298K(25℃)下H2S的Ka1=9.10×10-8,Ka2=1.10×10-12。
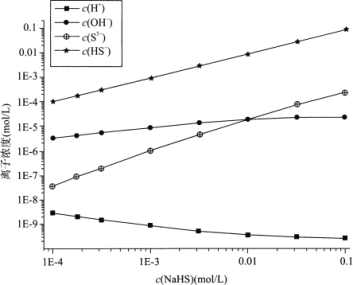
A. 0.10mol/LNaHS溶液:c(Na+)>c(HS-)>c(OH-)>c(S2-)
B. Na2S溶液中:c(OH-)-c(H+)=c(H2S)+c(HS-)
C. 当c(OH-)=c(S2-)时,c(HS-)=9.09×10-3
D. 室温下用NaOH溶液滴定NaHS溶液,滴定终点刚好形成0.1mol/LNa2S溶液,该过程可选择酚酞作指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,1mol化学键断裂形成气态原子所需要的能量用![]() 表示。结合表中信息判断下列说法不正确的是( )
表示。结合表中信息判断下列说法不正确的是( )
共价键 | H-H | F-F | H-F | H-Cl | H-I |
E(kJ/mol) | 436 | 157 | 568 | 432 | 298 |
A. 432kJ/mol>E(H-Br)>298kJ/mol B. 表中最稳定的共价键是H-F键
C. H2(g)→2H(g) △H=+436kJ/mol D. H2(g)+F2(g)=2HF(g) △H=-25kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国产航母001A等舰艇的船底都涂有含Cu2O的防污涂料,制备Cu2O的一种方法为:Zn+2CuSO4+2NaOH===Cu2O+ZnSO4+Na2SO4+H2O。该反应的下列说法正确的是( )

A. Zn得到电子
B. CuSO4被氧化
C. NaOH是还原剂
D. CuSO4是氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示(部分物质和条件己略去)。A是由两种元素组成的难溶于水的物质,摩尔质量为88 g·mol-l;B是常见的强酸;C是一种气态氢化物;气体E能使带火星的木条复燃;F是最常见的无色液体;无色气体G能使品红溶液褪色;向含有I的溶液中滴加KSCN试剂,溶液出现血红色。请回答下列问题:

(1)G的化学式为_________________________。
(2)C的电子式为________________________。
(3)写出反应①的离子方程式:_____________________。
(4)写出反应②的化学方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行如下反应3A(g)+2B(g) ![]() 4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是( )
4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是( )
A. 该反应的化学平衡常数表达式是![]()
B. 此时,B的平衡转化率是40%
C. 增大该体系的压强,化学平衡常数增大
D. 增加B,B的平衡转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2(g)+O2(g)===2H2O(l) ΔH=-571.6kJ·mol-1
CO(g)+1/2O2(g)===CO2(g) ΔH=-282.8kJ·mol-1
现有CO、H2、CO2组成的混合气体67.2L(标准状况),经完全燃烧后放出的总热量为710.0kJ,并生成18g液态水,则燃烧前混合气体中CO的体积分数为( )
A. 80% B. 50% C. 60% D. 20%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com