
،¾جâؤ؟،؟ءھ°±£¨N2H4£©¼°ئنرـةْخïتاز»ہàضطزھµؤ»ً¼ب¼ءد£¬N2H4سëN2O4ؤـ·إ³ِ´َء؟µؤبب،£
£¨1£©زرضھ£؛2NO2(g)£½N2O4(g) ،÷H£½£57.20kJ،¤mol£1،£ز»¶¨خآ¶بدآ£¬شعأـ±صبفئ÷ضذ·´س¦2NO2(g)£½N2O4(g) ´ïµ½ئ½؛â،£ئنثüجُ¼²»±نت±£¬دآءذ´ëت©£؛
A£®¼ُذ،NO2µؤإ¨¶ب B£®½µµحخآ¶ب C£®شِ¼سNO2µؤإ¨¶ب D£®ة¸كخآ¶ب
ؤـجل¸كNO2×ھ»¯آتµؤتا_______£¨جî×ضؤ¸£©،£
£¨2£©25،وت±£¬1.00gN2H4(l)سë×مء؟N2O4(l)حêب«·´س¦ةْ³ةN2(g)؛حH2O (l) £¬·إ³ِ19.14kJ
µؤببء؟،£شٍ·´س¦2N2H4(l)+N2O4(l)£½3N2(g)+4H2O (l)µؤ،÷H£½______kJ،¤mol£1،£
£¨3£©17،و،¢1.01،ء105Pa£¬أـ±صبفئ÷ضذN2O4؛حNO2µؤ»ى؛دئّجه´ïµ½ئ½؛âت±£¬c(NO2)£½0.0300mol،¤L£1،¢c(N2O4)£½0.0120mol،¤L£1،£¼ئثم·´س¦2 NO2(g)![]() N2O4(g)µؤئ½؛â³£تK=______،£
N2O4(g)µؤئ½؛â³£تK=______،£
£¨4£©دضسأز»¶¨ء؟µؤCu سë×مء؟µؤإ¨HNO3·´س¦£¬ضئµأ1.00Lزر´ïئ½؛âµؤN2O4؛حNO2
»ى؛دئّجه£¨17،و،¢1.01،ء105Pa£©£¬ہيآغةدضءةظذèدû؛ؤCuµؤضتء؟تا________،£
،¾´ً°¸،؟BC £1224.96 13.3 1.73g
،¾½âخِ،؟
£¨1£©سةسع¸أ·´س¦خھئّجهجه»¼ُذ،µؤ·إبب·´س¦£¬زھجل¸كNO2×ھ»¯آت£¬شٍس¦¸أ²ةب،£؛¢ظ½µµحخآ¶ب£»¢عشِ¼سNO2µؤإ¨¶ب£»¢غشِ´َر¹ا؟µب´ëت©،£ثùزشB،¢C·û؛دزھاَ£»
£¨2£©سة1.00gN2H4(l)·إ³ِ19.14kJ£¬شٍ2mol(¼´64g)N2H4(l)·إببخھ1224.96kJ£¬ثùزش،÷H£½1224.96kJ،¤mol£1،£
£¨3£©،¢¸ù¾فجâزâضھ£¬ئ½؛âت±c(N2O4)£½0.0120mol،¤L£1،¢c(NO2)£½0.0300mol،¤L£1£¬K£½c(N2O4)/c2(NO2) £½0.0120/0.0300،ء0.0300 £½13.3،£
£¨4£©سة£¨3£©؟ةضھ£¬شع17،و،¢1.01،ء105Pa´ïµ½ئ½؛âت±£¬1.00L»ى؛دئّجهضذ£¬n(N2O4)£½c(N2O4)،ءV£½0.0120mol،¤L£1،ء1.00L£½0.0120mol£¬n(NO2)£½c(NO2)،ءV£½0.0300mol،¤L£1،ء1.00L£½0.0300mol£¬شٍn×ـ(NO2)£½n(NO2)£«2،ءn(N2O4)£½0.0540mol£¬سةCu£«4HNO3£½Cu(NO3)2£«2NO2،ü£«2H2O؟ةµأ£؛m(Cu)£½ 64g،¤mol£1،ء0.0540mol/2 £½1.73g،£


 µ¼ر§سë²âتشدµءذ´ً°¸
µ¼ر§سë²âتشدµءذ´ً°¸ ذآ·ا·²½ج¸¨³ه´ج100·ضدµءذ´ً°¸
ذآ·ا·²½ج¸¨³ه´ج100·ضدµءذ´ً°¸
| ؤ꼶 | ¸كضذ؟خ³ج | ؤ꼶 | ³ُضذ؟خ³ج |
| ¸كز» | ¸كز»أâ·ر؟خ³جحئ¼ِ£، | ³ُز» | ³ُز»أâ·ر؟خ³جحئ¼ِ£، |
| ¸ك¶ | ¸ك¶أâ·ر؟خ³جحئ¼ِ£، | ³ُ¶ | ³ُ¶أâ·ر؟خ³جحئ¼ِ£، |
| ¸كب | ¸كبأâ·ر؟خ³جحئ¼ِ£، | ³ُب | ³ُبأâ·ر؟خ³جحئ¼ِ£، |
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟£¨1£©زرضھ²ً؟ھ1molH-H¼ü,1molN-H¼ü,1mol![]() ¼ü·ض±ًذèزھµؤؤـء؟تا436kJ،¢391kJ،¢946kJ,شٍN2سëH2·´س¦ةْ³ةNH3µؤبب»¯ر§·½³جت½خھ________،£
¼ü·ض±ًذèزھµؤؤـء؟تا436kJ،¢391kJ،¢946kJ,شٍN2سëH2·´س¦ةْ³ةNH3µؤبب»¯ر§·½³جت½خھ________،£
£¨2£©شع2A+B![]() 2C+D·´س¦ضذ,±يت¾¸أ·´س¦×î؟ىµؤتا_____(جîذ´×ضؤ¸ذٍ؛إ)،£
2C+D·´س¦ضذ,±يت¾¸أ·´س¦×î؟ىµؤتا_____(جîذ´×ضؤ¸ذٍ؛إ)،£
a. v(A)=0.8molL-1s-1
b. v(B)=0.3molL-1s-1
c. v(C)=0.6molL-1s-1
d.v(D)=0.5molL-1s-1
£¨3£©90،وت±,amolL-1ز»شھثلHAسëbmolL-1NaOHبـز؛µبجه»»ى؛د؛َ,»ى؛دز؛µؤpHخھ7,شٍبـز؛ضذثùسذہë×سµؤإ¨¶بسة´َµ½ذ،µؤث³ذٍتا________،£
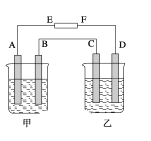
£¨4£©شعبçح¼ضذ£¬¼×ةص±ضذت¢سذ100 mL 0.50 molL£1 AgNO3بـز؛£¬ززةص±ضذت¢سذ100 mL 0.25 molL£1 CuCl2بـز؛£¬A،¢B،¢C،¢D¾ùخھضتء؟دàح¬µؤت¯ؤ«µç¼«£¬بç¹ûµç½âز»¶خت±¼ن؛َ£¬·¢دضA¼«±بC¼«ضط0.19 g£¬شٍµçش´Eخھ________¼«£¬A¼«µؤµç¼«·´س¦ت½خھ_______£¬D¼«خِ³ِئّجه________ mL(±ê×¼×´؟ِ)،£
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟×î½üزâ´َہû؟ئر§¼ز»ٌµأءث¼«¾كہيآغرذ¾؟زâزهµؤN4·ض×س،£N4·ض×س½ل¹¹بçح¼ثùت¾£¬زرضھ¢ٌ،¢¶دءر1 mol N،ھNخüتص167 kJببء؟£¬ذخ³ة1 mol ![]() ·إ³ِ942 kJببء؟£»¢ٍ،¢N2(g)£«3H2(g)
·إ³ِ942 kJببء؟£»¢ٍ،¢N2(g)£«3H2(g)![]() 2NH3(g) ¦¤H1£½£92 kJ/mol£¬N4(g)£«6H2(g)
2NH3(g) ¦¤H1£½£92 kJ/mol£¬N4(g)£«6H2(g)![]() 4NH3(g) ¦¤H2(kJ/mol)¸ù¾فزشةدذإد¢؛حت¾ف£¬دآءذثµ·¨صب·µؤتا(،،،،)
4NH3(g) ¦¤H2(kJ/mol)¸ù¾فزشةدذإد¢؛حت¾ف£¬دآءذثµ·¨صب·µؤتا(،،،،)

A.¦¤H2£¾0B.N2·ض×س±بN4·ض×سخب¶¨
C.¦¤H2£½2¦¤H1D.¦¤H2سë·½³جت½دµتخق¹ط
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟ؤ³·´س¦ضذ·´س¦خïسëةْ³ةخïسذ£؛AsH3،¢H2SO4،¢![]() ،¢H3AsO4،¢H2O؛حز»ضضخ´ضھخïضتX،£
،¢H3AsO4،¢H2O؛حز»ضضخ´ضھخïضتX،£
£¨1£©زرضھ![]() شع·´س¦ضذµأµ½µç×س£¬شٍ¸أ·´س¦µؤ»¹ش¼ءتا______________،£
شع·´س¦ضذµأµ½µç×س£¬شٍ¸أ·´س¦µؤ»¹ش¼ءتا______________،£
£¨2£©زرضھ0.2mol![]() شع·´س¦ضذµأµ½1molµç×سةْ³ةX£¬شٍXµؤ»¯ر§ت½خھ_____________،£
شع·´س¦ضذµأµ½1molµç×سةْ³ةX£¬شٍXµؤ»¯ر§ت½خھ_____________،£
£¨3£©¸ù¾فةدتِ·´س¦؟ةحئضھ_________،£
a£®رُ»¯ذش£؛![]() b£®رُ»¯ذش£؛
b£®رُ»¯ذش£؛![]()
c£®»¹شذش£؛![]() d£®»¹شذش£؛
d£®»¹شذش£؛![]()
£¨4£©½«رُ»¯¼ء؛ح»¹ش¼ءµؤ»¯ر§ت½¼°ئنإنئ½؛َµؤدµتجîبëدآءذ·½؟ٍضذ£¬²¢±ê³ِµç×س×ھزئµؤ·½
دٍ؛حتؤ؟£؛ ___________،£
___________،£
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟2SO2(g)+O2(g)![]() 2SO3(g)·´س¦¹³جضذµؤؤـء؟±ن»¯بçح¼ثùت¾£¨ح¼ضذE1±يت¾خق´ك»¯¼ءت±ص·´س¦µؤ»î»¯ؤـ£¬E2±يت¾خق´ك»¯¼ءت±ؤو·´س¦µؤ»î»¯ؤـ£©،£دآءذسذ¹طذًتِ²»صب·µؤتا
2SO3(g)·´س¦¹³جضذµؤؤـء؟±ن»¯بçح¼ثùت¾£¨ح¼ضذE1±يت¾خق´ك»¯¼ءت±ص·´س¦µؤ»î»¯ؤـ£¬E2±يت¾خق´ك»¯¼ءت±ؤو·´س¦µؤ»î»¯ؤـ£©،£دآءذسذ¹طذًتِ²»صب·µؤتا

A. ¸أ·´س¦µؤؤو·´س¦خھخüبب·´س¦£¬ة¸كخآ¶ب؟ةجل¸ك»î»¯·ض×سµؤ°ظ·ضت
B. 500،و،¢101kPaدآ£¬½«1molSO2(g)؛ح0.5molO2(g)ضأسعأـ±صبفئ÷ضذ³ن·ض·´س¦ةْ³ةSO3(g)·إببakJ£¬ئنبب»¯ر§·½³جت½خھ2SO2(g)+O2(g)![]() 2SO3(g) ¦¤H=-2a kJ،¤mol-l
2SO3(g) ¦¤H=-2a kJ،¤mol-l
C. ¸أ·´س¦ضذ£¬·´س¦خïµؤ×ـ¼üؤـذ،سعةْ³ةخïµؤ×ـ¼üؤـ
D. ¦¤H=E1-E2£¬ت¹سأ´ك»¯¼ء¸ؤ±ن»î»¯ؤـ£¬µ«²»¸ؤ±ن·´س¦بب
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟زرضھA،ھO·ض±ً´ْ±يز»ضضخïضت£¬ثüأاض®¼نµؤ×ھ»¯¹طدµبçدآح¼ثùت¾£¨·´س¦جُ¼آش£©،£A،¢B،¢H·ض±ًتاسة¶جضـئعشھثط×é³ةµؤµ¥ضت،£Bسëہنث®»؛آ·´س¦£¬سë·ذث®ر¸ثظ·´س¦£¬·إ³ِاâئّ،£Dتاز»ضضہë×س»¯؛دخئنزُرôہë×سµؤ¸ِت±بخھ2£؛3£¬ازؤـسëث®·´¾حس¦µأµ½ء½ضض¼î،£Cخھµ»ئة«¹ججه»¯؛دخOؤـسëGµؤث®بـز؛·´س¦ةْ³ةہ¶ة«³ءµي،£اë»ط´ًدآءذختجâ£؛
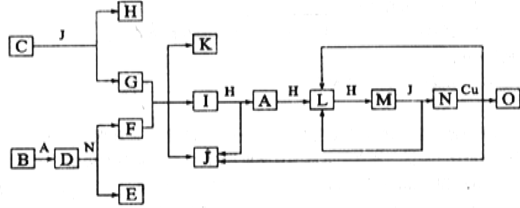
¢إ×é³ةBµ¥ضتµؤشھثطخ»سعضـئع±يخ»ضأ________________،£»¯؛دخïCµç×ست½خھ____________،£
¢ئJµؤبغ·ذµم±بخّ»¯ا⣨H2Se£©µؤبغ·ذµم¸ك£¬ئنشزٍتا_________________،£
¢اIسëHشعز»¶¨جُ¼دآز²؟ةض±½س·´س¦ةْ³ةL؛حJ, ذ´³ِ»¯ر§·½³جت½£؛_______________،£
¢بذ´³ِDسëث®·´س¦µؤ»¯ر§·½³جت½£؛_____________________،£
¢ة؛ى×طة«خغب¾ئّجهMµؤ´¦ہي¾كسذتµ¼تزâزه،£دضشع³£ہûسأ·´س¦![]() £¨·½³جأ»إنئ½£©ہ´´¦ہيM،£µ±×ھزئ0.4molµç×ست±£¬دû؛ؤµؤMشع±ê×¼×´؟ِدآتا_______L،£
£¨·½³جأ»إنئ½£©ہ´´¦ہيM،£µ±×ھزئ0.4molµç×ست±£¬دû؛ؤµؤMشع±ê×¼×´؟ِدآتا_______L،£
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟ةéAsتاµعثؤضـئع¢ُA×هشھثط£¬؟ةزشذخ³ة As2S3،¢As2O5،¢H3AsO3،¢H3AsO4µب »¯؛دخسذ×إ¹م·؛µؤسأح¾»ط´ًدآءذختجâ£؛
£¨1£©ذ´³ِةéµؤش×سذٍت______________
£¨2£©¹¤زµةد³£½«؛¬ةé·دشüض÷زھ³ة·ضخھAs2S3ضئ³ة½¬×´£¬ح¨بëO2رُ»¯£¬ةْ³ةH3AsO4؛حµ¥ضتءٍ,ذ´³ِ·¢ةْ·´س¦µؤ»¯ر§·½³جت½___________;¸أ·´س¦ذèزھشع¼سر¹دآ½ّذذ£¬شزٍتا___________.
£¨3£©زرضھ£؛As£¨s£©+ ![]() H2£¨g£©+2O2£¨g£©=H3AsO4£¨s£©،÷H1
H2£¨g£©+2O2£¨g£©=H3AsO4£¨s£©،÷H1
H2£¨g£©+![]() O2£¨g£©=H2O£¨l£©،÷H2
O2£¨g£©=H2O£¨l£©،÷H2
2As£¨s£©+![]() O2£¨g£©=As2O5£¨s£©،÷H3
O2£¨g£©=As2O5£¨s£©،÷H3
شٍ·´س¦As2O5£¨s£©+3H2O£¨l£©=2H3AsO4£¨s£©µؤ،÷H =___________
£¨4£©298Kت±£¬½«20mL 3x molL-1 Na3AsO3،¢20mL 3x molL-1 I2؛ح20mL NaOHبـز؛»ى؛د£¬·¢ةْ·´س¦£؛AsO33-£¨aq£©+I2£¨aq£©+2OH-AsO43-£¨aq£©+2I-£¨aq£©+H2O£¨l£©،£بـز؛ضذc£¨AsO43-£©سë·´س¦ت±¼ن£¨t£©µؤ¹طدµبçح¼ثùت¾،£

¢ظدآءذ؟ةإذ¶د·´س¦´ïµ½ئ½؛âµؤتا ______ جî±ê؛إ£®
a .بـز؛µؤpH²»شظ±ن»¯ b. v£¨I-£©=2v£¨AsO33-£©
c .c £¨AsO43-£©/c £¨AsO33-£©²»شظ±ن»¯ d. c£¨I-£©=ymolL-1
¢عtmت±vص_____vؤو£¨جî،°´َسع،±،°ذ،سع،±»ٍ،°µبسع،±£©،£
¢غtmت±vؤو_____ tnت±vص£¨جî،°´َسع،±،°ذ،سع،±»ٍ،°µبسع،±£©ہيسةتا _____
¢ـبôئ½؛âت±بـز؛c(OH-)=1 mol/L£¬شٍ¸أ·´س¦µؤئ½؛â³£تKخھ ______________
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟سزح¼خھتµرéتزضئب،ززثلززُ¥µؤ×°ضأ،£

اë»ط´ً£؛
£¨1£©¼ىرé¸أ×°ضأئّأـذشµؤ·½·¨تا_________________________________،£
£¨2£©إ¨ءٍثلµؤ×÷سأتا__________________،£
£¨3£©دآءذسذ¹ط¸أتµرéµؤثµ·¨ضذ£¬صب·µؤتا________،£
A£®دٍaتش¹ـضذ¼سبë·ذت¯£¬ئن×÷سأتا·ہض¹¼سببت±ز؛جه±¬·ذ
B£®±¥؛حج¼ثلؤئبـز؛؟ةزش³ب¥²ْخïضذ»ىسذµؤززثل
C£®ززثلززُ¥تاز»ضضخقة«ح¸أ÷،¢أـ¶ب±بث®´َµؤسح×´ز؛جه
D£®بôشءدخھCH3COOH؛حCH3CH218OH£¬شٍززثلززُ¥ضذ²»؛¬18O
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟¸كآ¯ء¶جْضذ·¢ةْµؤ»ù±¾·´س¦ض®ز»بçدآ£؛
FeO£¨¹ج£©£«CO£¨ئّ£©Fe£¨¹ج£©£«CO2£¨ئّ£©¦¤H£¾0
£¨1£©شٍ¸أ·´س¦ضذئ½؛â³£ت±ي´ïت½K£½_________________
£¨2£©زرضھ1100،وت±K£½0.263،£خآ¶بة¸ك£¬»¯ر§ئ½؛âزئ¶¯؛َ´ïµ½ذآµؤئ½؛⣬¸كآ¯ؤعCO2؛حCOµؤجه»±بضµ_______ئ½؛â³£تKضµ___£¨¾ùجîشِ´َ£¬¼ُذ،»ٍ²»±ن£©.
£¨3£©1100،وت±²âµأ¸كآ¯ضذc(CO2)£½0.025mol،¤L£1£¬c(CO)£½0.1mol،¤L£1£¬شعصâضضاé؟ِدآ£¬¸أ·´س¦تا·ٌ´¦سعئ½؛â×´ج¬________£¨ر،جîتا»ٍ·ٌ£©£¬´ثت±»¯ر§·´س¦ثظآتvص____vؤو£¨ر،ج£¬£¼£¬£½£©،£
²é؟´´ً°¸؛ح½âخِ>>
¹ْ¼تر§ذ£سإر، - ء·د°²لءذ±ي - تشجâءذ±ي
؛±±ت،»¥ءھحّخ¥·¨؛ح²»ء¼ذإد¢¾ظ±¨ئ½ج¨ | حّةدسذ؛¦ذإد¢¾ظ±¨×¨اّ | µçذإص©ئ¾ظ±¨×¨اّ | ةوہْت·ذéخقض÷زهسذ؛¦ذإد¢¾ظ±¨×¨اّ | ةوئَاضب¨¾ظ±¨×¨اّ
خ¥·¨؛ح²»ء¼ذإد¢¾ظ±¨µç»°£؛027-86699610 ¾ظ±¨ستدن£؛58377363@163.com