
����Ŀ��ͼ������ʵ���ҽ��а��������Ʊ�������̽��ʵ������װ�ã����̶ֹ�װ��δ������
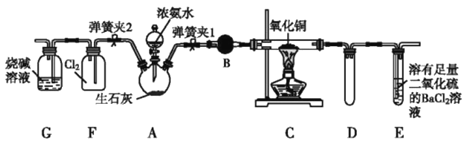
(1)����װ��װ�ú���Ҫ����A~Eװ�õ������ԣ�������ǣ�����______________�����ɼ�1����E��װ��ˮ��Ȼ����A���۲쵽E��������ð�����ƿ��ƾ��ƣ�E�е�����ˮ���γɣ�˵��װ�����������á�
(2)װ��B��ʢ�ŵ��Լ���______________________��
(3)��ȼC���ƾ��ƣ��رյ��ɼ�2�����ɼ�1���ӷ�Һ©���ų�Ũ��ˮ����û��ƿ�й���رշ�Һ©���������Ե�Ƭ�̣�װ��C�к�ɫ������죬װ��E����Һ����ִ������ݣ�ͬʱ����_____________(������)����E���ݳ�Һ����������ֱ�����������д��C�з�Ӧ�Ļ�ѧ����ʽ��_______��
(4)��C�й���ȫ�����ɫ�رյ��ɼ�1�������ƿ��ƾ��ƣ�����ȴ����C�й�������������Ӧǰ��������Ϊ16 g����Ӧ�������������2.4 g��ͨ������ȷ���ù������Ļ�ѧʽ��______��
(5)�ڹرյ��ɼ�1���ɼ�2�������������F�У��ܿ췢��װ��F�в������̣�ͬʱ����G����ҺѸ�ٵ�������F�С�д���������̵Ļ�ѧ����ʽ��_____��
���𰸡��رյ��ɼ�2�ͷ�Һ©������ ��ʯ��(����ʯ��) ��ɫ���� 2NH3+3CuO![]() N2+3H2O+3Cu Cu2O��Cu 3Cl2+8NH3�TN2+6NH4Cl
N2+3H2O+3Cu Cu2O��Cu 3Cl2+8NH3�TN2+6NH4Cl
��������
(1)����װ��A~E�������ԣ�Ҫ��ֹ�������F��
(2)װ��B�������Ǹ��ﰱ����
(3) װ��C�к�ɫ������죬��E���ݳ�Һ����������ֱ������գ�˵������ͭ�백����Ӧ����ͭ��������ˮ��û��Ӧ�İ�������E��ʹ��Һ�ʼ��ԣ����������ᱵ������
(4)����ͭԪ���غ��������Ļ�ѧʽ��
(5) װ��F�в������̣�˵�����Ȼ�����ɣ���֪F�������백����Ӧ�����Ȼ�狀͵�����
(1). �رյ��ɼ�2�ͷ�Һ©�����������ɼ�1����E��װ��ˮ��Ȼ����A���۲쵽E��������ð�����ƿ��ƾ��ƣ�E�е�����ˮ���γɣ�˵��װ�����������ã�
(2)װ��B�������Ǹ��ﰱ��������B��ʢ�ŵ��Լ��Ǽ�ʯ�ң�
(3) װ��C�к�ɫ������죬��E���ݳ�Һ����������ֱ������գ�˵������ͭ�백����Ӧ����ͭ��������ˮ����Ӧ����ʽ��2NH3+3CuO ![]() N2+3H2O+3Cu��û��Ӧ�İ�������E��ʹ��Һ�ʼ��ԣ����������ᱵ������E�е��������а�ɫ�������ɡ�
N2+3H2O+3Cu��û��Ӧ�İ�������E��ʹ��Һ�ʼ��ԣ����������ᱵ������E�е��������а�ɫ�������ɡ�
(4)��Ӧǰn(CuO)=![]() 0.2 mol����n(Cu)=0.2 mol��n(O)=0.2 mol����Ӧ�����У�ͭԪ�����ʵ������䣬��Ԫ�����ʵ������٣���Ӧ�������������2.4 g���������Ԫ�ص����ʵ�����
0.2 mol����n(Cu)=0.2 mol��n(O)=0.2 mol����Ӧ�����У�ͭԪ�����ʵ������䣬��Ԫ�����ʵ������٣���Ӧ�������������2.4 g���������Ԫ�ص����ʵ�����![]() =0.15mol��ʣ�������n(Cu)��n(O)=0.2:0.05=4:1��2:1�����Ըù������Ļ�ѧʽΪCu2O��Cu��
=0.15mol��ʣ�������n(Cu)��n(O)=0.2:0.05=4:1��2:1�����Ըù������Ļ�ѧʽΪCu2O��Cu��
(5)װ��F�������백����Ӧ�����Ȼ�狀͵�������Ӧ����ʽ��3Cl2+8NH3�TN2+6NH4Cl��


 ��������ѧ����ϵ�д�
��������ѧ����ϵ�д� ��Ԫ������ĩ��ϵ�д�
��Ԫ������ĩ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£���A��B��0.32 mol����10 L�ĺ����ܱ������У��������·�Ӧ��A(s)+B(g)![]() 2C(g) ��H<0����Ӧ�����вⶨ�����������������˵����ȷ����
2C(g) ��H<0����Ӧ�����вⶨ�����������������˵����ȷ����
t/min | 0 | 2 | 4 | 7 | 9 |
n(B)/mol | 0.32 | 0.24 | 0.22 | 0.20 | 0.20 |
A.��Ӧǰ2 min��ƽ����Ӧ����v(C)=0.004 mol/(L��min)
B.�����������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰ��v(��)>v(��)
C.�����������䣬��ʼʱ�������г����0.64 mol��A��B��ƽ��ʱn(C)<0.48 mol
D.�����������䣬��ƽ����ϵ���ٳ���0.32 mol B��0.16 mol C���ٴﵽƽ��ʱ��A��ת��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijУ��ѧ��ȤС������ͼ��ʾ���̳�ȥAlCl3��Һ�к��е�Mg2����K���������Ӳ������ܼ���AlCl3����ʧ��
 ������˵����ȷ����(����)
������˵����ȷ����(����)
A. NaOH��Һ�����ð�ˮ������
B. ��Һa�к���Al3����K����Cl����Na����OH��
C. ��Һb��ֻ����NaCl
D. ����Һa�еμ������������Һ��pH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ǿ����ʵĻ����Һ10 L�����п��ܺ���K+��Ba2+��Na+��NH4+��Cl-��SO42-��AlO2-��OH-�еļ��֣�������ͨ��CO2���壬��������������ͨ��CO2����֮��Ĺ�ϵ��ͼ��ʾ������˵����ȷ����( )

A.CD�ε����ӷ���ʽ���Ա�ʾΪ��CO32-+CO2+H2O�T2HCO3-
B.�϶������ڵ�������SO42-��OH-
C.����Һ����ȷ�����ڵ�������Ba2+��AlO2-��NH4+
D.OA�η�Ӧ�����ӷ���ʽ��2AlO2-+CO2+3H2O�T2Al(OH)3��+CO32-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2mol�����ƺ�1mol������Ӧ��������ϵ��ͼ��ʾ������˵������ȷ�ģ� ����
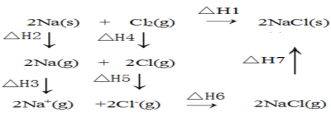
A.��H2+��H3+��H4+��H5+��H6+��H7=��H1
B.��H4��ֵ��ֵ�Ϻ�Cl-Cl���ۼ��ļ������
C.��H5��0������ͬ�����£�2Br��g������H5������H5
D.��H7��0���Ҹù����γ����Ӽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�����£�ϡ��![]() ��HClO�������ϡ��Һʱ����ҺpH���ˮ���ı仯������˵����ȷ����
��HClO�������ϡ��Һʱ����ҺpH���ˮ���ı仯������˵����ȷ����![]()

A.��ͬŨ�ȵ�![]() ��NaClO�Ļ����Һ�У�������Ũ�ȵĴ�С��ϵ�ǣ�
��NaClO�Ļ����Һ�У�������Ũ�ȵĴ�С��ϵ�ǣ�![]()
B.��Ũ�ȵ������![]() ��NaClO������Һ�У������ӵ������ʵ���ǰ��С�ں���
��NaClO������Һ�У������ӵ������ʵ���ǰ��С�ں���
C.ͼ��a��b�����Ӧ��������ʵ���Ũ��![]()
D.ͼ��a��c�������Һ�� ���
���![]() ����
����![]() ��
��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������K2CO3��Һ�л����صμ�ϡ���ᣬ�����Ͻ��衣��������ļ��룬��Һ��������ĿҲ��Ӧ�ط����仯����ͼ��ʾ��������������Һ�е�������Ŀ�Ķ�Ӧ��ϵ����ȫ��ȷ����( )
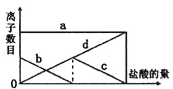
A. a��K+�� b��HCO3����c��CO32����d��Cl��
B. a��K+�� b��CO32����c��HCO3����d��Cl��
C. a��K+�� b��CO32����c��Cl����d��HCO3��
D. a��K+�� b��HCO3����c��Cl����d��CO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��SO2�ĺ����ǿ��������ձ���һ����Ҫ���ָ�꣬Ҳ���������������Ű�ҹ��ֵ�������Ҫԭ��֮һ���Ӵ�SO2�Ĵ������ȣ�������������Ⱦ�ĵ���֮����
I���绯ѧ������SO2��
���Ṥҵβ���е�SO2������������Ʊ����ᣬͬʱ��õ��ܣ�װ������ͼ��ʾ���缫��Ϊ���Բ��ϣ���

��1��M�������ĵ缫��ӦʽΪ________________��
��2����ʹ��װ�õĵ���ǿ�ȴﵽ2��0A��������ÿ����Ӧ��ͨ���״������������Ϊ________L����֪��1��e-��������Ϊ1.6��10-19C����
��.��Һ��绯ѧ�ۺϣ��Ƽ�ѭ����������SO2��
��3���Ƽ�ѭ�����У���Na2SO3��Һ��Ϊ����Һ������SO2���÷�Ӧ�����ӷ���ʽΪ______________��
��4������Һ����SO2�Ĺ����У�pH��n(SO32-)��n(HSO3-)�仯��ϵ����ͼ��ʾ��
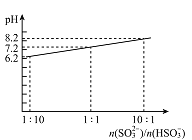
����ͼ�����ݺͱ仯����˵��NaHSO3��Һ�����Ե�ԭ��________________��
��n(SO32-)��n(HSO3-)=1��1ʱ����Һ������Ũ���ɴ�С��˳����_____________��
��5��������Һ��pH����ԼΪ6ʱ�����������۴�����ֱ���õ�pH>8������Һ��ѭ�����ã�����ʾ��ͼ���£�
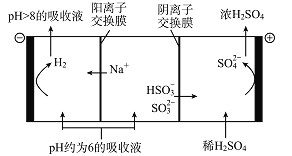
��д�����������ĵ缫��Ӧʽ________________��
�ڵ��缫����2 mol����ת��ʱ�������������Ϊ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и���������ָ����Һ��һ���ܴ����������
A.��Ư��Һ(����������Һ)�У�Ag+��K+��NO3-��SO32-
B.������Һ��K+��NO3-��Br-��Fe3+
C.![]() =1012����Һ�У�NH4+��Ca2+��Cl-��NO3-
=1012����Һ�У�NH4+��Ca2+��Cl-��NO3-
D.��ˮ�����c(H+)=1��10-10mol/L����Һ�У�K+��Na+��HCO3-��Al3+
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com