
【题目】《天工开物》中记载:人贱者短褐、枲裳,冬以御寒,夏以蔽体,其质造物之所具也。属草木者,为枲、麻、苘、葛,属禽兽与昆虫者为裘褐、丝绵。各载其半,而裳服充焉矣。文中的“枲、麻、苘、葛”和“裘褐、丝绵”分别属于( )
A. 纤维素、油脂B. 糖类、油脂
C. 纤维素、蛋白质D. 单糖、蛋白质
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】TK时,向2.0L恒容密闭容器中充入0.10molCOCl2,发生反应COCl2(g)![]() Cl2(g)+CO(g)经过一段时间后反应达到平衡。反应过程中测得的部分数据见下表,下列说法正确的是:
Cl2(g)+CO(g)经过一段时间后反应达到平衡。反应过程中测得的部分数据见下表,下列说法正确的是:
t/s | 0 | 2 | 4 | 6 | 8 |
n(Cl2)/mol | 0 | 0.030 | 0.039 | 0.040 | 0.040 |
下列说法正确的是
A. TK时该反应的化学平衡常数为1/75
B. 反应在前2s的平均速度v(CO)=0.015mol·L-1·s-
C. 保持其他条件不变,升高温度,平衡时c(Cl2)=0.022molL-1,则反应的△H<0
D. 平衡后向上还容器中再充入0.10molCOCl2,平衡正向移动,COCl2的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用丁烷催化脱氢侧备丁烯:C4H10(g)![]() CH4(g)+H2(g)(正反应吸热)。将丁烷和氢气以一定的配比通过填充有催化剂的反应器(氢气的作用是活化催化剂),反应的平衡转化率、产率与温度、投料比有关。下列判断不正确的是
CH4(g)+H2(g)(正反应吸热)。将丁烷和氢气以一定的配比通过填充有催化剂的反应器(氢气的作用是活化催化剂),反应的平衡转化率、产率与温度、投料比有关。下列判断不正确的是
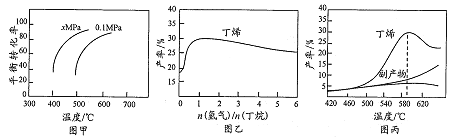
A. 由图甲可知,x小于0.1
B. 由图乙可知,丁烯产率先增大后减小,减小的原因是氢气是产物之一,随着n(氢气)/n(丁烷)增大,逆反应速 率减小
C. 由图丙可知产率在590℃之前随温度升高面增大的原因可能是溫度升高平衡正向移动
D. 由图丙可知,丁烯产率在590℃之后快速降低的主要原因为丁烯高温分解生成副产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应式:①Fe+Cu2+═Fe2++Cu ②2Fe3++Cu═2Fe2++Cu2+可判断离子的氧化性从强到弱的顺序是( )
A. Fe2+、Fe3+、Cu2+ B. Fe2+、Cu2+、Fe3+
C. Cu2+、Fe2+、Fe3+ D. Fe3+、Cu2+、Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含有Fe2+、Al3+、NO3-、NH4+的溶液中先加入过量金属钠,有气体和沉淀生成,然后再加入过量的稀硝酸使沉淀溶解,最终离子数一定不变的是
A.Fe2+B.Al3+C.NO3-D.NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F六种常见化合物,已知它们包含的阳离子有K+、Ag+、Na+、Ba2+、Fe2+、Al3+,阴离子有Cl-、OH-、AlO2-、NO3-、SO42-、CO32-。将它们分别配成0.1mol·L-1的溶液进行如下实验:
①测得A、C、E溶液均呈碱性,且碱性A>E>C,E的焰色呈浅紫色(透过蓝色钴玻璃观察);②向B溶液中滴加稀氨水至过量,先生成沉淀,后沉淀全部溶解;③向F溶液中滴加稀硝酸,溶液变成棕黄色,且有无色气体生成;④向D溶液中滴加Ba(NO3)2溶液,无明显现象。
(1)写出A、D、E、F的化学式:A.________;D.________;E._______;F.________。
(2)用离子方程式解释C溶液呈碱性的原因:____________________________________。
(3)写出实验③中反应的离子方程式: ___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:_____H2O2 +___Cr2(SO4)3 +_______KOH=________K2CrO4 +________K2SO4 +_______H2O
(1)配平该方程式,并用单线桥法表示电子转移情况。
(2)此反应中氧化剂是__________。
(3)若消耗1molL-1Cr2(SO4)3溶液的体积为50mL,则转移电子的物质的量是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中正确的是( )
A.过滤操作时,用玻璃棒搅拌漏斗内的液体,以加速过滤
B.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,可以选用酒精作为萃取剂从碘水中萃取碘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Fe3O4可表示成(FeO·Fe2O3),水热法制备Fe3O4纳米颗粒的总反应为:
3Fe2++2S2O![]() +O2+4OH-=Fe3O4+S4O62-+2H2O,下列说法正确的是( )
+O2+4OH-=Fe3O4+S4O62-+2H2O,下列说法正确的是( )
A. O2和S2O![]() 是氧化剂,Fe2+是还原剂
是氧化剂,Fe2+是还原剂
B. 每生成1mol Fe3O4,则转移电子数为2mol
C. 参加反应的氧化剂与还原剂的物质的量之比为1﹕1
D. 若有2mol Fe2+被氧化,则被Fe2+还原的O2为0.5mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com