
【题目】某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
时间(min) | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL)(标况下) | 50 | 120 | 232 | 290 | 310 |
⑴ 哪一时间段(指①0~1、②1~2、③2~3、④3~4、⑤4~5 min,下同)反应速率最大______ (填序号,下同),原因是_____________________________ 。
⑵ 哪一段时段的反应速率最小______,原因是________________________。
⑶ 求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变,不要求写出计算过程)_________________ 。
⑷ 如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液: A..蒸馏水 B.KNO3溶液 C. NaCl溶液 D.CuSO4溶液
你认为可行的是(填编号) _______________________ 。
【答案】 ③ 该反应放热,2-3min时温度最高 ⑤ 溶液中H+的浓度变小了 0.1mol·L-1·min-1 AC
【解析】试题分析:⑴计算每个时间段生成气体的体积,根据相同条件下气体体积与反应速率的关系判断速率,根据反应与能量变化的关系判断速率变化的原因;(2)计算每个时间段生成气体的体积,根据相同条件下气体体积与反应速率的关系判断速率,根据反应与能量变化的关系判断速率变化的原因;(3)先求出气体的物质的量,再计算盐酸变化的物质的量,利用速率计算公式计算速率;⑷根据浓度、电解质的强弱判断。
解析:0~1、②1~2、③2~3、④3~4、⑤4~5 min生成氢气的体积分别是50 mL、70 mL、112 mL、58 mL、20mL;
⑴ 相同条件下,反应速率最大,相同时间收集到气体体积越大,所以2~3 min反应速率最快,原因是该反应放热,2-3min时温度高与开始时的温度;⑵4~5 min的反应速率最小,原因是液中H+的浓度变小了;⑶ 2~3分钟时间段以生成氢气的体积是112mL,
设需要盐酸的物质的量是x mol,
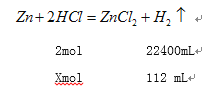
![]() x=0.01mol
x=0.01mol
![]() mol·L-1·min-1;
mol·L-1·min-1;
⑷ 改变反应速率的方法有:改变浓度、改变温度、改变固体表面积等;
A..蒸馏水,盐酸浓度变小,反应速率减慢,产生氢气的量不变,故A正确; B.加入KNO3溶液生成硝酸,硝酸具有强氧化性,不能生成氢气,故B错误; C. 加入NaCl溶液,盐酸体积增大,浓度减小 ,反应速率减慢,产生氢气的量不变,故C正确; D.CuSO4溶液,形成铜锌原电池,加快反应速率,故D错误。


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】下列有关烯烃的说法中,正确的是
A. 烯烃分子中所有的原子一定在同一平面上
B. 烯烃在适宜的条件下只能发生加成反应不能发生取代反应
C. 分子式是C4H8的烃分子中一定含有碳碳双键
D. 通过石油的催化裂化及裂解可以得到气态烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定实验室长期存放的Na2SO3固体的纯度,准确称取W g固体样品,配成250 mL溶液。设计了以下两种实验方案:
方案I:取25.00 mL上述溶液→加入足量的盐酸酸化的BaCl2溶液→操作I→洗涤→操作Ⅱ→称量,得到沉淀的质量为m1 g
方案Ⅱ:取25.00 mL上述溶液,用a mol/L 的酸性KMnO4溶液进行滴定。(5SO32-+2MnO4-+6H+→5SO42-+2Mn2++3H2O)
实验中所记录的数据如下表:
滴定次数 实验数据 | 1 | 2 | 3 | 4 |
待测溶液体积/mL | 25.00 | 25.00 | 25.00 | 25.00 |
滴定管初读数/mL | 0.00 | 0.20 | 0.10 | 0.15 |
滴定管末读数/mL | 20.95 | 21.20 | 20.15 | 21.20 |
(1)配制250 mL Na2SO3溶液时,必须用到的实验仪器有:烧杯、玻棒、滴管、药匙和__________________、_________________。
(2)操作I为____________________操作Ⅱ为________________
(3)方案I中如何判别加入的氯化钡已经过量_____________在方案Ⅱ中滴定终点的判断方法是________________。
(4)根据方案Ⅱ所提供的数据,计算Na2SO3的纯度为______________。(写成分数形式)有同学模仿方案I,提出方案Ⅲ:取25.00 mL上述溶液→加入足量的盐酸酸化的Ba(NO3)2溶液→操作I→洗涤→操作Ⅱ→称重,得到沉淀质量为m2 g 并用方案I的方法计算结果。
(5)根据方案Ⅲ,从理论上讲,下列说法正确的是________(填序号)
a. 方案I比方案Ⅲ的计算结果要低
b. 方案I比方案Ⅲ的计算结果要高
c. m1=m2 ,方案I和方案Ⅲ的结果一样
d. 方案Ⅲ不应根据方案I的方法计算
(6)上述实验中,由于操作错误所引起的实验误差分析正确的是__________(填序号)。
a. 方案I中如果没有洗涤操作,实验结果将偏小
b. 方案I中如果没有操作Ⅱ,实验结果将偏大
c. 方案Ⅲ中如果没有洗涤操作,实验结果将偏小
d. 方案Ⅲ中如果没有操作Ⅱ,实验结果将偏大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.甲烷—空气燃料电池若以KOH溶液为电解质溶液,负极的电极反应式为______________;若以稀硫酸为电解质溶液,正极的电极反应式为 __________________________。
Ⅱ.现有纯铁片、纯银片、纯铜片,稀硫酸、FeSO4溶液、Fe2(SO4)3溶液、大烧杯、导线若干,请运用原电池原理设计实验,验证Cu2+、Fe3+的氧化性强弱。
(1)写出电极反应式,负极:__________________,正极:___________________。
(2)请在下面方框中画出原电池的装置图,标出外电路电子流向(注明电极材料、电解质溶液,连成闭合回路)________。

该装置反应一段时间后,当溶液的质量增加3.2 g时,通过导线的电子的数目是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作的叙述错误的是( )
A.过滤操作中,玻璃棒应适时搅拌漏斗器
B.蒸发时,不能把蒸发皿放置于石棉网上加热
C.萃取分液时,将塞上凹槽或小孔对准漏斗上小孔,然后打开活塞才能放出下层液体
D.配制容量瓶,定容时改用胶头滴管滴加蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置可以测定铜锌原电池工作时转移电子的物质的量,假设量筒的量程足够大,锌片和 铜片中无杂质,气体体积已转换为标准状况。下列说法正确的是 ( )

A. a 电极的电极材料是铜
B. 如果将稀硫酸换为 CuSO4 溶液,则不能达到实验目的
C. 锌与稀硫酸反应时放出的热量对实验测定不产生影响
D. 若量筒中收集到 a L H2,则电解质溶液中通过了![]() mol 电子
mol 电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应
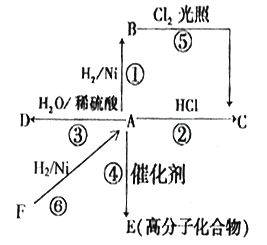
根据上图回答下列问题:
(1)写出A和D的结构简式:A______________,D________________。
(2)写出②⑤两步反应的化学方程式,其中②属于______反应。
②_______________________;
⑤_______________________。
(3)写出实验室中制取F的化学方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是( )
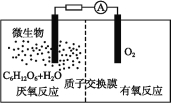
A.正极反应中有CO2生成
B.微生物促进了反应中电子的转移
C.质子通过交换膜从负极区移向正极区
D.电池总反应为C6H12O6+6O2=6CO2+6H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com